- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к открытому уроку по химии по теме: Растворы. Растворение (8 класс)
Содержание
- 1. Презентация к открытому уроку по химии по теме: Растворы. Растворение (8 класс)
- 2. Задание 1. Напишите уравнение реакции, укажите ее
- 3. CuSO4 +Fe=FeSO4 + Cu (замещения)KCl + AgNO3=KNO3+AgCl (обмена)CaCO3+2HCl=CaCl2+H2CO3 (обмена)
- 4. Как-то утром я проспал. в школу быстро собирался: Чай
- 5. Тема урока: Растворение. Типы растворов.
- 6. Цель урока: Дать определения понятия раствор, изучить типы растворов,изучить факторы, влияющие на растворимость веществ в воде.
- 7. К какому физическому или химическому процессу относится процесс растворения?
- 8. 1. Теории растворовФизическаяЯ. Х. Вант-Гофф,
- 9. Выделение теплоты – разбавление серной кислоты – http://files.school-collection.edu.ru/dlrstore/f49172af-18e9-8812-9c38-5b58785c7bd5/index.htm
- 10. Гидраты – непрочные соединения веществ с водой,
- 11. Растворение безводного сульфата
- 12. CuSO4 . 5H2O – медный купоросCuSO4 Раствор CuSO4 в воде
- 13. Современная теория растворовРастворение – физико-химический процесс.Раствор –
- 14. Почему у различных веществ разная растворимость? От чего она зависит?
- 15. 2. Факторы, от которых зависит растворимость веществ
- 16. Слайд 16
- 17. Задание1:Определите растворимость ВаCl при t° по графику
- 18. ВаСI
- 19. 3. Типы растворов по содержанию растворенного
- 20. ω=mв-ваmр-ра.100 %4. Концентрация растворовМассовая
- 21. . Какова растворимость хлорида калия при 30
- 22. (40 г)(20 г)(при 90 0С)(сульфата магния)
- 23. Домашнее задание § 35, упр. 2,5
- 24. СПАСИБО ЗА УРОК!
Слайд 2Задание 1. Напишите уравнение реакции, укажите ее тип.
Сульфат меди (II) вступает
Хлорид калия реагирует с нитратом серебра.
Карбонат кальция реагирует с соляной кислотой.
«Химическая разминка»
Слайд 3CuSO4 +Fe=FeSO4 + Cu (замещения)
KCl + AgNO3=KNO3+AgCl (обмена)
CaCO3+2HCl=CaCl2+H2CO3 (обмена)
Слайд 4
Как-то утром я проспал.
в школу быстро собирался:
Чай холодный наливал,
Сахар всыпал, помешал,
Но не сладким
Слайд 6Цель урока:
Дать определения понятия раствор,
изучить типы растворов,
изучить факторы, влияющие
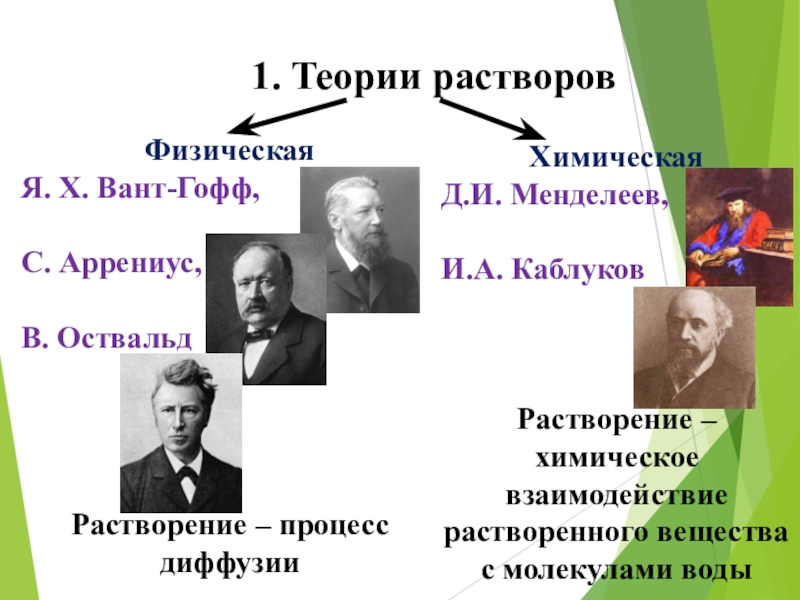
Слайд 8 1. Теории растворов
Физическая
Я. Х. Вант-Гофф,
С. Аррениус,
В. Оствальд
Растворение
Химическая
Д.И. Менделеев,
И.А. Каблуков
Растворение – химическое взаимодействие растворенного вещества с молекулами воды
Слайд 9Выделение теплоты – разбавление серной кислоты – http://files.school-collection.edu.ru/dlrstore/f49172af-18e9-8812-9c38-5b58785c7bd5/index.htm
Слайд 10Гидраты – непрочные соединения веществ с водой, существующие в растворе
Кристаллогидраты –
(кристаллизационная)
Слайд 11 Растворение безводного сульфата меди (Растворение безводного сульфата меди (IIРастворение безводного сульфата
Слайд 13Современная теория растворов
Растворение – физико-химический процесс.
Раствор – однородная система переменного состава,
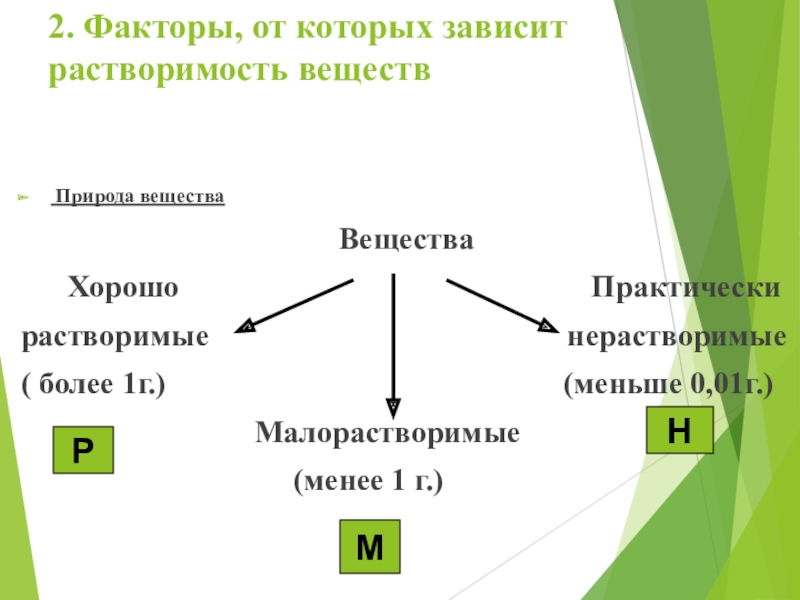
Слайд 152. Факторы, от которых зависит растворимость веществ
Природа вещества
Вещества
растворимые нерастворимые
( более 1г.) (меньше 0,01г.)
Малорастворимые
(менее 1 г.)
Р
Н
М
Слайд 16
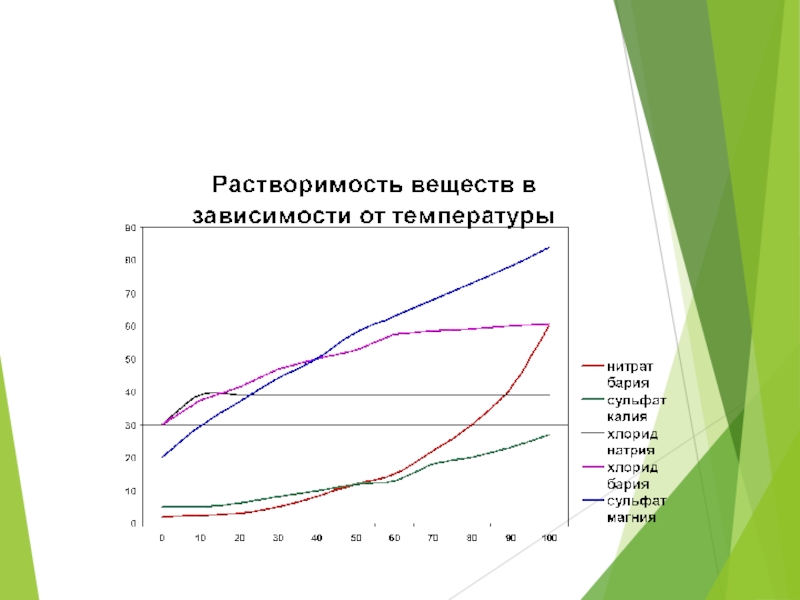
Температура
С повышением температуры растворимость
твердых веществ увеличивается, газообразных - уменьшается
Слайд 17Задание1:
Определите растворимость ВаCl при t° по графику на с. 213:
10 °
30
80 °
Задание2:
Определить растворимость NaCl при t° по графику:
10 °
30 °
80 °
Слайд 193. Типы растворов
по содержанию растворенного вещества
Насыщенный раствор – раствор, в
Ненасыщенный раствор – раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе
Пересыщенный раствор – раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях.
Слайд 20 ω=
mв-ва
mр-ра
.
100 %
4. Концентрация растворов
Массовая доля
растворенного вещества в
Задача. Для консервирования огурцов приготовили рассол: на 2 л воды взяли 100г соли, а для консервирования томатов – рассол из 100г соли и 3 л воды. Какой рассол получится более концентрированным?
Слайд 21. Какова растворимость хлорида калия при 30 0С?
2. Какова растворимость
3. При какой температуре в 100 г воды может раствориться 60 г хлорида бария?
4. Растворимость какого вещества при 55 0С составляет 60 г на 100 г воды?
Закрепление