ход развития
человеческой цивилизации.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к нетрадиционному уроку по химии на тему Общие способы получения металлов 9, 11 класс
Содержание
- 1. Презентация к нетрадиционному уроку по химии на тему Общие способы получения металлов 9, 11 класс
- 2. Знать-общие способы получения металлов-проблемы экологии-источники металлов вприродеПонимать-химизм процессов получения металлов
- 3. Медь, серебро, золото – самородные металлыКиноварь, галенит, касситерит – природные соединения легкоплавких металлов (ртути, свинца. олова)CuAgAuHgSPbSSnS
- 4. Пирит FeS2Красный железняк Fe2O3Метеорит FeНекоторые соединения железа
- 5. Минера́л — однородная по составу и строению
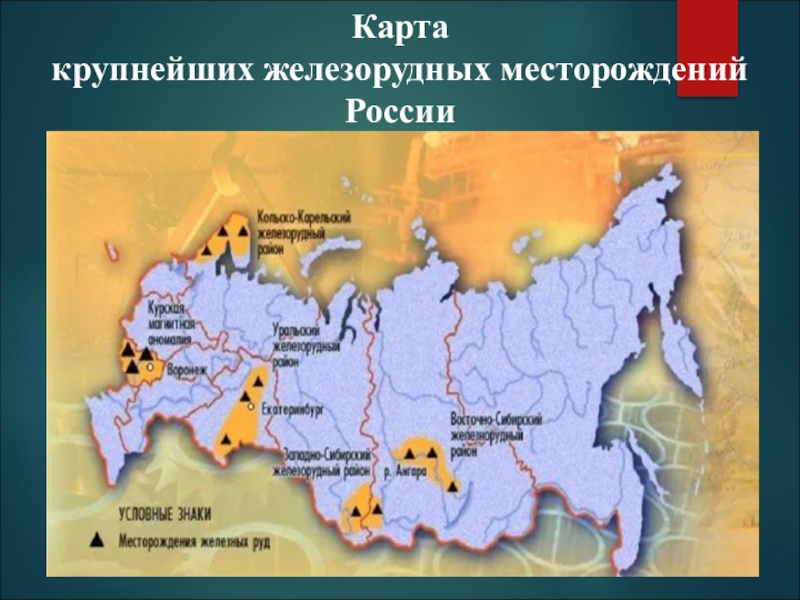
- 6. Карта крупнейших железорудных месторождений Россиит
- 7. Сыродутный способ получения железа
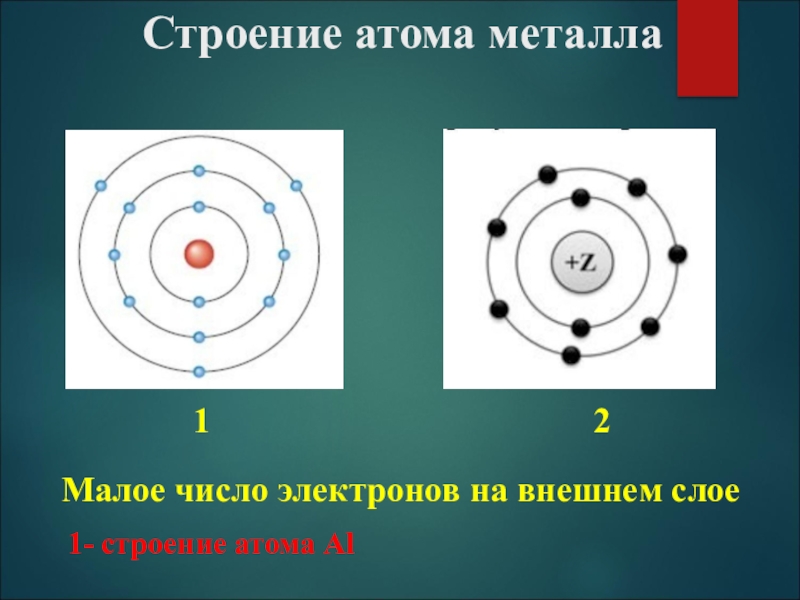
- 8. Строение атома металла1
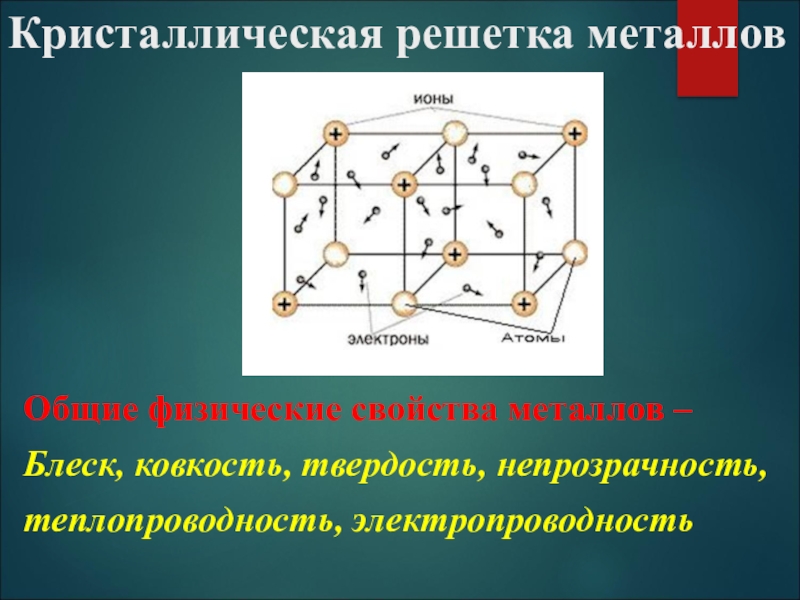
- 9. Кристаллическая решетка металловОбщие физические свойства металлов –Блеск, ковкость, твердость, непрозрачность,теплопроводность, электропроводность
- 10. Общие способы получения металлов1.Пирометаллургический – используется огонь2.Гидрометаллургический – используются растворы3.Электрометаллургический – с помощью электрического тока.
- 11. ПирометаллургияВосстановители СО, С, Н2, АL, MgСульфиды переводят
- 12. Слайд 12
- 13. Плавильные печи для получения сплавов железаДоменная печь (чугун)Мартеновская печь (чугун, сталь)Индукционная печь (сталь)
- 14. ГидрометаллургияГидрометаллурги́я — выделение металлов из руд,
- 15. Электрометаллургия (электролиз)Расплав NaClNa(+) + e = Na(0)
- 16. Биологическая роль металловИоны Na участвуют в сохранении
- 17. Проблемы экологии
- 18. Слайд 18
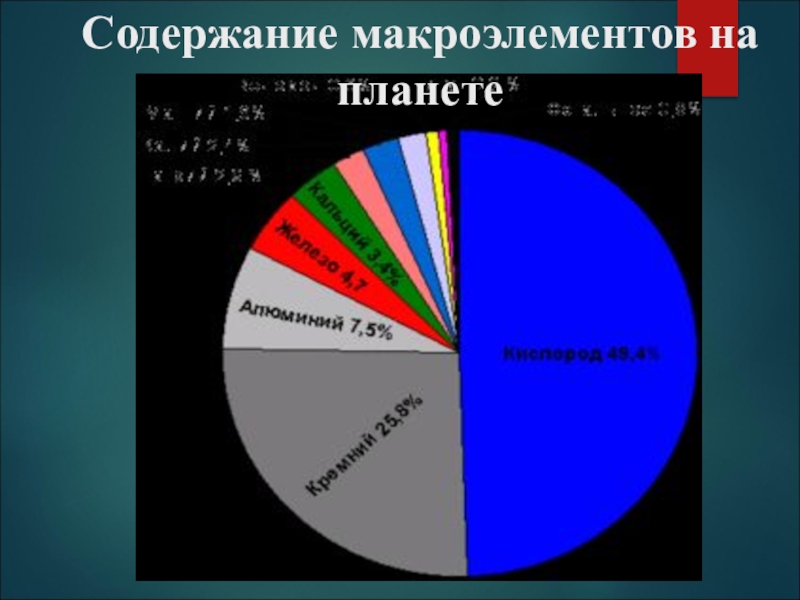
- 19. Содержание макроэлементов на планете
- 20. Вы узнали и поняли -общие способы получения металлов-проблемы экологии-источники металлов в природе-химизм процессов производства металлов
- 21. СПАСИБО ЗА ВНИМАНИЕ
Знать-общие способы получения металлов-проблемы экологии-источники металлов вприродеПонимать-химизм процессов получения металлов
Слайд 1ТЕМА УРОКА
«ОБЩИЕ СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛОВ»
В.И. Вернадский считал, что
металлы позволили изменить
Слайд 2
Знать
-общие способы получения металлов
-проблемы экологии
-источники металлов вприроде
Понимать
-химизм процессов
получения металлов
Слайд 3
Медь, серебро, золото – самородные металлы
Киноварь, галенит, касситерит –
природные соединения
легкоплавких металлов
(ртути, свинца. олова)
(ртути, свинца. олова)
Cu
Ag
Au
HgS
PbS
SnS
Слайд 5
Минера́л — однородная по составу и строению часть горных пород, руд,
метеоритов, являющаяся естественным продуктом геологических процессов и представляющая собой химическое соединение или химический элемент.
Горные породы — это природные тела, состоящие из нескольких минералов
Руда́ — вид полезных ископаемых, природное минеральное образование, содержащее соединения полезных компонентов в концентрациях, делающих извлечение этих компонентов экономически целесообразным.
Горные породы — это природные тела, состоящие из нескольких минералов
Руда́ — вид полезных ископаемых, природное минеральное образование, содержащее соединения полезных компонентов в концентрациях, делающих извлечение этих компонентов экономически целесообразным.
Слайд 9Кристаллическая решетка металлов
Общие физические свойства металлов –
Блеск, ковкость, твердость, непрозрачность,
теплопроводность, электропроводность
Слайд 10Общие способы получения металлов
1.Пирометаллургический – используется огонь
2.Гидрометаллургический – используются растворы
3.Электрометаллургический –
с помощью электрического тока.
Слайд 11Пирометаллургия
Восстановители СО, С, Н2, АL, Mg
Сульфиды переводят в оксиды
2FeS2 +
5O2 = 2FeO + 4SO2
Восстанавливают оксиды
2Fe2O3 + 3C = 2Fe +3CO2
Fe2O3 + 3CO = 2Fe + 3CO2
Al2O3 + 3H2 = 2Al + 3H2O
Алюмо-магний термия
Fe2O3 + 3Mg = 2Fe + 3MgO
Этими способами получают железо и некоторые
цветные металлы (Zn,Ti, Mo, Pb)
Восстанавливают оксиды
2Fe2O3 + 3C = 2Fe +3CO2
Fe2O3 + 3CO = 2Fe + 3CO2
Al2O3 + 3H2 = 2Al + 3H2O
Алюмо-магний термия
Fe2O3 + 3Mg = 2Fe + 3MgO
Этими способами получают железо и некоторые
цветные металлы (Zn,Ti, Mo, Pb)
Слайд 13Плавильные печи для получения сплавов железа
Доменная печь (чугун)
Мартеновская печь (чугун, сталь)
Индукционная
печь (сталь)
Слайд 14Гидрометаллургия
Гидрометаллурги́я — выделение металлов из руд,
с помощью водных растворов.
1
стадия - перевод оксидов (сульфидов) в раствор
CuS +2HCl = CuCl2 + H2S
2 стадия – восстановление из раствора более активным
металлом
CuCl2 + Fe = FeCl2 + Cu
Получают
Cu, Ni, Cd, Co, Ag, Au
и другие цветные металлы
CuS +2HCl = CuCl2 + H2S
2 стадия – восстановление из раствора более активным
металлом
CuCl2 + Fe = FeCl2 + Cu
Получают
Cu, Ni, Cd, Co, Ag, Au
и другие цветные металлы
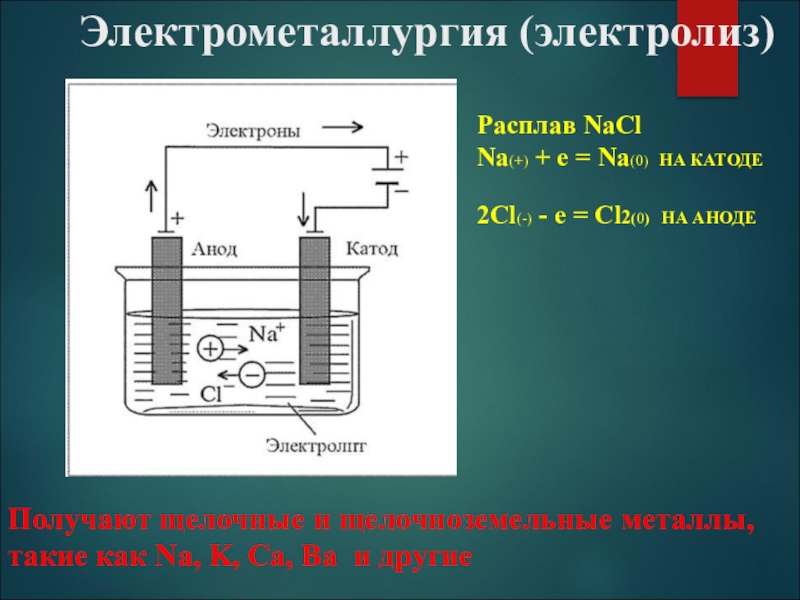
Слайд 15Электрометаллургия (электролиз)
Расплав NaCl
Na(+) + e = Na(0) НА КАТОДЕ
2Cl(-) - e
= Cl2(0) НА АНОДЕ
Получают щелочные и щелочноземельные металлы,
такие как Na, K, Ca, Ba и другие
Слайд 16Биологическая роль металлов
Ионы Na участвуют в сохранении кислотно-основного баланса в организме
животных и человека, в регуляции сердечной деятельности (успокаивают), удерживают воду в организме.
Ионы K регулируют белковый и углеводный обмен, влияют на процесс фотосинтеза и рост растений.
Ионы Ca необходимы для процессов кроветворения, обмена веществ, уменьшения проницаемости сосудов (они препятствуют проникновению микроорганизмов в кровь), для нормального роста костей (скелета, зубов).
Ионы Mg определяют зеленый цвет растений и участвуют в фотосинтезе. У человека синтезируют белок.
Ионы Fe определяют красный цвет крови и способствуют транспортировки кислорода гемоглобином.
Ионы K регулируют белковый и углеводный обмен, влияют на процесс фотосинтеза и рост растений.
Ионы Ca необходимы для процессов кроветворения, обмена веществ, уменьшения проницаемости сосудов (они препятствуют проникновению микроорганизмов в кровь), для нормального роста костей (скелета, зубов).
Ионы Mg определяют зеленый цвет растений и участвуют в фотосинтезе. У человека синтезируют белок.
Ионы Fe определяют красный цвет крови и способствуют транспортировки кислорода гемоглобином.
Слайд 20Вы узнали и поняли
-общие способы получения металлов
-проблемы экологии
-источники металлов в
природе
-химизм процессов производства металлов
-химизм процессов производства металлов