Автор: Шишлянникова Людмила Петровна, учитель химии МБОУ «Бондаревская СОШ»
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к Мастер - классу Развитие приёмов логического мышления учащихся на уроках химии с использованием игровых технологий
Содержание
- 1. Презентация к Мастер - классу Развитие приёмов логического мышления учащихся на уроках химии с использованием игровых технологий
- 2. ЭТАП ТЕОРЕТИЧЕСКИЙРазвивать логическое мышление учащихся в процессе
- 3. анализ, синтез, обобщения, абстрагирование, формирую через различные
- 4. Найди ошибкуВ каком уравнении неправильно расставлены коэффициенты?а)
- 5. Составить как можно больше химических формул из
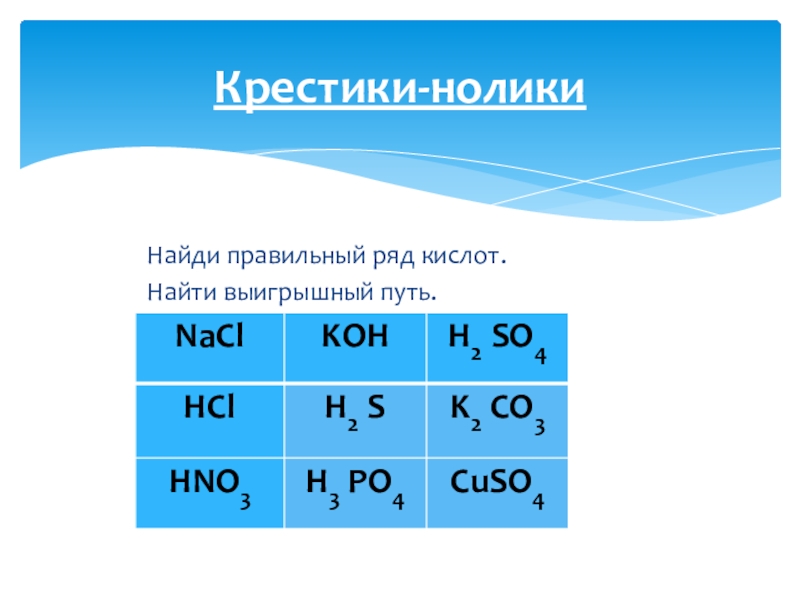
- 6. Найди правильный
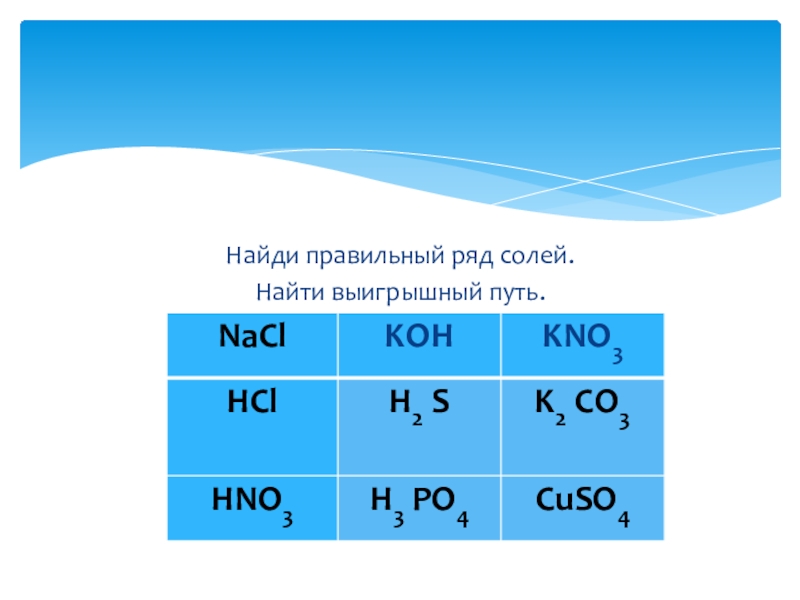
- 7. Найди правильный ряд солей.Найти выигрышный путь.
- 8. если речь о кислотах, то учащиеся поднимают
- 9. СО2, К2SO3, SO2ВаSO4, NaOH, CaCO3RbOH, ZnCl2, LiOHFe(OH)2, KOH, Cu(OH)2BaO, P2O5, CaOHNO3, H2SiO3, H2SO4 Игра «третий лишний».
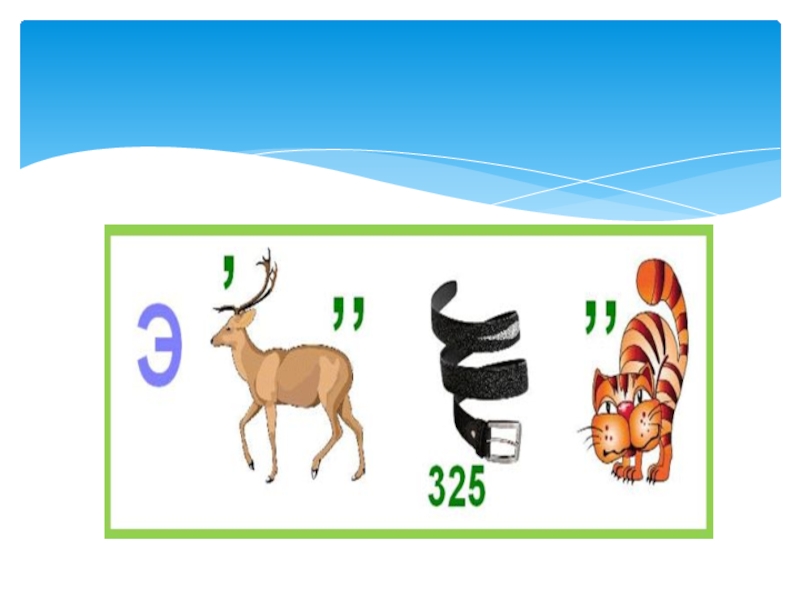
- 10. Ребусы
- 11. Слайд 11
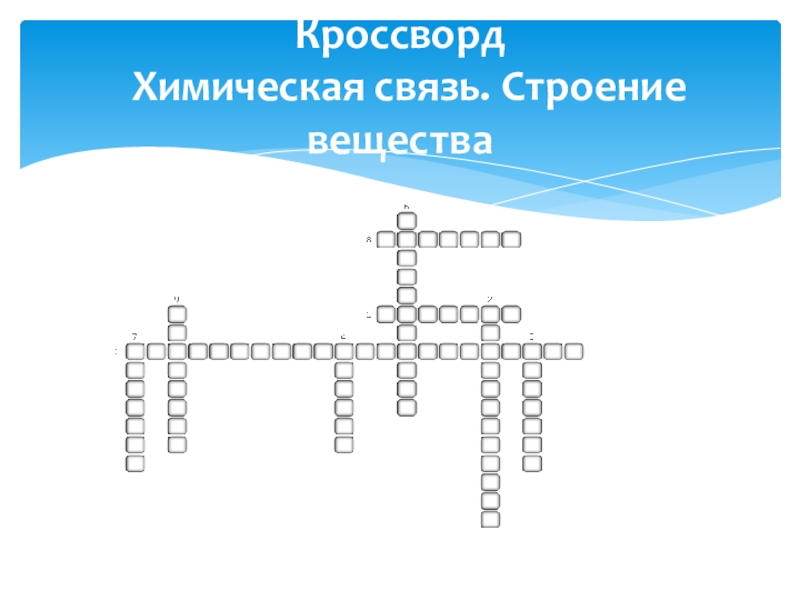
- 12. Кроссворд Химическая связь. Строение вещества
- 13. 1. Кристаллическая структура, характеризующаяся правильным расположением частиц
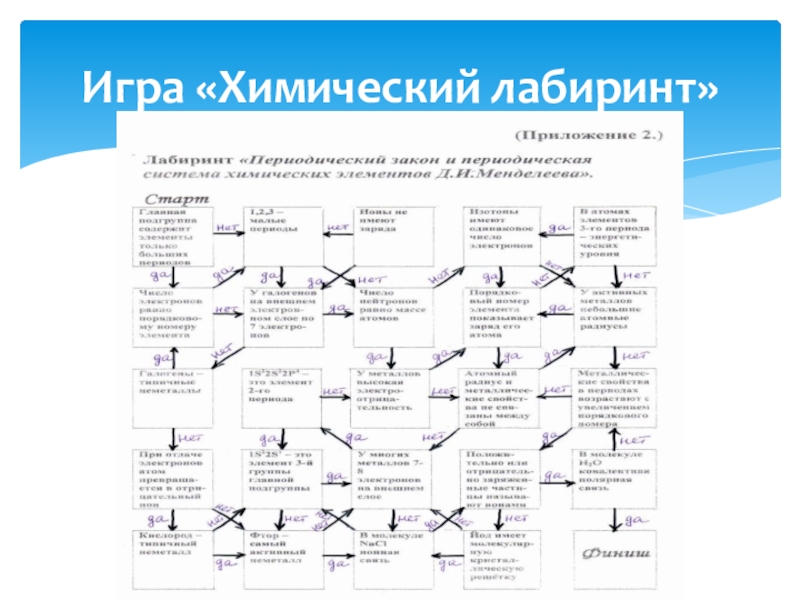
- 14. Игра «Химический лабиринт»
- 15. Активное мышление возникает тогда, когда возникает проблема.
- 16. II ЭТАП ПРАКТИЧЕСКИЙКакие из перечисленных явлений относятся
- 17. По горизонтали:1. Коль хлор в конце формулы
- 18. Цели: образовательные:– формирование представлений об оксидах; воспитательные:
- 19. Слайд 19
- 20. Первое – вода – жидкость, без которой
- 21. Слайд 21
- 22. Оксиды – сложные вещества, состоящие из двух
- 23. Волшебный цветок - ромашка
- 24. Выигрышный путь в обоих случаях составляют формулы
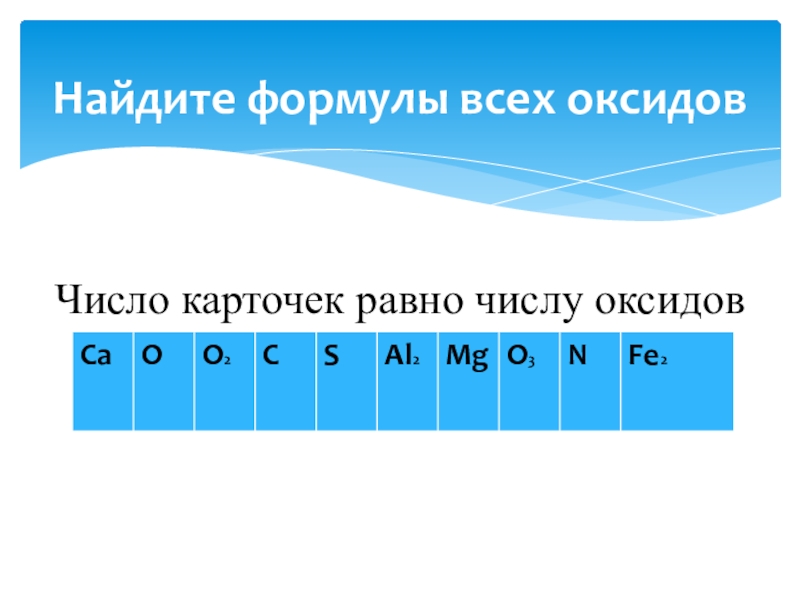
- 25. Найдите формулы всех оксидов, которые можно составить
- 26. СаО, СН4, N2О,
- 27. 1. SО3
- 28. Продолжить предложение:сегодня я узнал… было интересно… было
- 29. Успехов в работе и отличного настроения!
Слайд 1Мастер класс
Развитие приёмов логического мышления учащихся
на уроках химии с
Слайд 2ЭТАП ТЕОРЕТИЧЕСКИЙ
Развивать логическое мышление учащихся в процессе обучения это значит:
развивать умение
учить детей мысленно расчленять (анализировать) предмет на составные части в целях познания каждой составной части и соединять (синтезировать) расчлененные мысленно предметы в одно целое;
вырабатывать умение выделять существенные свойства предметов и отвлекать (абстрагировать) их от второстепенных, несущественных;
учить делать правильные выводы из наблюдений или фактов, уметь проверять эти выводы; прививать умение обобщать эти факты;
развивать у учащихся умение убедительно доказывать истинность своих суждений и опровергать ложные умозаключения;
следить за тем, чтобы мысли учащихся излагались определенно, последовательно, непротиворечиво, обоснованно.
Цель: Ознакомить педагогов с приёмами развития логического мышления и показать использование приемов в своей педагогической деятельности
Слайд 3анализ, синтез, обобщения, абстрагирование,
формирую через различные упражнения: на классификацию,
использование игровых ситуаций:
«Найди соответствие», «Крестики – нолики», «Исправь ошибку», «Третий лишний», «Неоконченный текст»,
КВН, кроссворды, ребусы.
Приёмы логического мышления:
Слайд 4Найди ошибку
В каком уравнении неправильно расставлены коэффициенты?
а) 2P+5O2 = P2O5
б) 2Н2О2 = 2Н2О +
в) 3KOH + Al(NO3)3 = 3КNO3 + Аl(OH)3
г) Mg + 2HCl=MgCl2+ H2
Слайд 5Составить как можно больше химических формул из данных элементов и дать
Ca, C, N, P, O, H, Cu, Al
Игра «Кто больше»
Слайд 8если речь о кислотах, то
учащиеся поднимают левую руку,
если о
Игра « соответствие движению»:
Слайд 9СО2, К2SO3, SO2
ВаSO4, NaOH, CaCO3
RbOH, ZnCl2, LiOH
Fe(OH)2, KOH, Cu(OH)2
BaO, P2O5, CaO
HNO3, H2SiO3, H2SO4
Игра «третий лишний».
Слайд 131. Кристаллическая структура, характеризующаяся правильным расположением частиц в строго определённых точках
2. Распределение электронов по энергетическим уровням, существующим в электронном облаке атома.
3. Условная величина, характеризующая способность атома в молекуле приобретать отрицательный заряд.
4. Один из видов химической связи, в основе которой лежит электростатическое взаимодействие между противоположно заряженными ионами.
5. Условный показатель, характеризующий заряд атома в соединениях.
6. Вид связи, при котором происходит связывание атомов с помощью общих электронных пар.
7. Совокупность атомов с одинаковым зарядом ядра.
8. Запись распределения имеющихся в атоме электронов по энергетическим уровням и подуровням.
9. Устойчивая элементарная частица с элементарным отрицательным электрическим зарядом и массой 9,11 х 10-31 кг.
Слайд 15Активное мышление возникает тогда, когда возникает проблема.
Отсюда одним из условий
Слайд 16II ЭТАП ПРАКТИЧЕСКИЙ
Какие из перечисленных явлений относятся к физическим и какие
1) появление зеленого налета на старинных медных монетах,
2) обращение расплавленного свинца в свинцовую дробь,
3) протухание яиц,
4) появление запаха при открывании флакона с духами,
5) появление зимой инея на деревьях,
6) взрыв пороха,
7) отстаивание мутной воды,
8) прокисание молока,
9) выделение кристаллов сахара при высыхании сахарного раствора (или “осахаривании” варенья) и т.д.
Тема “Химическая реакция”
Слайд 17По горизонтали:
1. Коль хлор в конце формулы стоит, то перед нами
2. Название этого элемента содержит в своем составе хвойное дерево, а атом этого элемента весит 28 а.е.м.
3. Он бесцветный, но тяжелый,
В нем огонь всегда веселый.
Он в крови у нас живет,
Ну, конечно …
4. Назовите науку о веществах и их превращениях
5. Он с морской капустой дружит,
И лекарством людям служит,
Знает млад и стар народ –
Коль ушиб, то нужен …
6. Назовите элемент, в названии которого спряталось сразу двое животных
Кроссворд
Слайд 18Цели:
образовательные:
– формирование представлений об оксидах;
воспитательные:
показать значение важнейших представителей
развивающие:
– развивать коммуникативные умения через работу в парах, группах;
– формировать умения выделять главное, логически излагать материал;
– развивать мыслительную и познавательную деятельность учащихся.
Планируемые результаты:
Личностные:
Развитие самостоятельности, уважения друг к другу, терпимости.
Метапредметные:
Научиться обобщать полученную информацию, классифицировать объекты по предложенным критериям, выполнять учебное задание в соответствии с планом,
оценивать свои учебные достижения.
Предметные:
Давать определение «оксиды», распознавать оксиды среди других веществ, составлять формулы оксидов и называть их.
Оксиды.
Слайд 20Первое – вода – жидкость, без которой немыслимо существование жизни на
Второе вещество – углекислый газ, газ необходимый растениям для фотосинтеза, а значит для питания и жизни.
Третье вещество твердое – оксид меди (II).
Три разных вещества.
Слайд 22Оксиды – сложные вещества, состоящие из двух элементов, один из которых
Название оксида
А) по международной номенклатуре:
Название = «Оксид» + название элемента + степень окисления
Оксида в родительном падеже
её указывают римскими цифрами, взятыми в скобки, после названия химического элемента. Элементы с постоянной степенью окисления – металлы главных подгрупп I, II, III групп. Элементы с переменной степенью окисления – остальные металлы.
Б) тривиальные названия: NO – окись азота, N2O – закись азота.
Слайд 24Выигрышный путь в обоих случаях составляют формулы оксидов.
HNO3 SO2 SO3
CO CuO MnO NaOH SO2 H2SO4
O2 NaOH ZnSO4 Cu(OH)2 N2O3 CO2
Игра в «Крестики нолики»
Слайд 25Найдите формулы всех оксидов, которые можно составить и записать в приведенных
Слайд 27 1. SО3 а.
2. ZnО b. Оксид натрия
3. NО2 с. Оксид серы (VI)
4. SО2 d. Оксид цинка
5. Nа2О е. оксид серы (IV)
«Найди соответствие».
Слайд 28Продолжить предложение:
сегодня я узнал…
было интересно…
было трудно…
я выполнял задания…
я понял, что…
теперь я могу…
я почувствовал, что…
я приобрел…
я научился…
у меня получилось …
я смог…
я попробую…
меня удивило…
урок дал мне для жизни…
мне захотелось…
Рефлексия