- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Ионная связь 8 класс
Содержание
- 1. Презентация Ионная связь 8 класс
- 2. Химическая связьВодороднаяМеталлическаяКовалентнаяИонная
- 3. Слайд 3
- 4. Ионная химическая связь
- 5. Восемь электронов на внешнем уровне предельное число
- 6. Свойства атомов химических элементов изменятся с увеличением порядкового номера
- 7. Ионная химическая связь - связь, образующаяся
- 8. Частица, отдающая электроны, превращается в положительный ион
- 9. Ион – это частица образующаяся в результате
- 10. Механизм образования ионной связи1s22s22p63s11s2s3s2p1s2s3s2p3p1s22s22p63s23p5Na0 – 1e- =Cl0 + 2e- = Na+Cl-хлорид натрия+11Na+17 Cl
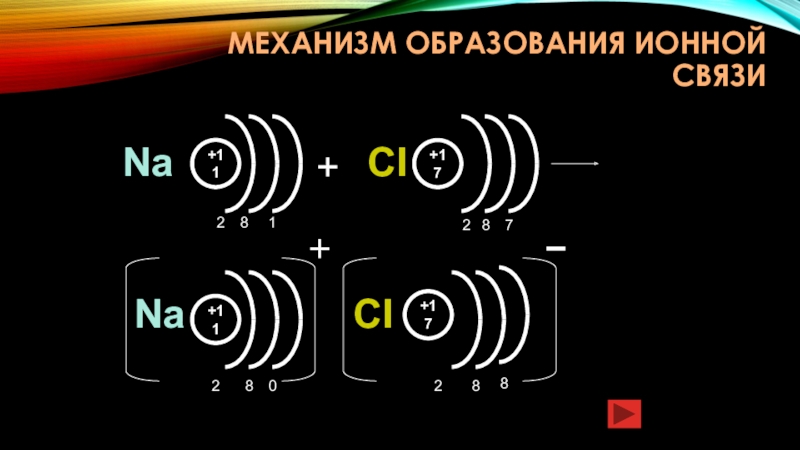
- 11. Механизм образования ионной связи+11082+1782+NaNa+1128CI+177CI2818
- 12. Na+SNaNaS Na[]++2-Механизм образования ионной связи
- 13. Алгоритм (последовательность) действий при записи схемы
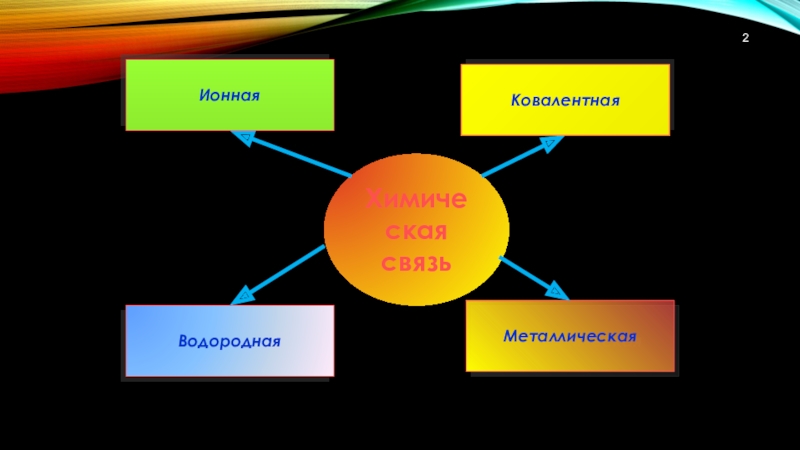
- 14. Типы химических связейИоннаяМеталл – неметаллИоныПереход ē от атомов металлов. к атомам неметалловNaClCa F2 Li2O
- 15. Составьте схемы образования ионной связи между атомами:
- 16. Слайд 16
Слайд 5Восемь электронов на внешнем уровне предельное число для каждого элемента Периодической
Добиваются этого атомы либо отдавая электроны с внешнего уровня, либо принимая
Атомы металлов имеют тенденцию к отдаче электронов с внешнего уровня
Атомы неметаллов имеют тенденцию к принятию электронов недостающих до завершения уровня
Слайд 7 Ионная химическая связь
- связь, образующаяся за счет электростатического притяжения
Эл0 – nе- = Элn+
Эл0 + nе- = Элn-
+
-
-
+
-
ион-катион
-
ион-анион
Слайд 8Частица, отдающая электроны,
превращается в положительный ион (катион)
Частица, принимающая электроны,
превращается в отрицательный ион (анион).
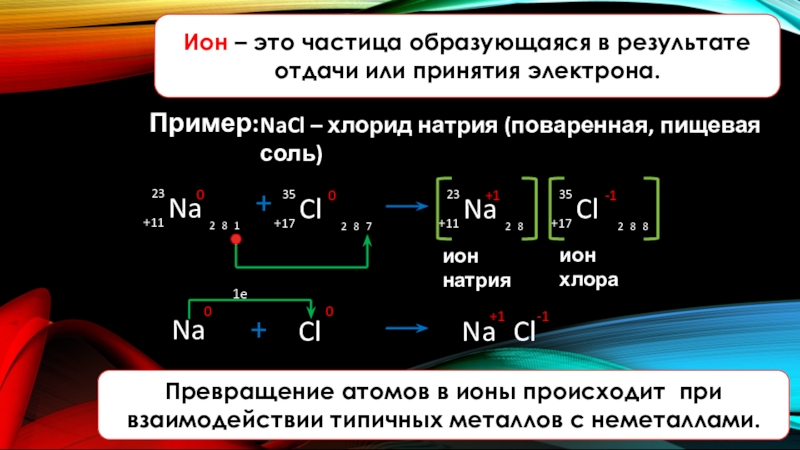
Слайд 9Ион – это частица образующаяся в результате отдачи или принятия электрона.
Пример:
NaCl – хлорид натрия (поваренная, пищевая соль)
+
1e
Превращение атомов в ионы происходит при взаимодействии типичных металлов с неметаллами.
Слайд 10Механизм образования ионной связи
1s22s22p63s1
1s
2s
3s
2p
1s
2s
3s
2p
3p
1s22s22p63s23p5
Na0 – 1e- =
Cl0 + 2e- =
Na+
Cl-
хлорид
+11Na
+17 Cl
Слайд 13Алгоритм (последовательность) действий
при записи схемы образования ионной связи
1.Кальций - элемент
Он отдаёт два электрона.
Ca0 2 е Ca2+
2. Хлор – элемент главной подгруппы VII группы, неметалл.
Он принимает один электрон.
Cl0 + 1е Cl-
3. Находим наименьшее общее кратное между зарядами (равно 2)
4. Определяем, сколько атомов кальция нужно взять, чтобы они отдали два электрона (один атом) и сколько атомов хлора, чтобы они смогли принять 2 электрона (два атома )
5. Составляем схему реакции
2 е
Ca0 + 2Cl0 Ca2+ Cl2-
Слайд 14Типы химических связей
Ионная
Металл
– неметалл
Ионы
Переход ē от
атомов металлов.
к атомам
NaCl
Ca F2
Li2O
Слайд 15Составьте схемы образования ионной связи между атомами:
Ca0 + O0
К0 +
Na0 + O0
Li0 + Cl0
Mg0 + F0







![Презентация Ионная связь 8 класс Na+SNaNaS Na[]++2-Механизм образования ионной связи Na+SNaNaS Na[]++2-Механизм образования ионной связи](/img/tmb/4/379018/e77eb03a3bcac83c1712998fb33c1378-800x.jpg)