- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад интегрированного урока по химии и биологии на тему Строение белков
Содержание
- 1. Презентация интегрированного урока по химии и биологии на тему Строение белков
- 2. С полным основанием можно утверждать, что белки
- 3. Цель:Продолжить изучение органических веществ клетки. Рассмотреть химическийсостав, строение и свойства белков
- 4. План изучения нового материала: 1. Белки
- 5. Молекула белка – макромолекула ( греч.
- 6. В клетке бактерий кишечной палочки - 5
- 7. Содержание белка в некоторых тканях (после
- 8. Химический составВ белке следующие химические элементы: С,
- 9. Белки – это нерегулярные полимеры, мономерами которых
- 10. Состав и классификация белковПо составу различают:протеины, состоящие
- 11. Слайд 11
- 12. Общая формула аминокислотH R1
- 13. Классификация: моноаминокарбоновые, моноаминодикарбоновые, диаминокарбоновые, моноаминотрикарбоновые.
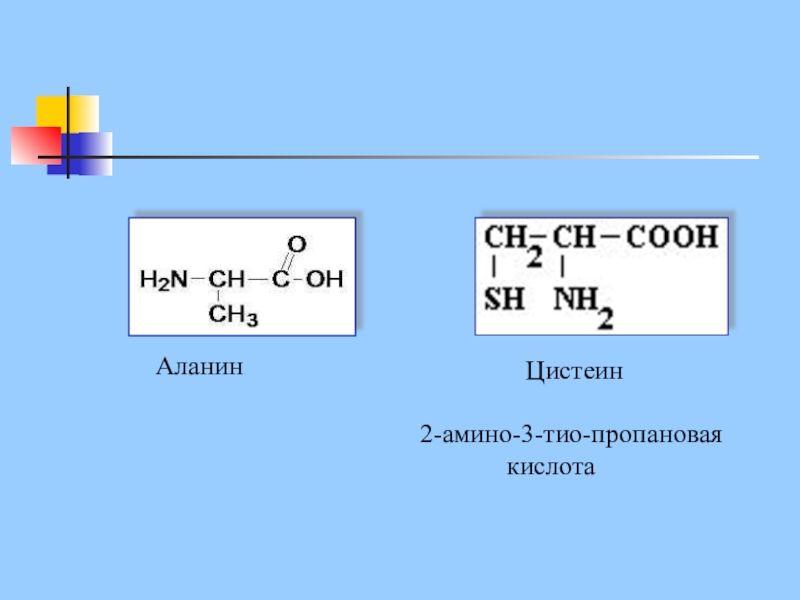
- 14. Аланин
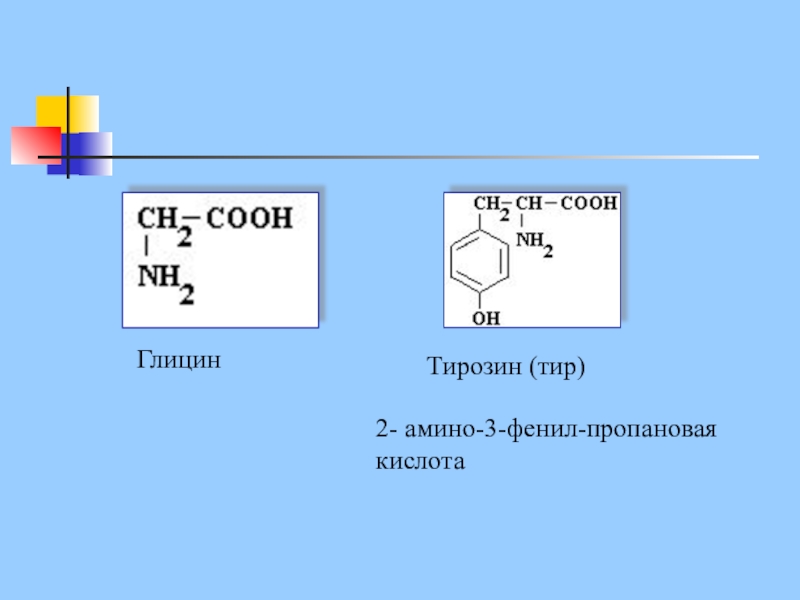
- 15. Глицин Тирозин (тир) 2- амино-3-фенил-пропановая
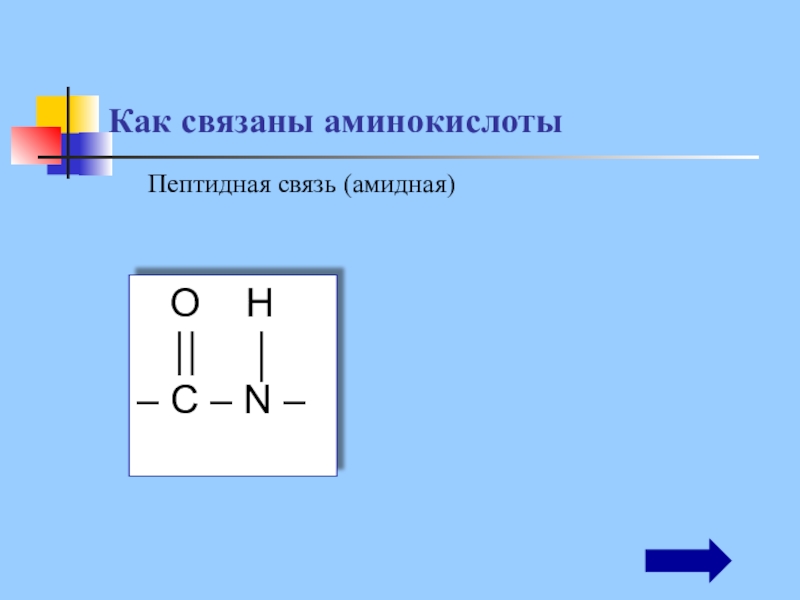
- 16. O H– С –
- 17. Образование дипептидаПри взаимодействии двух аминокислотпроисходит реакция конденсации и образуется пептидная связь
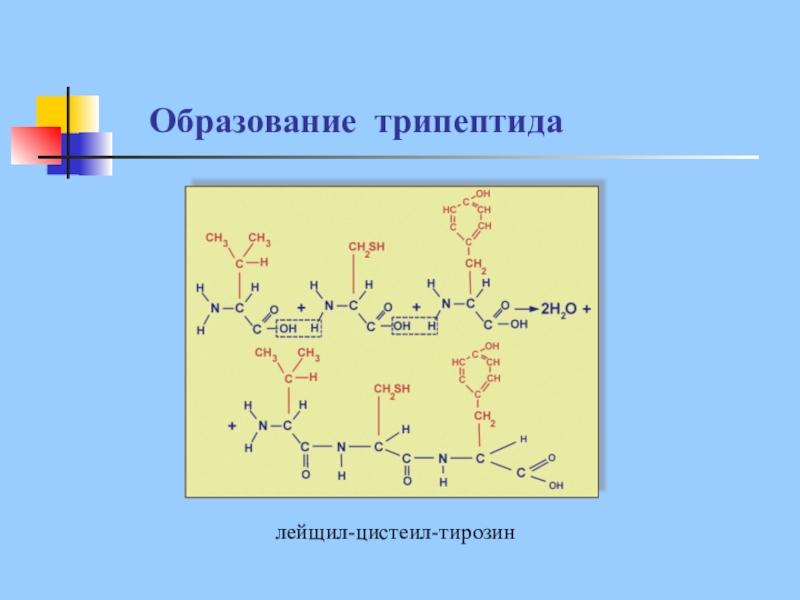
- 18. Образование трипептида лейщил-цистеил-тирозин
- 19. Слайд 19
- 20. Уровни организации белка Размер каждой аминокислоты около
- 21. Первичная структураПервичная структура – полипептидная цепь, в
- 22. Вторичная структура – спираль, поддерживается водородными связями,каждая
- 23. В образовании третичной структуры большая роль принадлежит
- 24. Четвертичная структураЧетвертичная структура – это объединение нескольких
- 25. Свойства белков Чем выше уровень организации
- 26. Свойства белковРастворимость белковГидролиз белковЦветные реакции белков: биуретовая, ксантопртеиноваяАмфотерный характер белковых молекул (амфотерность белков)
- 27. Выводы по уроку:белки – это высокомолекулярные органические
- 28. Домашнее задание: § 11(с.40-43), повторите § 9-10.
С полным основанием можно утверждать, что белки – самые важные из всех веществ, входящих в состав организмов животных и растений.
Слайд 2С полным основанием можно утверждать,
что белки – самые важные из
всех веществ,
входящих в состав организмов животных
и растений.
Л. Полинг
входящих в состав организмов животных
и растений.
Л. Полинг
Слайд 3 Цель:
Продолжить изучение органических
веществ клетки. Рассмотреть химический
состав, строение и
свойства белков
Слайд 4План изучения нового материала:
1. Белки – органические вещества, биополимеры.
2. Аминокислотный состав белков.
3. Химический состав и строение аминокислот.
4. Принцип объединения аминокислотных звеньев в полипептидную молекулу.
5. Пространственные структуры белка.
6. Денатурация и ренатурация белка.
3. Химический состав и строение аминокислот.
4. Принцип объединения аминокислотных звеньев в полипептидную молекулу.
5. Пространственные структуры белка.
6. Денатурация и ренатурация белка.
Слайд 5 Молекула белка – макромолекула ( греч. «Макрос» - большой, гигантский),
обладает большой молекулярной массой
Сравните: молекулярная масса спирта – 46
уксусной кислоты – 60
альбумина (одного из белков яйца) – 36000
гемоглобина – 152000
миозина (белок мышц) – 500000
Сравните: молекулярная масса спирта – 46
уксусной кислоты – 60
альбумина (одного из белков яйца) – 36000
гемоглобина – 152000
миозина (белок мышц) – 500000
Слайд 6В клетке бактерий кишечной палочки - 5 тыс. молекул органических соединений,
из них – 3 тыс. - белки.
В организме человека более 5 мил. белков
В клетке 10-20% сырой массы и 50-80% от сухой массы клетки составляют белки
белки называют протеинами – это название подчёркивает первостепенную роль этих веществ (греч. «протео» - занимаю первое место)
Без белков невозможно представить движение. способность расти, сократимость, размножение
В организме человека более 5 мил. белков
В клетке 10-20% сырой массы и 50-80% от сухой массы клетки составляют белки
белки называют протеинами – это название подчёркивает первостепенную роль этих веществ (греч. «протео» - занимаю первое место)
Без белков невозможно представить движение. способность расти, сократимость, размножение
Слайд 7Содержание белка в некоторых тканях
(после обезвоживания органа):
Мышцы –
80%;
Почки – 72%;
Кожа – 63%;
Печень – 57%;
Мозг – 45%;
Жировая ткань, кости, зубы – 14 – 28%;
Семена растений – 10 – 15 %;
Стебли, корни, листья – 3% - 5%
Плоды – 1-2%
Почки – 72%;
Кожа – 63%;
Печень – 57%;
Мозг – 45%;
Жировая ткань, кости, зубы – 14 – 28%;
Семена растений – 10 – 15 %;
Стебли, корни, листья – 3% - 5%
Плоды – 1-2%
Слайд 8Химический состав
В белке следующие химические элементы: С, Н, О, N, S,
P, Fe.
Железо в гемоглобине крови, фосфор в казеине молока….
Массовая доля элементов:
С – 50% - 55%;
О – 19% - 24%;
Н – 6,5% - 7,3%;
N – 15% – 19%;
S – 0,3% - 2,5%;
P – 0,1% - 2%
Железо в гемоглобине крови, фосфор в казеине молока….
Массовая доля элементов:
С – 50% - 55%;
О – 19% - 24%;
Н – 6,5% - 7,3%;
N – 15% – 19%;
S – 0,3% - 2,5%;
P – 0,1% - 2%
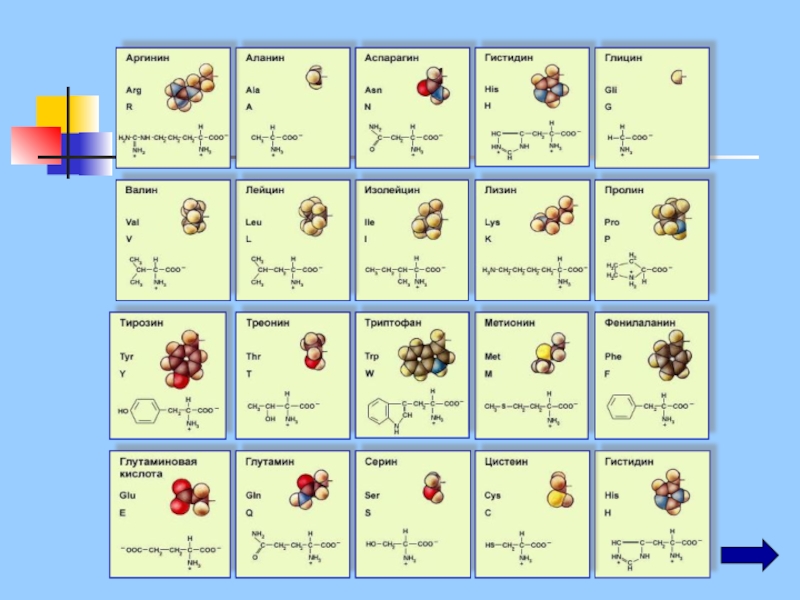
Слайд 9Белки – это нерегулярные полимеры, мономерами которых являются аминокислоты
в природе существует
около 100 α-аминокислот,
в организме встречается 25
в каждом белке 20, из них может быть образовано 2 432 902 008 176 640 000 комбинаций (~2*1018)
заменимые аминокислоты - они могут синтезироваться в организме
незаменимые - в организме не образуются, их получают с пищей (лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, тирозин, метионин)
в организме встречается 25
в каждом белке 20, из них может быть образовано 2 432 902 008 176 640 000 комбинаций (~2*1018)
заменимые аминокислоты - они могут синтезироваться в организме
незаменимые - в организме не образуются, их получают с пищей (лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, тирозин, метионин)
Слайд 10Состав и классификация белков
По составу различают:
протеины, состоящие только аминокислот,
протеиды – содержащие
небелковую часть,
простые белки – состоят из аминокислот,
сложные – могут включать углеводы (гликопротеиды), жиры (липопротеиды), нуклеиновые кислоты (нуклеопротеиды)
полноценные – содержат весь набор аминокислот
неполноценные – какие-то аминокислоты в них отсутствуют
простые белки – состоят из аминокислот,
сложные – могут включать углеводы (гликопротеиды), жиры (липопротеиды), нуклеиновые кислоты (нуклеопротеиды)
полноценные – содержат весь набор аминокислот
неполноценные – какие-то аминокислоты в них отсутствуют
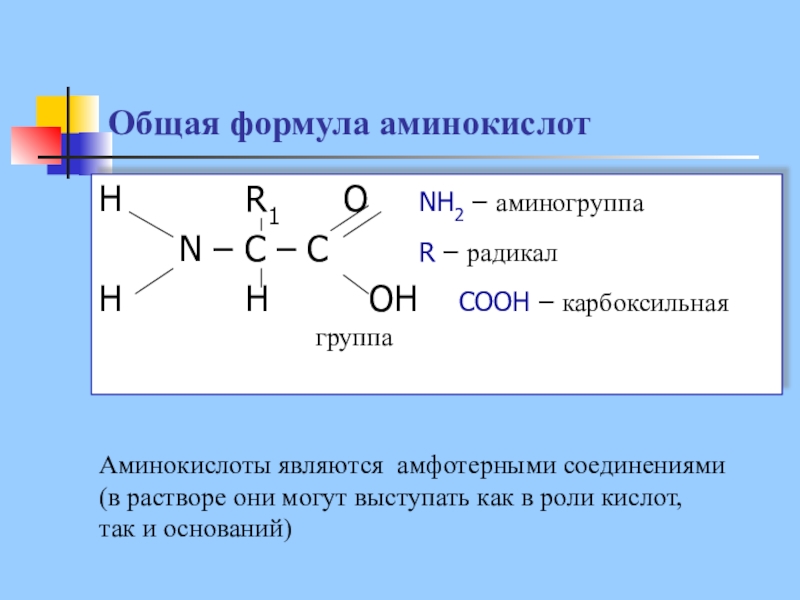
Слайд 12Общая формула аминокислот
H R1 O NH2 – аминогруппа
N –
C – C R – радикал
H H OH COOH – карбоксильная группа
H H OH COOH – карбоксильная группа
Аминокислоты являются амфотерными соединениями
(в растворе они могут выступать как в роли кислот,
так и оснований)
Слайд 13Классификация:
моноаминокарбоновые,
моноаминодикарбоновые,
диаминокарбоновые,
моноаминотрикарбоновые.
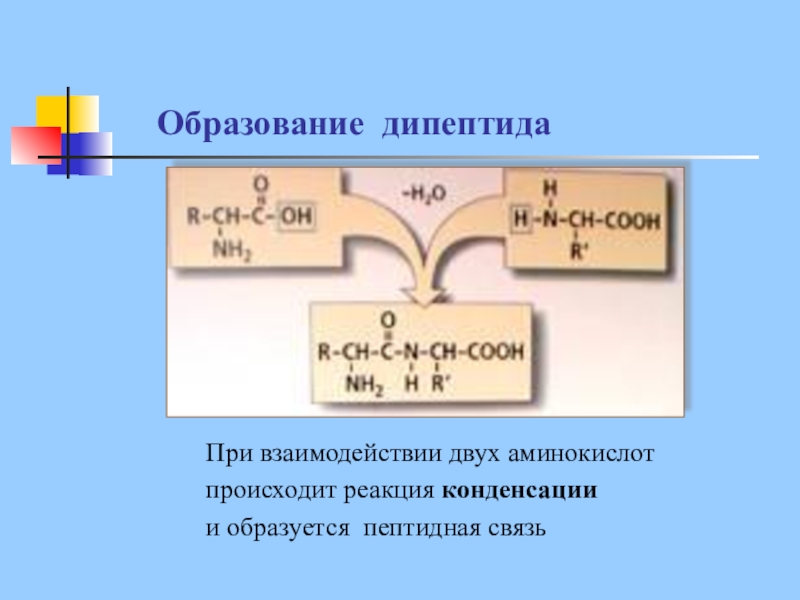
Слайд 17 Образование дипептида
При взаимодействии двух аминокислот
происходит реакция конденсации
и образуется пептидная
связь
Слайд 19 O H
О Н CH2OH O H О
Н2N - CH2 - C - - - N - CH - C - N - - - CH - C - N - CH - C
CH3 СН2SH OН
Н2N - CH2 - C - - - N - CH - C - N - - - CH - C - N - CH - C
CH3 СН2SH OН
Глицил-аланил-серил-цистеин
Слайд 20Уровни организации белка
Размер каждой аминокислоты около 0,3 нм,
Белок, состоящий
из многих аминокислотных остатков, должен представлять собой длинную нить
Размеры молекул белков гораздо меньше
Макромолекулы белков имеют форму компактных шариков (глобул) или вытянутых структур (фибрилл)
Полипептидная цепь каким-то образом сплетена, образуя клубок или пучок нитей
Она свёртывается упорядоченно, для каждого белка определённым образом
Размеры молекул белков гораздо меньше
Макромолекулы белков имеют форму компактных шариков (глобул) или вытянутых структур (фибрилл)
Полипептидная цепь каким-то образом сплетена, образуя клубок или пучок нитей
Она свёртывается упорядоченно, для каждого белка определённым образом
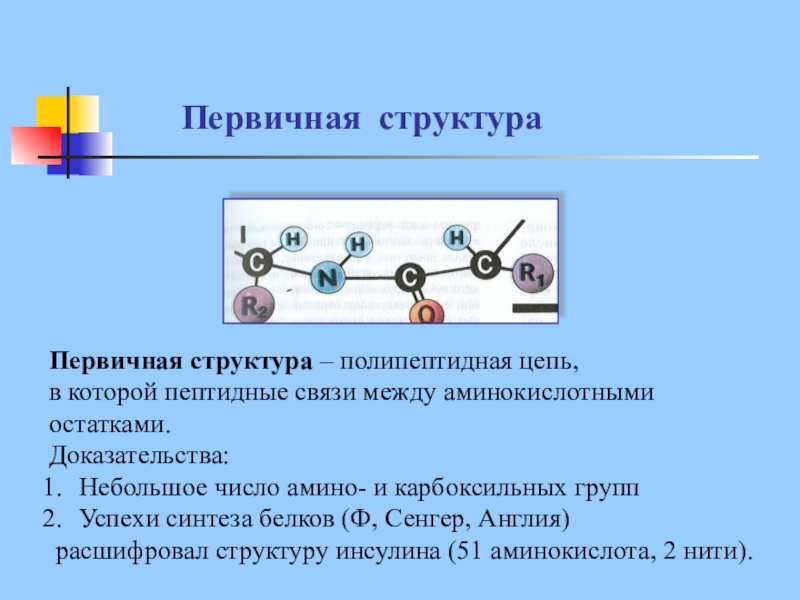
Слайд 21Первичная структура
Первичная структура – полипептидная цепь,
в которой пептидные связи между
аминокислотными
остатками.
Доказательства:
Небольшое число амино- и карбоксильных групп
Успехи синтеза белков (Ф, Сенгер, Англия)
расшифровал структуру инсулина (51 аминокислота, 2 нити).
остатками.
Доказательства:
Небольшое число амино- и карбоксильных групп
Успехи синтеза белков (Ф, Сенгер, Англия)
расшифровал структуру инсулина (51 аминокислота, 2 нити).
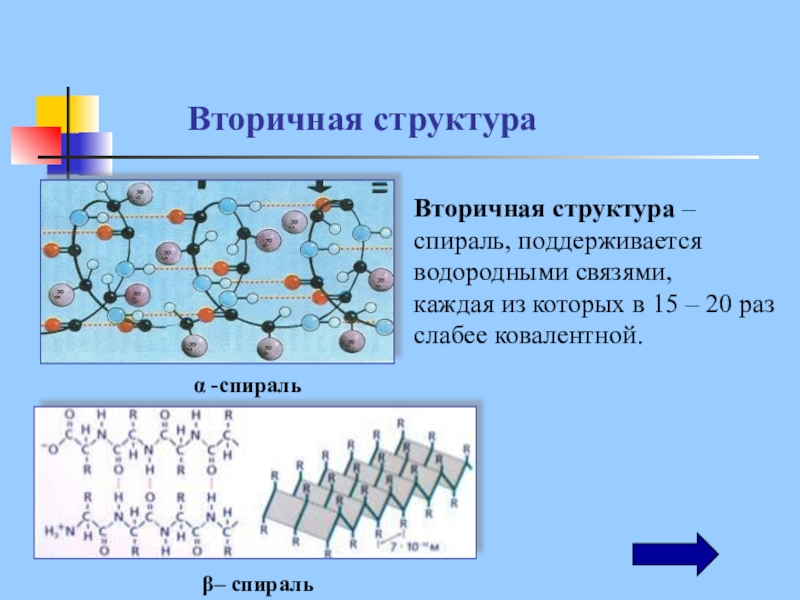
Слайд 22Вторичная структура –
спираль, поддерживается
водородными связями,
каждая из которых в 15
– 20 раз слабее ковалентной.
β– спираль
α -спираль
Вторичная структура
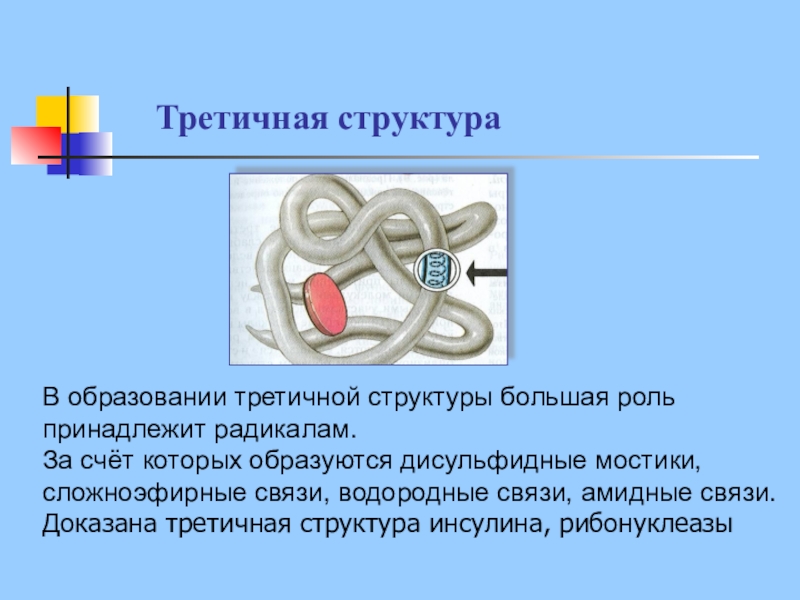
Слайд 23В образовании третичной структуры большая роль
принадлежит радикалам.
За счёт которых
образуются дисульфидные мостики,
сложноэфирные связи, водородные связи, амидные связи.
Доказана третичная структура инсулина, рибонуклеазы
сложноэфирные связи, водородные связи, амидные связи.
Доказана третичная структура инсулина, рибонуклеазы
Третичная структура
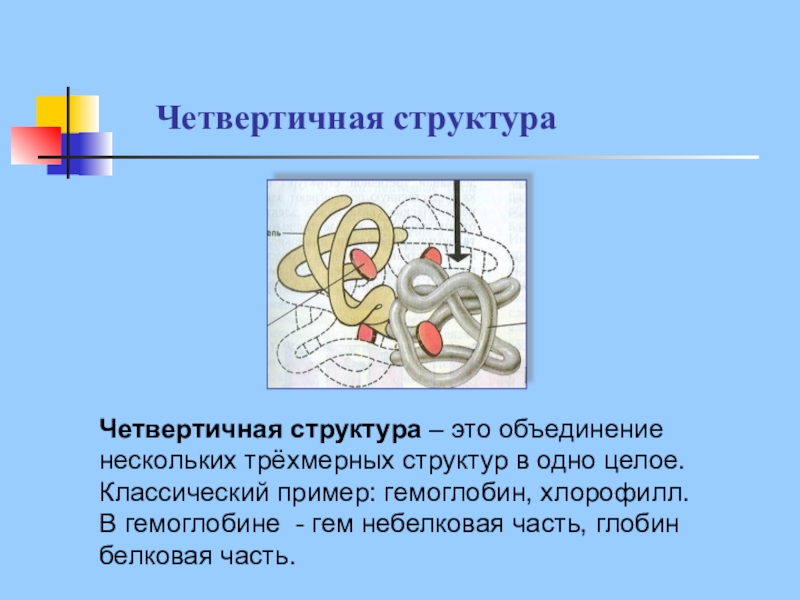
Слайд 24Четвертичная структура
Четвертичная структура – это объединение нескольких трёхмерных структур в одно
целое.
Классический пример: гемоглобин, хлорофилл.
В гемоглобине - гем небелковая часть, глобин белковая часть.
Классический пример: гемоглобин, хлорофилл.
В гемоглобине - гем небелковая часть, глобин белковая часть.
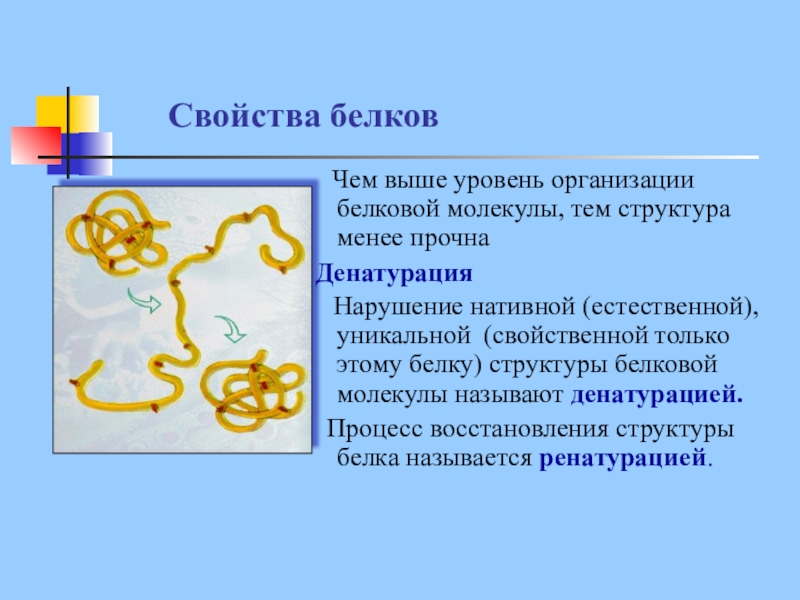
Слайд 25Свойства белков
Чем выше уровень организации белковой молекулы, тем структура
менее прочна
Денатурация
Нарушение нативной (естественной), уникальной (свойственной только этому белку) структуры белковой молекулы называют денатурацией.
Процесс восстановления структуры белка называется ренатурацией.
Денатурация
Нарушение нативной (естественной), уникальной (свойственной только этому белку) структуры белковой молекулы называют денатурацией.
Процесс восстановления структуры белка называется ренатурацией.
Слайд 26Свойства белков
Растворимость белков
Гидролиз белков
Цветные реакции белков: биуретовая, ксантопртеиновая
Амфотерный характер белковых молекул
(амфотерность белков)
Слайд 27Выводы по уроку:
белки – это высокомолекулярные органические соединения, биополимеры, состоящие из
мономеров
α -аминокислот
аминокислоты соединяются в полипептидную цепочку за счёт пептидной связи
аминокислоты заменимые и незаменимые
белки могут быть простыми и сложными
четыре структуры белка (первичная, вторичная, третичная и четвертичная)
денатурация – это утрата белковой молекулой своей структурной организации, обеспечивающей функциональные свойства белка
ренатурация - процесс восстановления структуры белка
α -аминокислот
аминокислоты соединяются в полипептидную цепочку за счёт пептидной связи
аминокислоты заменимые и незаменимые
белки могут быть простыми и сложными
четыре структуры белка (первичная, вторичная, третичная и четвертичная)
денатурация – это утрата белковой молекулой своей структурной организации, обеспечивающей функциональные свойства белка
ренатурация - процесс восстановления структуры белка