- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Химическая связь 11класс
Содержание
- 1. Презентация Химическая связь 11класс
- 2. Почему атомы взаимодействуют между собой? Что такое
- 3. Под химической связью понимают такое взаимодействие
- 4. Как определить число электронов на наружном слое
- 5. Ионная химическая связьэто связь, образовавшаяся за счет
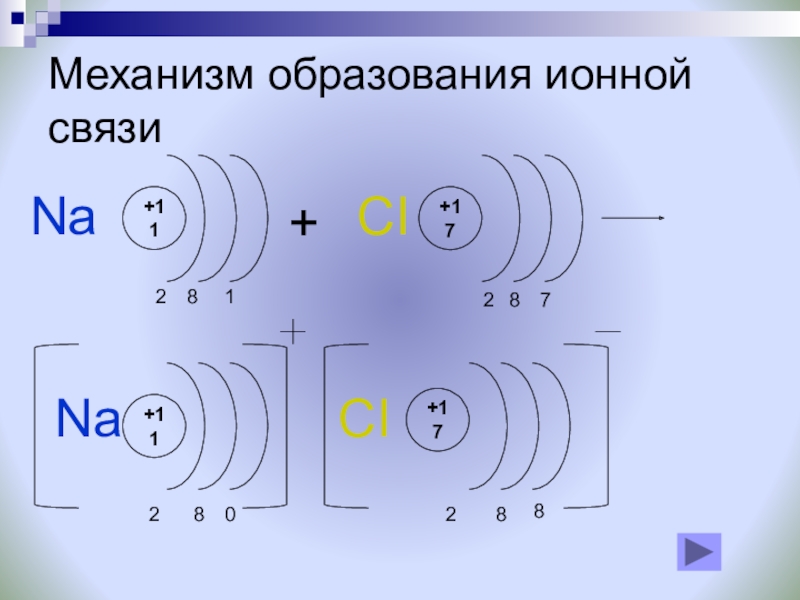
- 6. Механизм образования ионной связи+11082+1782+NaNa+1128CI+177CI2818
- 7. Физические свойства веществ с ионным типом связи:
- 8. Металлическая связьсвязь в металлах и сплавах, которую
- 9. Физические свойства.Валентные электроны принадлежат одновременно всем атомам
- 10. Ковалентная химическая связьэто связь, возникающая между атомами
- 11. Слайд 11
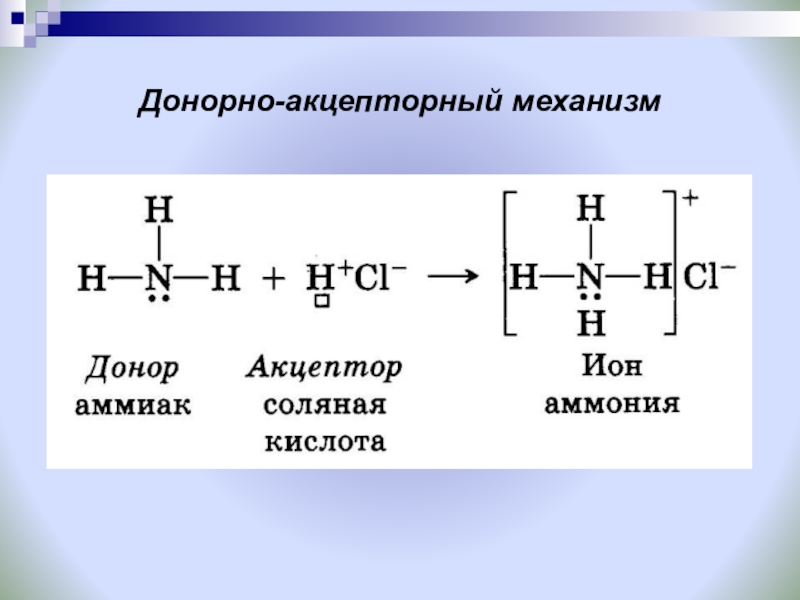
- 12. Донорно-акцепторный механизм
- 13. Способ перекрывания электронных орбиталей:Задание № 1: Вспомните,
- 14. Полярность ковалентной связистепень смещенности общих электронных пар
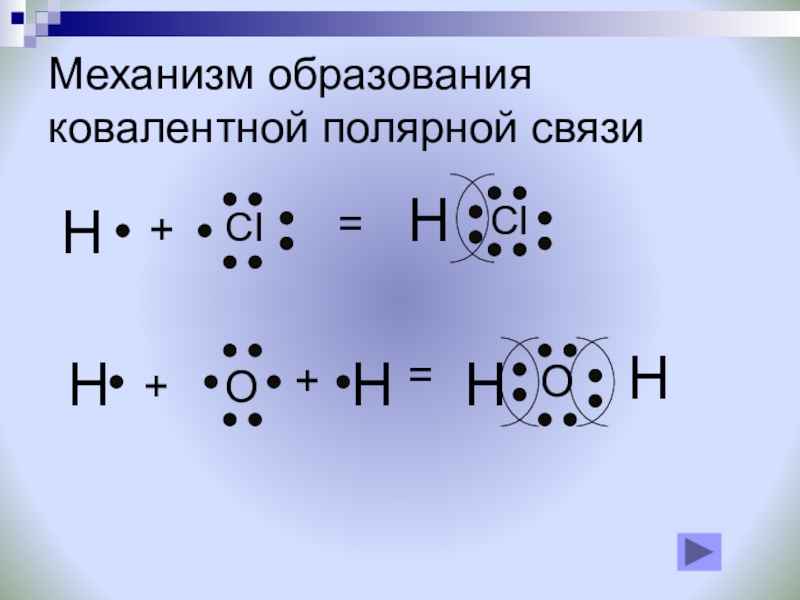
- 15. Механизм образования ковалентной полярной связиHCI+=HCIHOHHH=++O
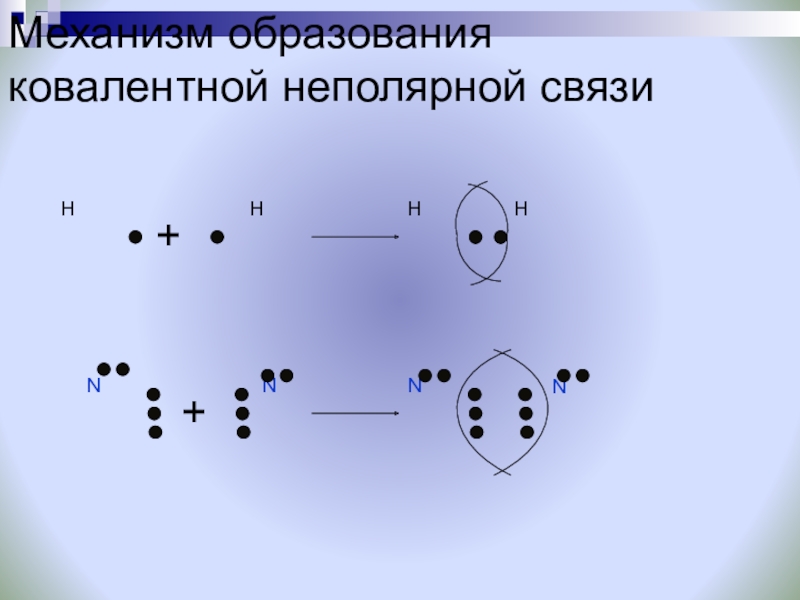
- 16. Механизм образования ковалентной неполярной связиHHNNHHNN++
- 17. Кратность ковалентной связичисло общих электронных пар, связывающих
- 18. ВЕЩЕСТВА С АТОМНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙАЛМАЗ(С), КРЕМНИЙ (Si),
- 19. ВЕЩЕСТВА С МОЛЕКУЛЯРНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙВ УЗЛАХ –
- 20. Водородная связьХимическая связь между положительно поляризованными атомами
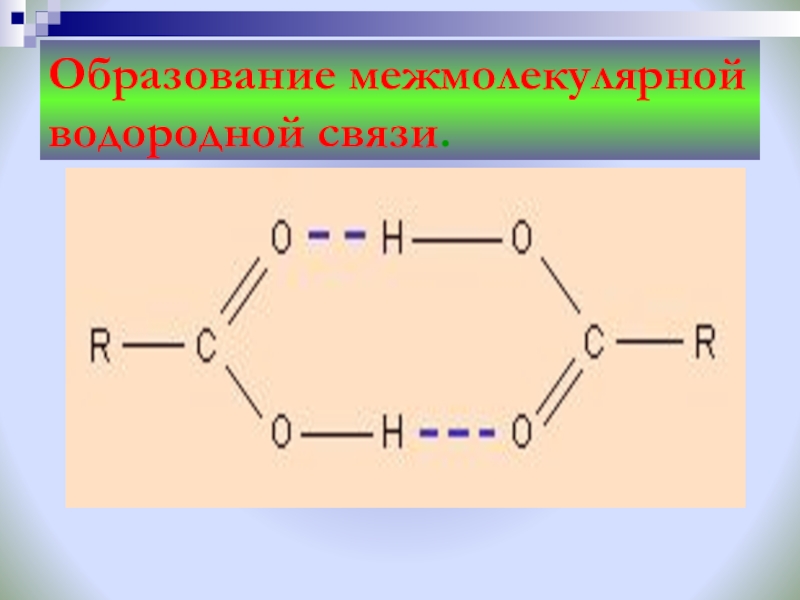
- 21. Образование межмолекулярной водородной связи.
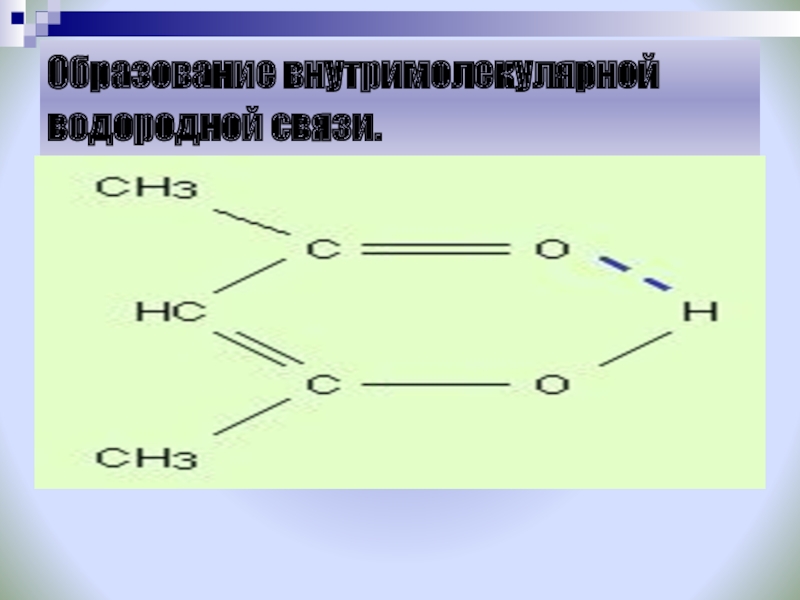
- 22. Образование внутримолекулярной водородной связи.
- 23. Механизм образования водородной связи имеет
- 24. Самостоятельная работаОпределите типы химических связей между атомами
Слайд 2Почему атомы взаимодействуют между собой?
Что такое химическая связь?
Каждый атом стремится к
Сила,связывающая атомы в единый агрегат.
Слайд 3Под химической связью понимают такое взаимодействие атомов, которое связывает их в
Слайд 4Как определить число электронов на наружном слое атомов элементов главных подгрупп?
Число
Как определить число неспаренных электронов?
Число неспаренных электронов= 8- №группы.
Слайд 5Ионная химическая связь
это связь, образовавшаяся за счет
катионов к анионам
Задание:
Выпишите формулы веществ с ионной связью.
РС13; С2Н2; Na3P; СС14 MgCl2; СН4; K3N; NaBr.
Слайд 7Физические свойства веществ с ионным типом связи: твердые, тугоплавкие, не имеющие
Вещества с ионном связью, образуют ионную кристаллическую решетку.
Слайд 8Металлическая связь
связь в металлах и сплавах, которую выполняют относительно свободные электроны
о п+
М — пе М
Схема образования металлической связи:
Задание:
Выпишите формулы веществ, в которых присутствует металлическая и водородная связи
Na, KF, NH3, C2H2, CH3-COOH, H2S, AL, NaCL.
Слайд 9Физические свойства.
Валентные электроны принадлежат одновременно всем атомам металла, свободно перемещаясь по
Образуя единое электронное облако («электронный газ»).
Электроны обладают свойствами волны, они «размазаны» по всему куску металла.
В этом типе связи электроны обусловливают высокую тепло- и электропроводность, металлический блеск
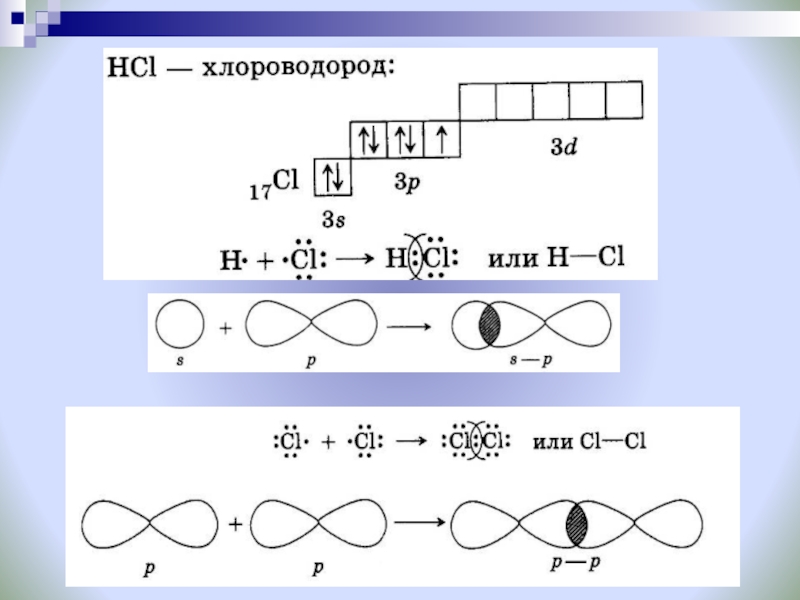
Слайд 10Ковалентная химическая связь
это связь, возникающая между атомами за счет образования общих
Обменный
Донорно-акцепторный
Механизм образования связи:
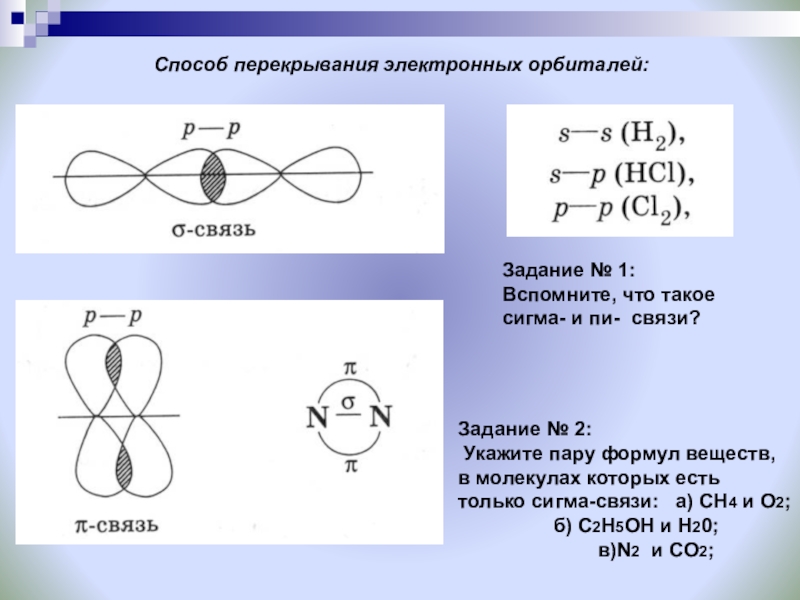
Слайд 13Способ перекрывания электронных орбиталей:
Задание № 1:
Вспомните, что такое сигма- и пи-
Задание № 2:
Укажите пару формул веществ, в молекулах которых есть только сигма-связи: а) СН4 и О2;
б) С2Н5ОН и Н20;
в)N2 и CO2;
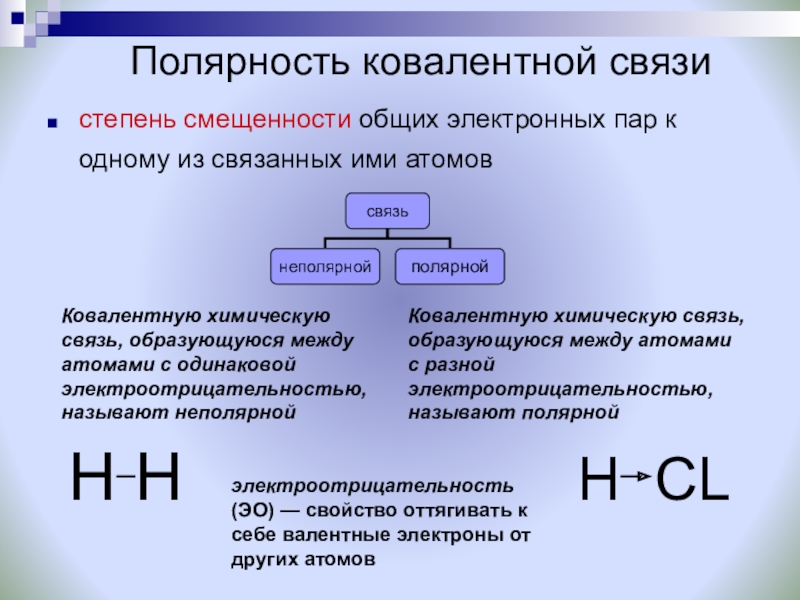
Слайд 14Полярность ковалентной связи
степень смещенности общих электронных пар к одному из связанных
электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов
Ковалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной
Ковалентную химическую связь, образующуюся между атомами с разной электроотрицательностью, называют полярной
H H
H СL
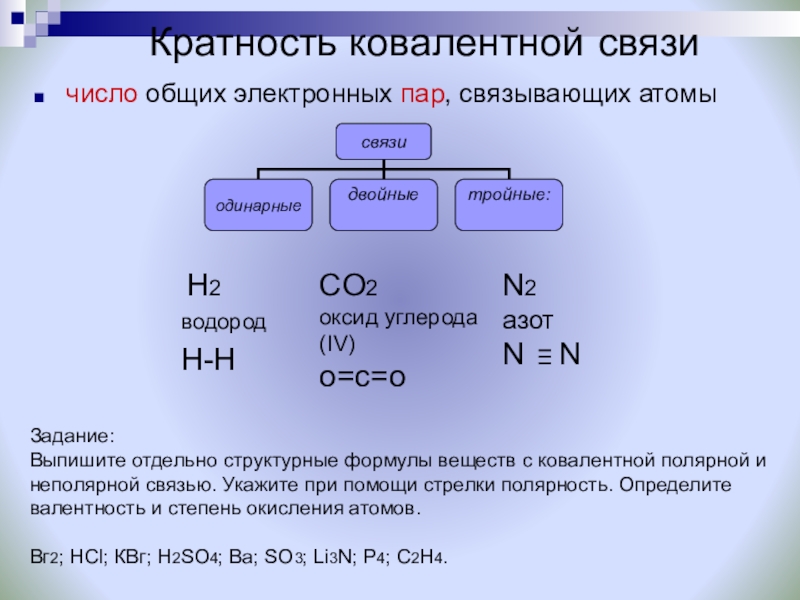
Слайд 17Кратность ковалентной связи
число общих электронных пар, связывающих атомы
CO2
оксид углерода (IV)
о=с=о
N2
азот
N
H2
водород
H-H
Задание:
Выпишите отдельно структурные формулы веществ с ковалентной полярной и неполярной связью. Укажите при помощи стрелки полярность. Определите валентность и степень окисления атомов.
Вг2; НСl; КВг; H2SO4; Ba; SO3; Li3N; P4; C2H4.
Слайд 18ВЕЩЕСТВА С АТОМНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ
АЛМАЗ(С), КРЕМНИЙ (Si), КВАРЦ (SiO2).
Они состоят
Атомный каркас обладает высокой прочностью.
Кристаллы твердые, тугоплавкие, без запаха, в воде нерастворимы.
Слайд 19ВЕЩЕСТВА С МОЛЕКУЛЯРНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ
В УЗЛАХ – НАХОДЯТСЯ МОЛЕКУЛЫ.
УДЕРЖИВАЮТСЯ СЛАБЫМИ
ВЕЩЕСТВА ЛЕГКОПЛАВКИ, ЧАСТО ИМЕЮТ ЗАПАХ.
ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ ПРЕДСТАВЛЯЮТ СОБОЙ ЖИДКОСТИ (ВОДА,БРОМ), ГАЗЫ (КИСЛОРОД, АЗОТ) ИЛИ ЛЕГКОПЛАВКИЕ ТВЕРДЫЕ ВЕЩЕСТВА (ИОД, СЕРА)
Слайд 20Водородная связь
Химическая связь между положительно поляризованными атомами водорода одной молекулы (или
O H…..O H…..O H….
H H H
Слайд 23Механизм образования водородной связи имеет частично электростатический, частично донорно-акцепторный характер. Примеры
Слайд 24Самостоятельная работа
Определите типы химических связей между атомами в веществах.
CaВг2; НСl;
SO2; LiNО3; S2; C2H2; Na; HCОOК.