- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Белки для изучения темы в школьных курсах биологии и химии
Содержание
- 1. Презентация Белки для изучения темы в школьных курсах биологии и химии
- 2. Цели и задачи:
- 3. Белки - обязательная составная часть всех клеток.В
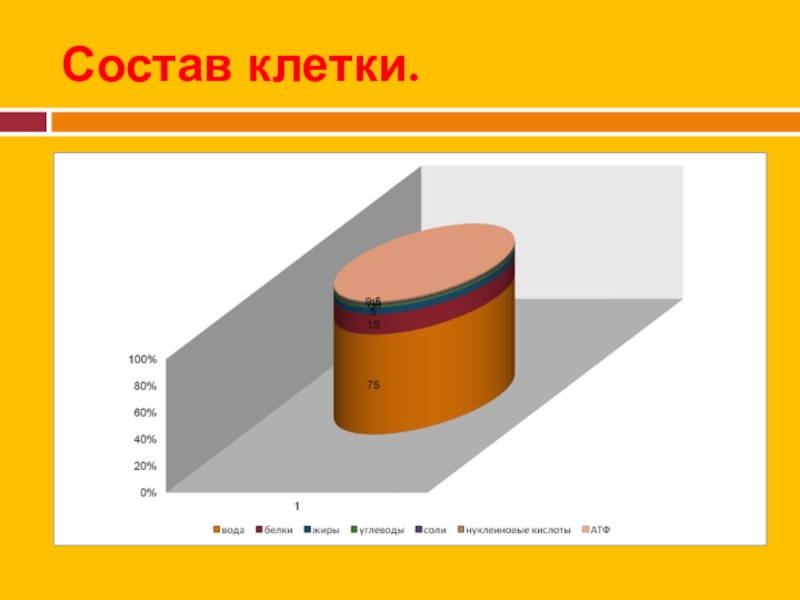
- 4. Состав клетки.
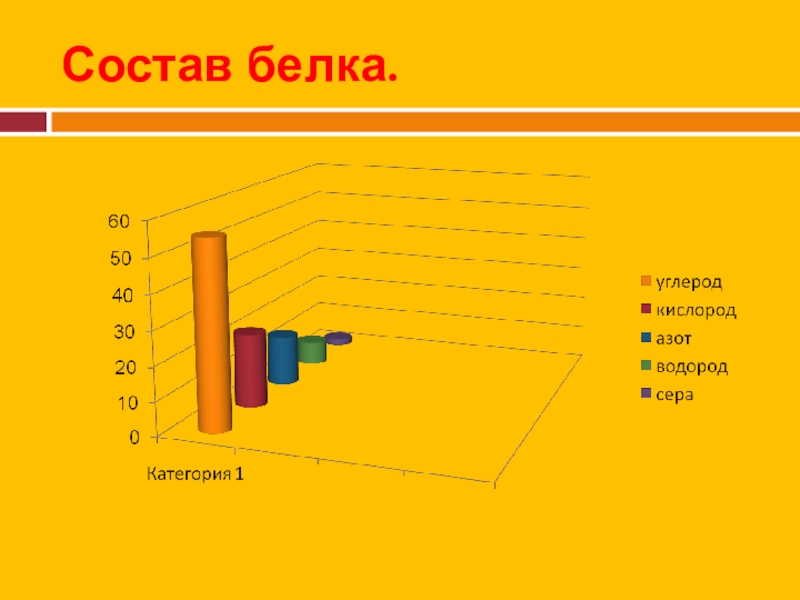
- 5. Состав белка.
- 6. Белки – это азотсодержащие высокомолекулярные органические вещества
- 7. БелкиБелками, или протеинами называют высокомолекулярные (Mr от
- 8. Белки отличаются друг от другаПоследовательностью 20 аминокислот
- 9. Слайд 9
- 10. БелкиАминокислоты в белках связаны пептидными связямиR1, R2, R3 - боковые радикалы одинаковых или различных аминокислот
- 11. Общая структурная формула аминокислот, входящая в состав белков.РАДИКАЛАминогруппаКарбоксильная группа
- 12. Соединение аминокислот в полипептидную цепь.Пептидная связь –
- 13. Уровни организации молекулыПервичная структура - линейная цепь
- 14. Первичная структура белка
- 15. Уровни организации молекулыВторичная структура - полипептидная цепь
- 16. Вторичная структура белкаГлавные элементы - -спирали и
- 17. Уровни организации молекулыТретичная структура - спираль, свернута
- 18. Третичная структура белка
- 19. Третичная структура белкаГлобулярные белки. Имеют вид шара
- 20. Уровни организации молекулыЧетвертичная структура белка - характерна
- 21. Функции белков.Структурная (строительная);Ферментативная;Транспортная;Защитная;Регуляторная;Энергетическая;Двигательная;Запасающая.Далее
- 22. Структурная функция Строительная (пластическая) функцияВходят в состав клеточных мембран и многих органоидов;Коллаген, эластин, кератин и др.
- 23. Ферментативная функция Реакции в живых организмах протекают
- 24. Транспортная функция Гемоглобин (перенос кислорода);Сывороточный альбумин (перенос
- 25. Защитная функция Белки формируют иммунитет (белки — антитела); Лизоцимы — белки-ферменты,
- 26. Регуляторная функция Гормоны регулируют физиологические процессы в
- 27. Энергетическая функция Белки могут являться источниками энергии.
- 28. Двигательная функция Жгутики и реснички двигаются благодаря наличию сократительных белков;Мышцы сокращаются благодаря взаимодействию актина и миозина.
- 29. Запасающая функция Резервные белки, являющиеся источниками питания
- 30. Химические свойства белковБелки обладают амфотерными свойствами:Кислотные свойства
- 31. Химические свойства белковДенатурация – нарушение вторичной и третичной структуры белка
- 32. Причины денатурации:Длительной механическое воздействие,Высокие температуры,Излучение,Воздействие химических веществ.
- 33. Цветные реакцииКсантопротеиновая реакция на белки (для обнаружения
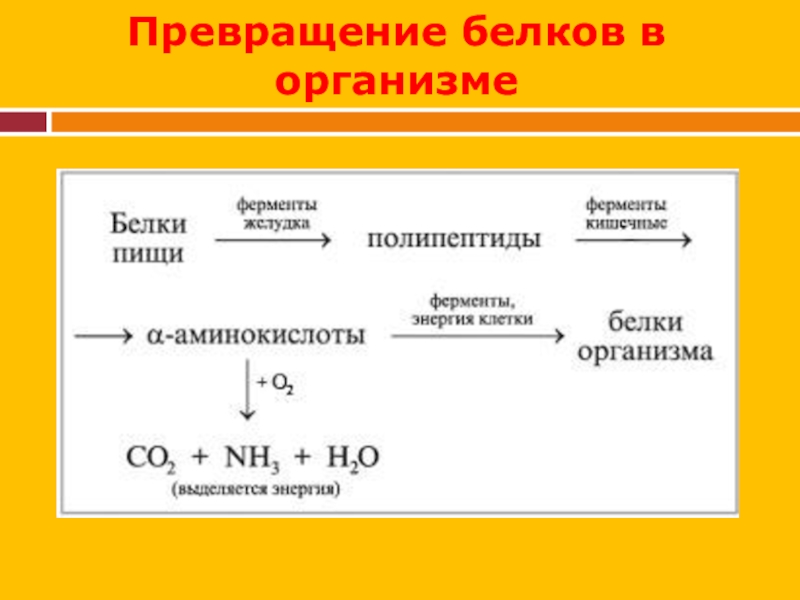
- 34. Превращение белков в организме
- 35. ВыводыБелок – высшая форма развития органических веществ.
- 36. Слайд 36
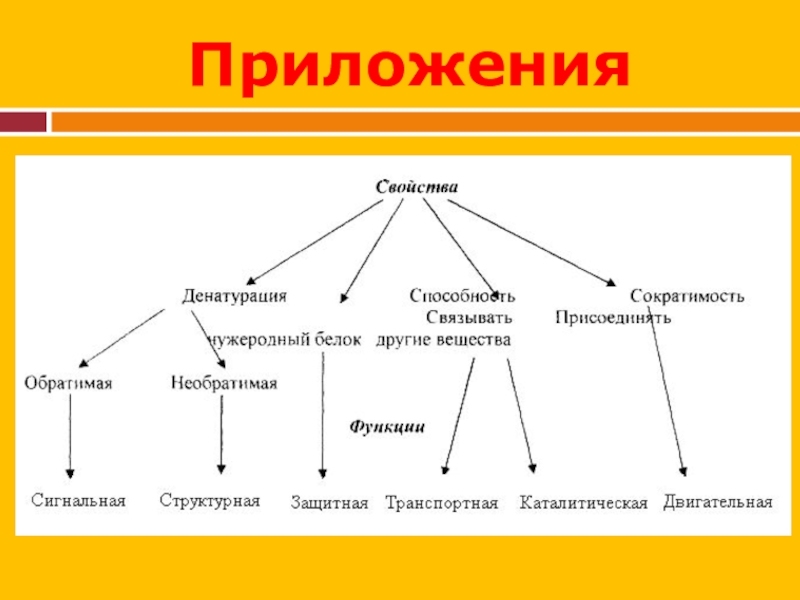
- 37. Приложения
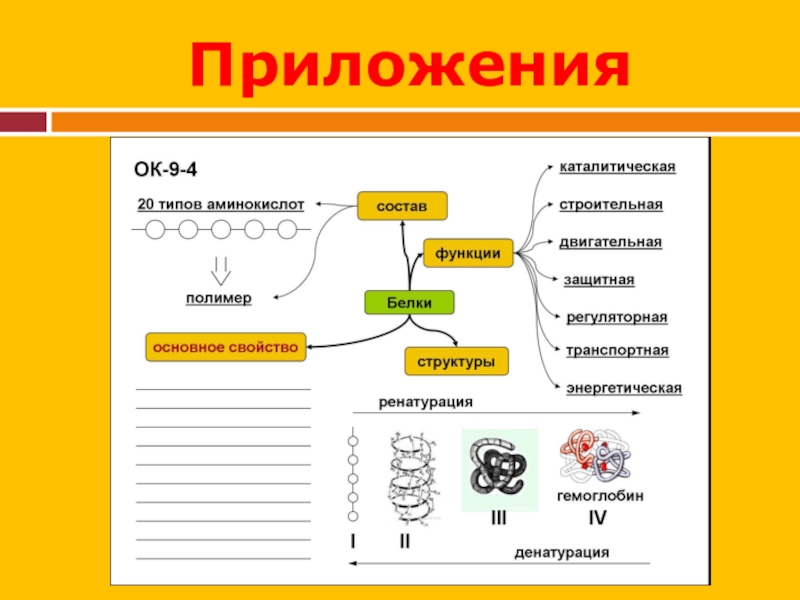
- 38. Приложения
Цели и задачи: Цель: расширение знаний о природных высокомолекулярных веществах – белках. Задачи: 1. Раскрыть ведущую роль белков в строении и
Слайд 2Цели и задачи:
Цель: расширение знаний
о
природных высокомолекулярных веществах – белках.
Задачи:
1. Раскрыть ведущую роль белков в строении и
и жизнедеятельности клетки.
2. Углубить знания о связи между строением,
свойствами белков.
3. Раскрыть роль белков в живой природе.
природных высокомолекулярных веществах – белках.
Задачи:
1. Раскрыть ведущую роль белков в строении и
и жизнедеятельности клетки.
2. Углубить знания о связи между строением,
свойствами белков.
3. Раскрыть роль белков в живой природе.
Слайд 3Белки - обязательная составная часть всех клеток.
В состав этих биополимеров входят
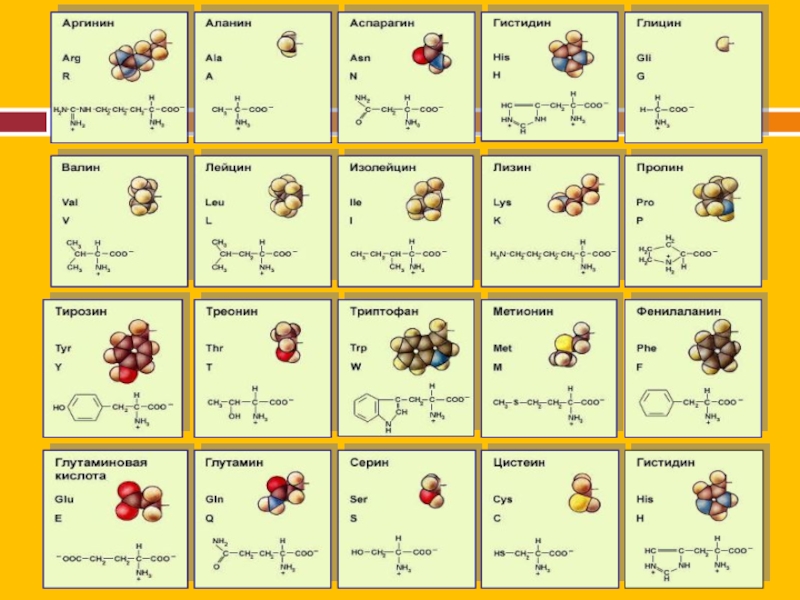
мономеры 20ти типов (аминокислоты).
Белки, или протеины ( от греческого protos-первый).
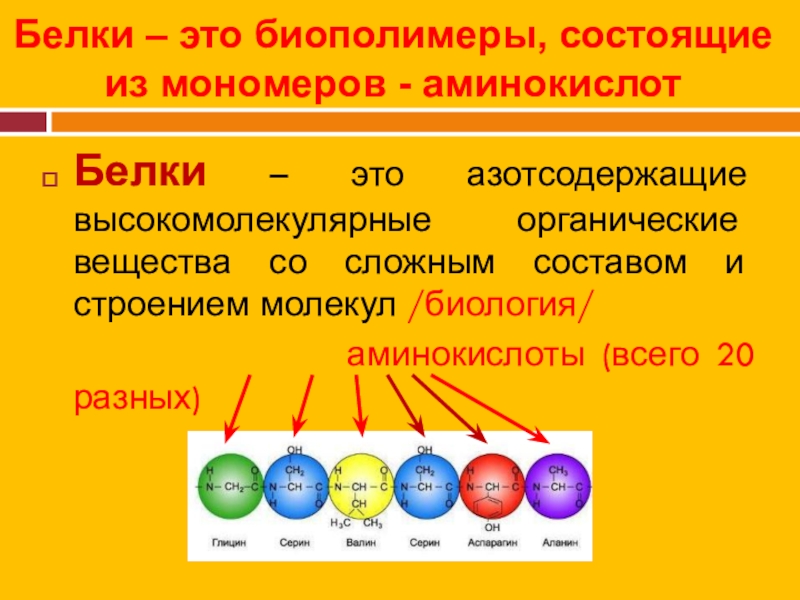
Слайд 6Белки – это азотсодержащие высокомолекулярные органические вещества со сложным составом и
строением молекул /биология/
аминокислоты (всего 20 разных)
аминокислоты (всего 20 разных)
Белки – это биополимеры, состоящие из мономеров - аминокислот
Слайд 7Белки
Белками, или протеинами называют высокомолекулярные (Mr от 5-10 тыс. до 1
млн. и более) природные полимеры, молекулы которых построены из остатков аминокислот, соединенных амидной (пептидной) связью.
Дипептид – имеет 2 изомера;
Трипептид (длина в три аминокислоты) имеет 3!=6 изомеров (ABC, АСВ, ВАС, ВСА, CAB и СВА);
Тетрапептид (4 аминокислоты) имеет 24 различные последовательности;
Полипептид из 20 различных аминокислот имеет 1018 изомеров (Mr ≈2600).
Дипептид – имеет 2 изомера;
Трипептид (длина в три аминокислоты) имеет 3!=6 изомеров (ABC, АСВ, ВАС, ВСА, CAB и СВА);
Тетрапептид (4 аминокислоты) имеет 24 различные последовательности;
Полипептид из 20 различных аминокислот имеет 1018 изомеров (Mr ≈2600).
Слайд 8Белки отличаются друг от друга
Последовательностью 20 аминокислот в длинных цепях, поэтому
каждый организм обладает своими собственными белками, специфичными для данного вида;
Составом аминокислот;
Количеством аминокислот.
Составом аминокислот;
Количеством аминокислот.
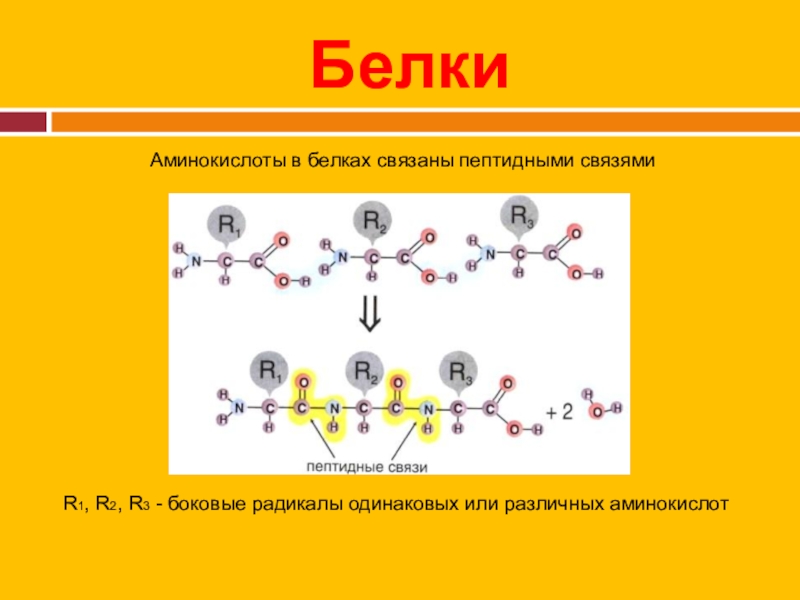
Слайд 10Белки
Аминокислоты в белках связаны пептидными связями
R1, R2, R3 - боковые радикалы
одинаковых или различных аминокислот
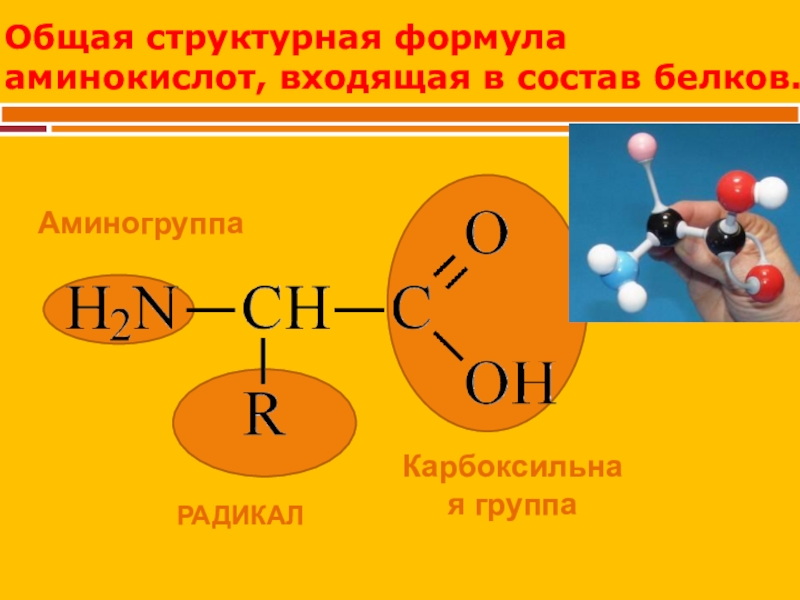
Слайд 11Общая структурная формула аминокислот, входящая в состав белков.
РАДИКАЛ
Аминогруппа
Карбоксильная группа
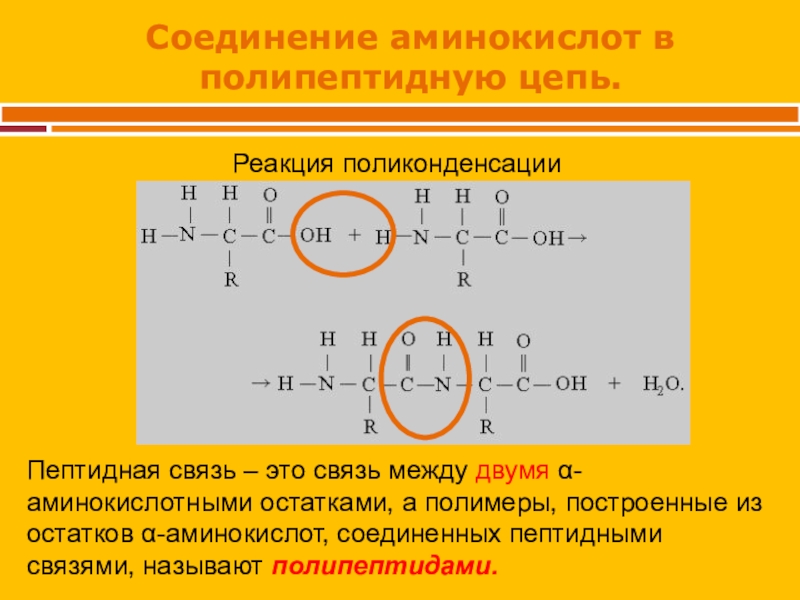
Слайд 12Соединение аминокислот в полипептидную цепь.
Пептидная связь – это связь между двумя
-аминокислотными остатками, а полимеры, построенные из остатков -аминокислот, соединенных пептидными связями, называют полипептидами.
Реакция поликонденсации
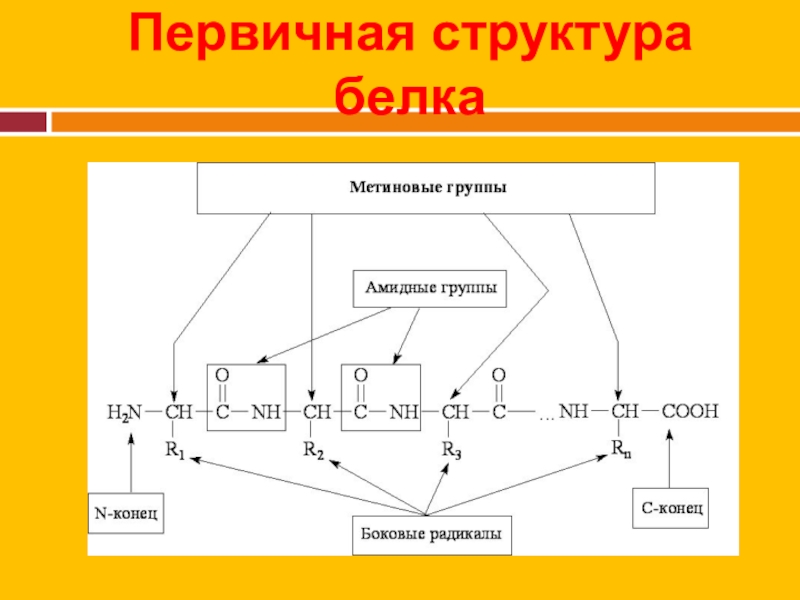
Слайд 13Уровни организации молекулы
Первичная структура - линейная цепь аминокислот, расположенных в определенной
последовательности и соединенных между собой пептидными связями.
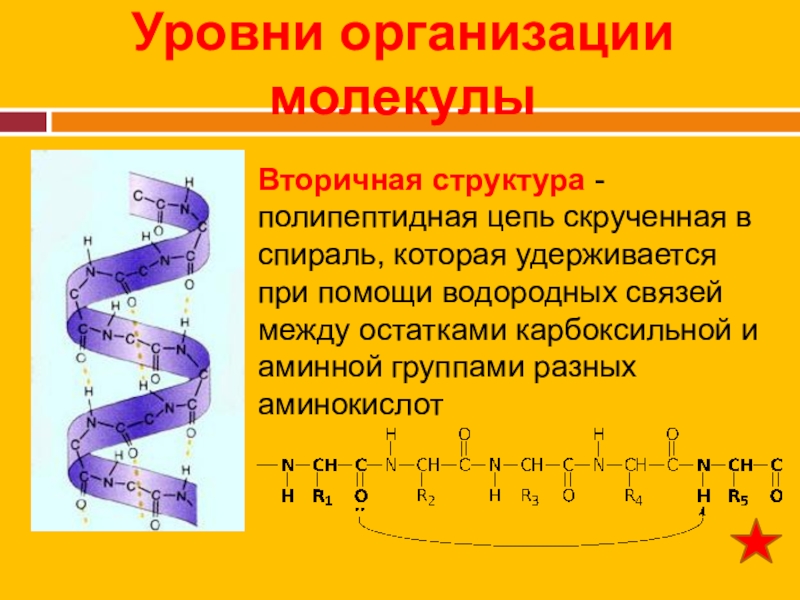
Слайд 15Уровни организации молекулы
Вторичная структура - полипептидная цепь скрученная в спираль, которая
удерживается при помощи водородных связей между остатками карбоксильной и аминной группами разных аминокислот
Слайд 16Вторичная структура белка
Главные элементы - -спирали и -складки.
Идеальная -спираль имеет
шаг 0,54 нм и число однотипных атомов на один виток спирали 3,6, что означает полную периодичность на пяти витках спирали через каждые 18 аминокислотных остатков.
-складки также стабилизируются водородными связями между атомом водорода аминной группы одного фрагмента и атомом кислорода карбоксильной группы другого фрагмента. При этом фрагменты могут иметь как параллельную, так и антипараллельную ориентацию относительно друг друга.
-складки также стабилизируются водородными связями между атомом водорода аминной группы одного фрагмента и атомом кислорода карбоксильной группы другого фрагмента. При этом фрагменты могут иметь как параллельную, так и антипараллельную ориентацию относительно друг друга.
Слайд 17Уровни организации молекулы
Третичная структура - спираль, свернута в форме глобулы и
шара, это закрученная в пространстве в разных направлениях спираль полипептидной цепи.
Эта структура стабилизируется водородными, ионными, ковалентными, дисульфидными связями и гидрофобными взаимодействиями.
Каждому белку свойственна в определенной среде своя особая пространственная структура.
Эта структура стабилизируется водородными, ионными, ковалентными, дисульфидными связями и гидрофобными взаимодействиями.
Каждому белку свойственна в определенной среде своя особая пространственная структура.
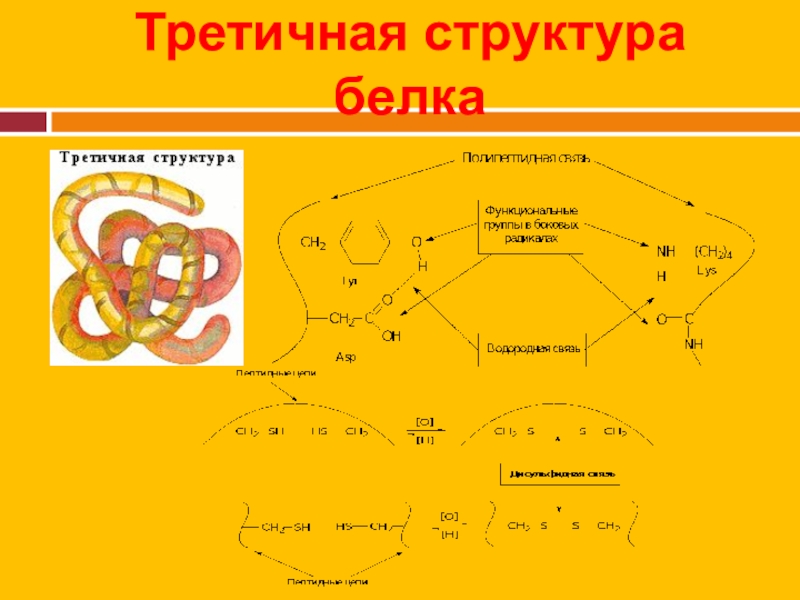
Слайд 19Третичная структура белка
Глобулярные белки. Имеют вид шара или эллипсоида - глобулы.
Значительная часть цепи формирует -спирали и -складки. Например, у миоглобина имеется 5 -спиральных сегментов и нет ни одной -складки.
Фибриллярные белки. Имеют вытянутую нитевидную форму, выполняют структурную функцию. Например, белок -креатин построен из протяженных -спиралей.
Фибриллярные белки. Имеют вытянутую нитевидную форму, выполняют структурную функцию. Например, белок -креатин построен из протяженных -спиралей.
Слайд 20Уровни организации молекулы
Четвертичная структура белка - характерна не для всех белков.
Она возникает в результате соединения нескольких глобул в сложный комплекс.
Например: гемоглобин человека
Например: гемоглобин человека
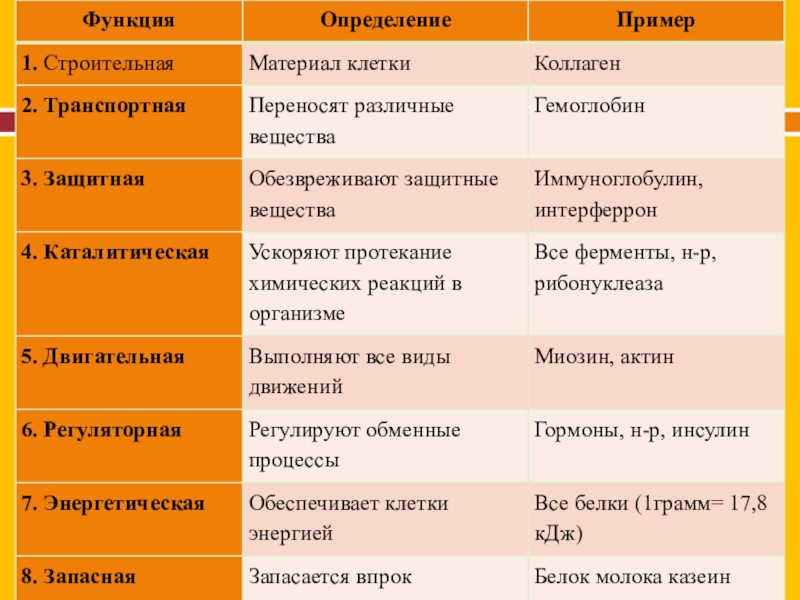
Слайд 21Функции белков.
Структурная (строительная);
Ферментативная;
Транспортная;
Защитная;
Регуляторная;
Энергетическая;
Двигательная;
Запасающая.
Далее
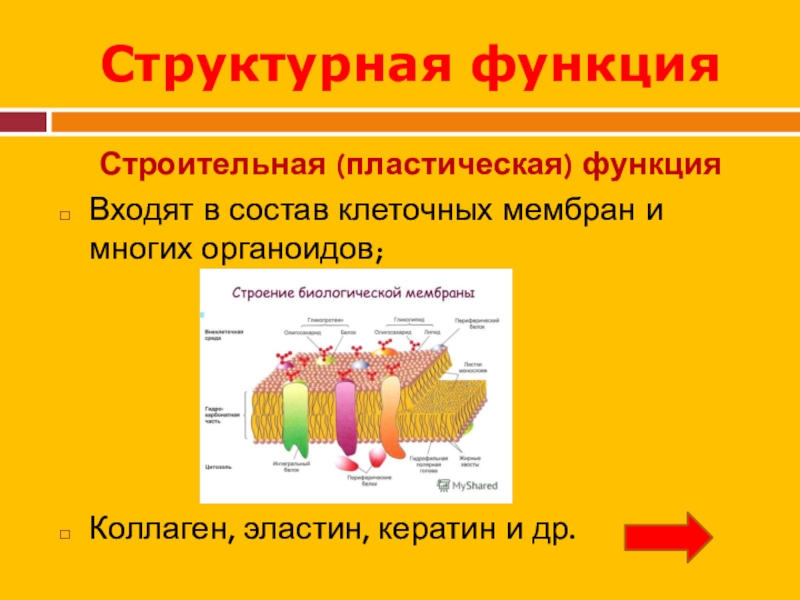
Слайд 22Структурная функция
Строительная (пластическая) функция
Входят в состав клеточных мембран и многих
органоидов;
Коллаген, эластин, кератин и др.
Коллаген, эластин, кератин и др.
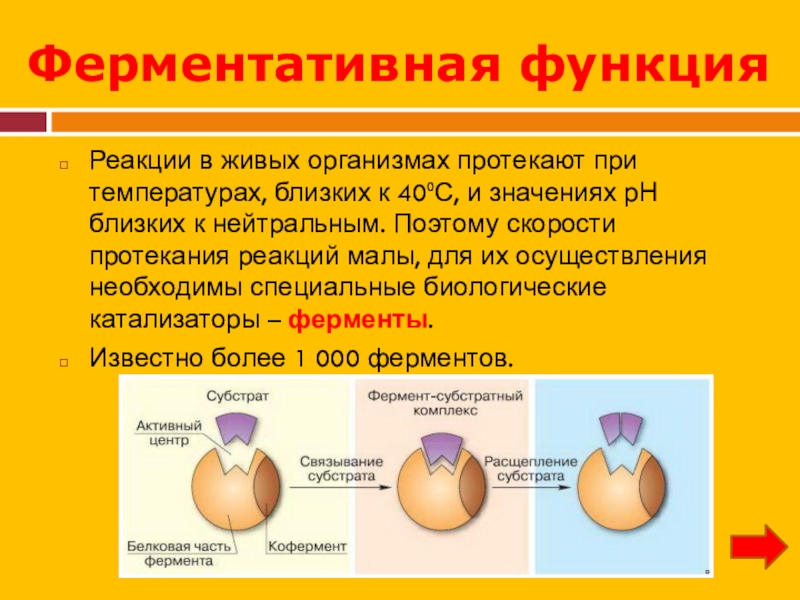
Слайд 23Ферментативная функция
Реакции в живых организмах протекают при температурах, близких к
40⁰С, и значениях рН близких к нейтральным. Поэтому скорости протекания реакций малы, для их осуществления необходимы специальные биологические катализаторы – ферменты.
Известно более 1 000 ферментов.
Известно более 1 000 ферментов.
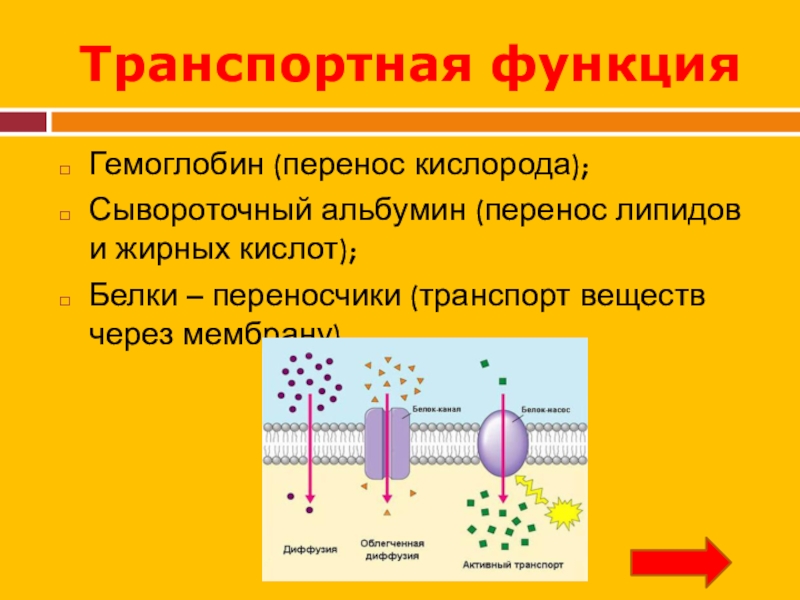
Слайд 24Транспортная функция
Гемоглобин (перенос кислорода);
Сывороточный альбумин (перенос липидов и жирных кислот);
Белки
– переносчики (транспорт веществ через мембрану)
Слайд 25Защитная функция
Белки формируют иммунитет (белки — антитела);
Лизоцимы — белки-ферменты, которые разрушают стенки бактерий;
Интерфероны
– универсальные противовирусные белки;
Образование тромба, свертывание крови;
Выделение токсинов и антитоксинов.
Образование тромба, свертывание крови;
Выделение токсинов и антитоксинов.
Слайд 26Регуляторная функция
Гормоны регулируют физиологические процессы в организме:
Инсулин регулирует содержание глюкозы
в крови;
Соматотропин – гормон роста, усиливает синтез белка и линейный рост костей;
Соматотропин – гормон роста, усиливает синтез белка и линейный рост костей;
Слайд 27Энергетическая функция
Белки могут являться источниками энергии.
При полном расщиплении 1
г. белка выделяется 17,6 кДж энергии.
Аминокислоты, высвобождающиеся при этом используются на построение новых белков.
Функция реализуется редко.
Аминокислоты, высвобождающиеся при этом используются на построение новых белков.
Функция реализуется редко.
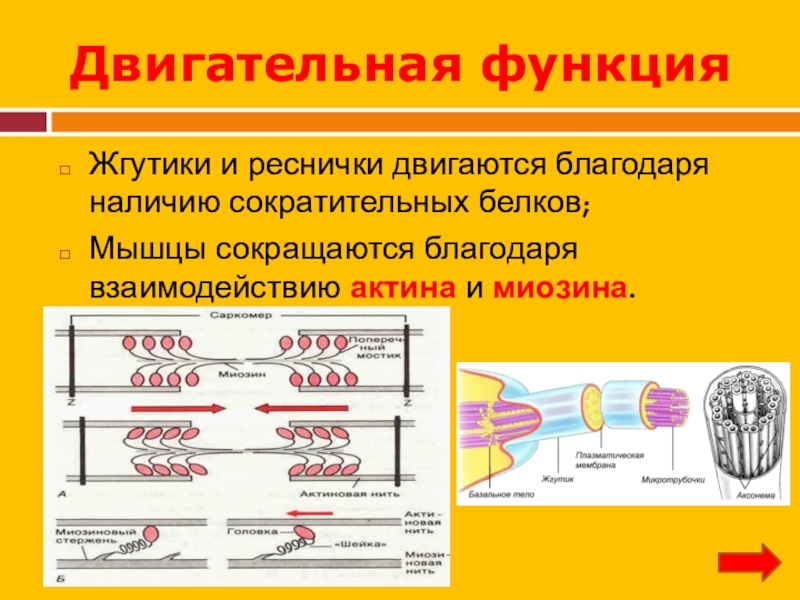
Слайд 28Двигательная функция
Жгутики и реснички двигаются благодаря наличию сократительных белков;
Мышцы сокращаются
благодаря взаимодействию актина и миозина.
Слайд 29Запасающая функция
Резервные белки, являющиеся источниками питания для развития плода; белки
яйца (овальбумины) и основной белок молока (казеин). Они в основном выполняют питательную функцию.
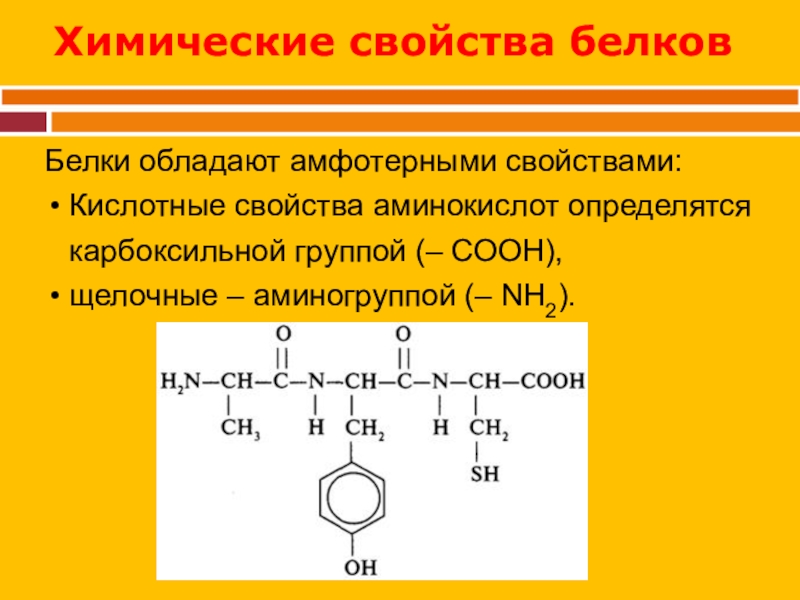
Слайд 30Химические свойства белков
Белки обладают амфотерными свойствами:
Кислотные свойства аминокислот определятся карбоксильной группой
(– СООН),
щелочные – аминогруппой (– NH2).
щелочные – аминогруппой (– NH2).
Слайд 32Причины денатурации:
Длительной механическое воздействие,
Высокие температуры,
Излучение,
Воздействие химических веществ.
Слайд 33Цветные реакции
Ксантопротеиновая реакция на белки (для обнаружения белков, содержащих в своем
составе ароматические аминокислоты),
Биуретовая реакция. Эта реакция характерна для групп атомов, образующих пептидную связь.
Биуретовая реакция. Эта реакция характерна для групп атомов, образующих пептидную связь.
Слайд 35Выводы
Белок – высшая форма развития органических веществ. В нем объединяются признаки
разных классов органических соединений, и в своем сочетании они дают совершенно новые качества, играющие большую роль в жизненных процессах организма