- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Презениация по химии на тему Алюминий (9 класс)
Содержание
- 1. Презениация по химии на тему Алюминий (9 класс)
- 2. ЦЕЛИ УРОКАРассмотреть положение алюминия в Периодической системе
- 3. Изучаемые вопросыАлюминий как химический элемент: положение в
- 4. Al 13Алюминий (лат. Aluminium) 38226,98153s2 3p1Был впервые
- 5. Al 13Алюминий (лат. (лат. Aluminium(лат. Aluminium) 38226,98153s2
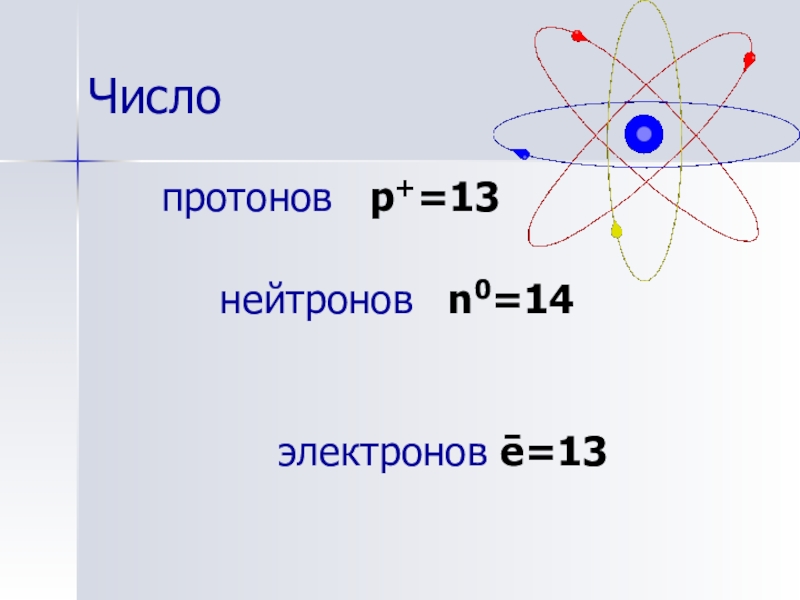
- 6. Числопротонов p+=13 нейтронов n0=14 электронов ē=13
- 7. Изотопы алюминия В природе представлен лишь один стабильный
- 8. Схема расположения электронов на энергетических подуровнях+13Al 1s2
- 9. Al – типичный металлСхема образования вещества
- 10. Физические свойства вещества Al – серебристо-белый металл, пластичный,
- 11. Химические свойства вещества Al активный металл восстанавливает
- 12. Алюминий реагирует: 1. 4Al+3O2 =
- 13. Алюминий реагирует:6. С водой при удалении с
- 14. Пассивация поверхностиКонцентрированные азотная и серная кислоты на холоде пассивируют алюминий, упрочняя защитную пленку на его поверхности.
- 15. Получение веществаАлюминий получают электролизом раствора глинозема в
- 16. Домашнее задание:И.И.Новошинский, Н.С.НовошинскаяС. 182-185Задания 1-3,5,6.
- 17. Соединения алюминияЦели урока: ознакомить учащихся с соединениями
- 18. Соединения алюминияИзучаемые вопросы: соединения алюминия, их состав
- 19. Оксид алюминия Al2О3:Очень твердый (корунд, рубин) порошок
- 20. Белый нерастворимый в воде порошок.Проявляет амфотерные свойства,
- 21. Качественная реакция на ион Al3+ Реактивом на
- 22. ЛО.14 Получение гидроксида алюминия и исследование его
- 23. Применение Al
- 24. Ряд факторов применения алюминия:Алюминий – самый распространенный
- 25. Влияние соединений алюминия на загрязнение окружающей среды. Почти
- 26. Металл будущего Вывод: Обладая такими свойствами как
- 27. Домашнее заданиеИ.И.Новошинский, Н.С.НовошинскаяС. 185-186Задания 4Н. РаботаIV,вариант 11(5). 16(2).17(3). 19(2).
ЦЕЛИ УРОКАРассмотреть положение алюминия в Периодической системе элементов.Ознакомить учащихся с нахождением алюминия в природе, получением, физическими и химическими свойствами.Сформировать понятие «пассивация поверхности».
Слайд 2ЦЕЛИ УРОКА
Рассмотреть положение алюминия в Периодической системе элементов.
Ознакомить учащихся с нахождением
алюминия в природе, получением, физическими и химическими свойствами.
Сформировать понятие «пассивация поверхности».
Сформировать понятие «пассивация поверхности».
Слайд 3Изучаемые вопросы
Алюминий как химический элемент: положение в Периодической системе, строение атома,
электроотрицательность, Нахождение в природе. Алюминий – простое вещество. Получение, физические и химические свойства: взаимодействие с кислородом и другими неметаллами, оксидами металлов, водой, растворами кислот и щелочей. Действие на алюминий концентрированных азотной и серной кислот на холоде.
Слайд 4Al
13
Алюминий
(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Был впервые получен датским физиком Х.К. Эрстедом
в 1825 г. Название этого элемента происходит от латинского алюмен, так в древности назывались квасцы, которые использовали для крашения тканей. Латинское название, вероятно, восходит к греческому «халмэ» - рассол, соляной раствор.
Слайд 5Al
13
Алюминий
(лат. (лат. Aluminium(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Порядковый номер. Химический элемент III
группы главной подгруппы 3-го периода.
Слайд 7Изотопы алюминия
В природе представлен лишь один стабильный изотоп 27Al. Искусственно получен
ряд радиоактивных изотопов алюминия, наиболее долгоживущий 26Al имеет период полураспада 720 тысяч лет.
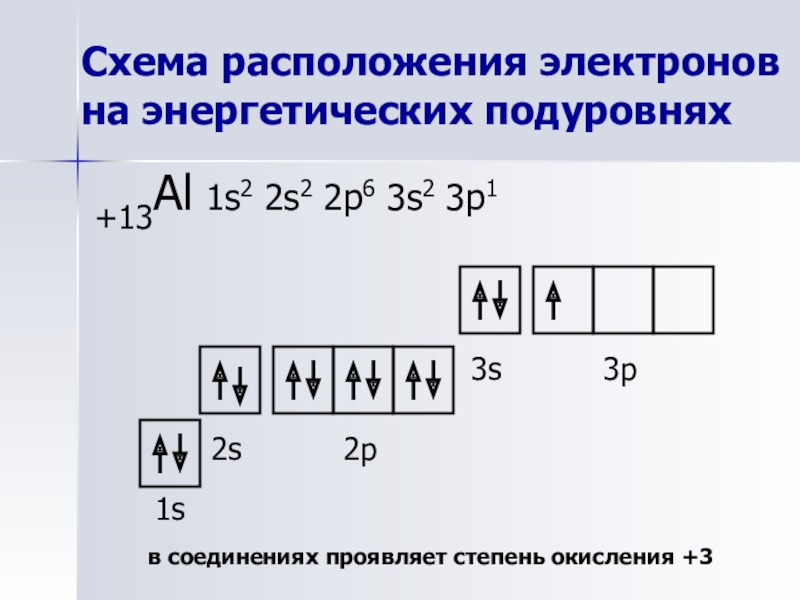
Слайд 8Схема расположения электронов на энергетических подуровнях
+13Al 1s2 2s2 2p6 3s2 3p1
1s
2s
2p
3s
3p
в соединениях проявляет степень окисления +3
Слайд 9Al – типичный металл
Схема образования вещества
Al 0- 3ē
↔ Al+3
Тип химической связи -металлическая
Тип кристаллической решетки – металлическая
Тип химической связи -металлическая
Тип кристаллической решетки – металлическая
Слайд 10Физические свойства вещества
Al – серебристо-белый металл, пластичный, легкий, хорошо проводит тепло
и электрический ток, обладает хорошей ковкостью, легко поддаётся обработке, образует лёгкие и прочные сплавы.
ρ=2,7 г/см3
tпл.=6600С
ρ=2,7 г/см3
tпл.=6600С
Слайд 11Химические свойства вещества
Al активный металл восстанавливает все элементы, находящиеся справа
от него в электрохимическом ряду напряжения металлов, простые вещества – неметаллы. Из сложных соединений алюминий восстанавливает ионы водорода и ионы менее активных металлов. Однако при комнатной температуре на воздухе алюминий не изменяется, поскольку его поверхность покрыта защитной оксидной плёнкой Al2 O3
Слайд 12Алюминий реагирует:
1. 4Al+3O2 = 2Al2O3 + Q – покрывается
пленкой оксида, но в мелкораздроблен-ном виде горит с выделением большого количества теплоты.
2. 2Al + 3Cl2 = 2 AlCl3 (Br2, I3) – на холоду
3. 2Al + 3S = Al2S3 - при нагревании
4. 4Al + 3С = Al4С3 - при нагревании
5. Алюминотермия – получение металлов: Fe, Cr, Mn, Ti, W и другие, например:
3Al + 3Fe3O4 = 4Al2O3 + 9Fe
2. 2Al + 3Cl2 = 2 AlCl3 (Br2, I3) – на холоду
3. 2Al + 3S = Al2S3 - при нагревании
4. 4Al + 3С = Al4С3 - при нагревании
5. Алюминотермия – получение металлов: Fe, Cr, Mn, Ti, W и другие, например:
3Al + 3Fe3O4 = 4Al2O3 + 9Fe
Слайд 13Алюминий реагирует:
6. С водой при удалении с поверхности оксидной пленки
2 Al + 6Н2O = 2Al(ОН)3 + 3Н2
7. С растворами щелочей образуя соли алюминаты:
2Al + 2NаОН + 2Н2O = 2NаAlО2 + 3Н2
8. С разбавленными кислотами
(НCL,H2SO4)
2Al + 6НCL = 2AlCl3 + 3Н2
7. С растворами щелочей образуя соли алюминаты:
2Al + 2NаОН + 2Н2O = 2NаAlО2 + 3Н2
8. С разбавленными кислотами
(НCL,H2SO4)
2Al + 6НCL = 2AlCl3 + 3Н2
Слайд 14Пассивация поверхности
Концентрированные азотная и серная кислоты на холоде пассивируют алюминий, упрочняя
защитную пленку на его поверхности.
Слайд 15Получение вещества
Алюминий получают электролизом раствора глинозема в расплавленном криолите (Na3AIF6), электролизом
расплава AlCl3 (расходуется около 16 кВт·час на 1 кг Al)
Электролиз: Al2O3 при 9500С в расплаве криолита: На катоде: Al3+ + 3e = Al0
На угольном аноде (расходуется в процессе электролиза):
O2- - 2e = 00;
C + O = CO;
2CO + O2 = 2CO2;
Электролиз: Al2O3 при 9500С в расплаве криолита: На катоде: Al3+ + 3e = Al0
На угольном аноде (расходуется в процессе электролиза):
O2- - 2e = 00;
C + O = CO;
2CO + O2 = 2CO2;
Слайд 17Соединения алюминия
Цели урока: ознакомить учащихся с соединениями алюминия. Сформировать знания о
свойствах его оксида и гидроксида. Охарактеризовать области применения алюминия, его сплавов и соединений. Сформировать умение распознавать ион алюминия.
Слайд 18Соединения алюминия
Изучаемые вопросы: соединения алюминия, их состав и способы получения. Амфотерность
оксида и гидроксида алюминия. Качественная реакция на ион алюминия. Применение алюминия, его сплавов и соединений.
Слайд 19Оксид алюминия Al2О3:
Очень твердый (корунд, рубин) порошок белого цвета, тугоплавкий -
20500С. Не растворяется в воде.
Амфотерный оксид, взаимодействует:
а) с кислотами Al2O3 + 6H+ = 2Al3+ + 3H2O
б) со щелочами Al2O3 + 2OH- = 2AlO-2 + H2O
Образуется:
а) при окислении или горении алюминия на воздухе
4Al + 3O2 = 2Al2O3
б) в реакции алюминотермии
2Al + Fe2O3 = Al2O3 + 2Fe
в) при термическом разложении гидроксида алюминия 2Al (OH)3 = Al2O3 + 3H2O
Амфотерный оксид, взаимодействует:
а) с кислотами Al2O3 + 6H+ = 2Al3+ + 3H2O
б) со щелочами Al2O3 + 2OH- = 2AlO-2 + H2O
Образуется:
а) при окислении или горении алюминия на воздухе
4Al + 3O2 = 2Al2O3
б) в реакции алюминотермии
2Al + Fe2O3 = Al2O3 + 2Fe
в) при термическом разложении гидроксида алюминия 2Al (OH)3 = Al2O3 + 3H2O
Слайд 20Белый нерастворимый в воде порошок.
Проявляет амфотерные свойства, взаимодействует:
а) с кислотами Al
(OH)3 + 3HCl = AlCl3 + 3H2O
б) со щелочами Al (OH)3 + Na OH = NaAlO2 + 2H2O
Разлагается при нагревании 2Al (OH)3 = Al2O3 + 3H2O
Образуется:
а) при взаимодействии растворов солей алюминия с растворами щелочей (без избытка)
Al3+ + 3OH- = Al (OH)3
б) при взаимодействии алюминатов с кислотами (без избытка)
AlO-2 + H+ + H2O = Al (OH)3
б) со щелочами Al (OH)3 + Na OH = NaAlO2 + 2H2O
Разлагается при нагревании 2Al (OH)3 = Al2O3 + 3H2O
Образуется:
а) при взаимодействии растворов солей алюминия с растворами щелочей (без избытка)
Al3+ + 3OH- = Al (OH)3
б) при взаимодействии алюминатов с кислотами (без избытка)
AlO-2 + H+ + H2O = Al (OH)3
Гидроксид алюминия Al(ОН)3:
Слайд 21Качественная реакция на ион Al3+
Реактивом на ионы Al3+ являются ионы
OH- При действии раствора щелочи на соль алюминия образуется белый осадок Al(ОН)3, который растворяется в избытке щелочи.
AlCl3 + 3NaOH = Al(OH)3 + 3 NaCl
Al3+ + 3OH- = Al (OH)3
Al (OH)3 + NaOH = NaAlO2 + 2H2O
Al (OH)3 + OH- = AlO-2 + 2H2O
AlCl3 + 3NaOH = Al(OH)3 + 3 NaCl
Al3+ + 3OH- = Al (OH)3
Al (OH)3 + NaOH = NaAlO2 + 2H2O
Al (OH)3 + OH- = AlO-2 + 2H2O
Слайд 22ЛО.14 Получение гидроксида алюминия и исследование его кислотно-основных свойств
1.В пробирку налейте
2-3мл раствора соли алюминия и прилейте столько же водного раствора аммиака
AlCl3 + 3NН4OH = Al(OH)3 + 3NН4Cl
2. Полученный в предыдущем опыте осадок разделите на две части. К первой прилейте соляную кислоту, к другой – избыток раствора гидроксида натрия
Al (OH)3 + 3HCl = AlCl3 + 3H2O
Al (OH)3 + Na OH = NaAlO2 + 2H2O
AlCl3 + 3NН4OH = Al(OH)3 + 3NН4Cl
2. Полученный в предыдущем опыте осадок разделите на две части. К первой прилейте соляную кислоту, к другой – избыток раствора гидроксида натрия
Al (OH)3 + 3HCl = AlCl3 + 3H2O
Al (OH)3 + Na OH = NaAlO2 + 2H2O
Слайд 24Ряд факторов применения алюминия:
Алюминий – самый распространенный металл земной коры. Его
ресурсы практически неисчерпаемы.
Обладает высокой коррозионной стойкостью и практически не нуждается в специальной защите.
Высокая химическая активность алюминия используется в алюминотермии.
Малая плотность в сочетании с высокой прочностью и пластичностью его сплавов делает алюминий незаменимым конструкционным материалом в самолетостроений и способствует расширению его применения в наземном и водном транспорте, а также в строительстве.
Относительно высокая электропроводность позволяет заменять им значительно более дорогую медь в электротехнике.
Обладает высокой коррозионной стойкостью и практически не нуждается в специальной защите.
Высокая химическая активность алюминия используется в алюминотермии.
Малая плотность в сочетании с высокой прочностью и пластичностью его сплавов делает алюминий незаменимым конструкционным материалом в самолетостроений и способствует расширению его применения в наземном и водном транспорте, а также в строительстве.
Относительно высокая электропроводность позволяет заменять им значительно более дорогую медь в электротехнике.
Слайд 25 Влияние соединений алюминия на загрязнение окружающей среды.
Почти все загрязняющие вещества, которые
первоначально попали в атмосферу, в конечном итоге оказываются на поверхности суши и воды. Оседающие аэрозоли могут содержать ядовитые тяжелые металлы – свинец, кадмий, ртуть, медь, ванадий, кобальт, никель. Обычно они малоподвижны и накапливаются в почве. Но в почву попадают с дождями также кислоты. Соединяясь с ними, металлы могут переходить в растворимые соединения, доступные растениям. В растворимые формы переходят также вещества, постоянно присутствующие в почвах, что иногда приводит к гибели растений. Примером может служить весьма распространенный в почвах алюминий, растворимые соединения которого поглощаются корнями деревьев. Алюминиевая болезнь, при которой нарушается структура тканей растений, оказывается для деревьев смертельной.
Слайд 26Металл будущего
Вывод: Обладая такими свойствами как лёгкость, прочность, коррозионноустойчивость, устойчивость
к действию сильных химических реагентов - алюминий нашёл большое значение в авиационном и космическом транспорте, применение во многих отраслях народного хозяйства. Особое место занял алюминий и его сплавы в электротехнике, а за ними будущее нашей науки и техники.