КОЛЛЕДЖ»
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Предмет органической химии
Содержание
- 1. Предмет органической химии
- 2. Проблемные вопросы:Почему углерод называют элементом жизни?Какие вещества
- 3. Возникновение органической химии как науки-1807 год Йенс
- 4. История развития органической химии :1824г. – синтезирована
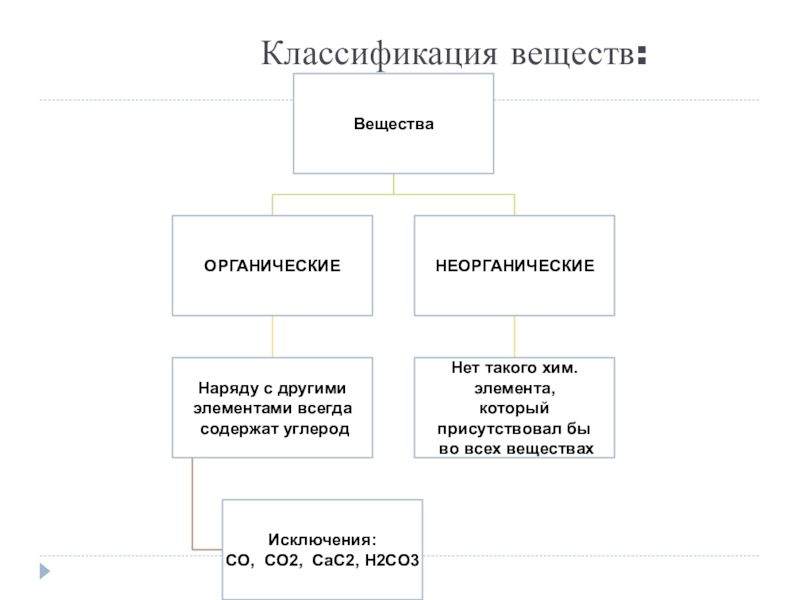
- 5. Классификация веществ:
- 6. Определение органической химии:Органическая химия-раздел химической науки, изучающий
- 7. Предмет органической химииПредметом органической химии являются вещества,
- 8. Причины выделения в самостоятельную дисциплину органическую химию:
- 9. Признаки органических веществ:Содержат углерод в валентности 4Горят
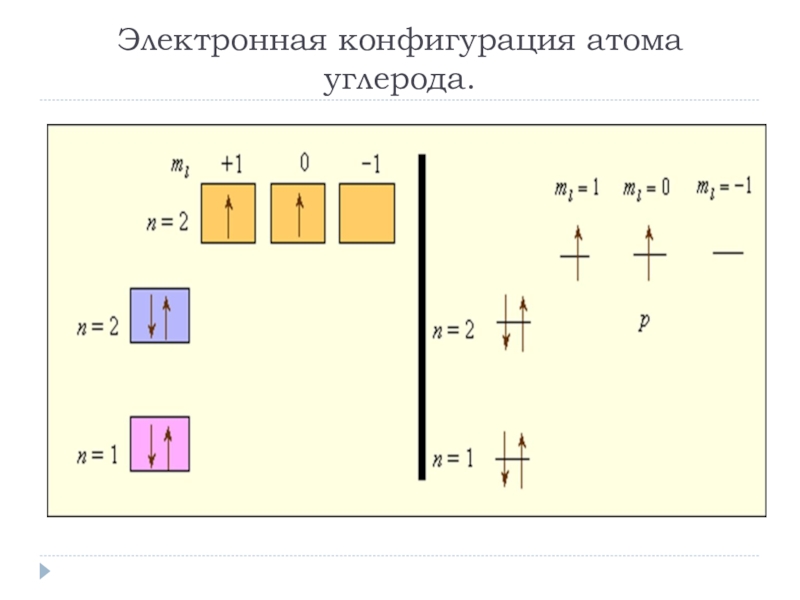
- 10. Электронная конфигурация атома углерода.
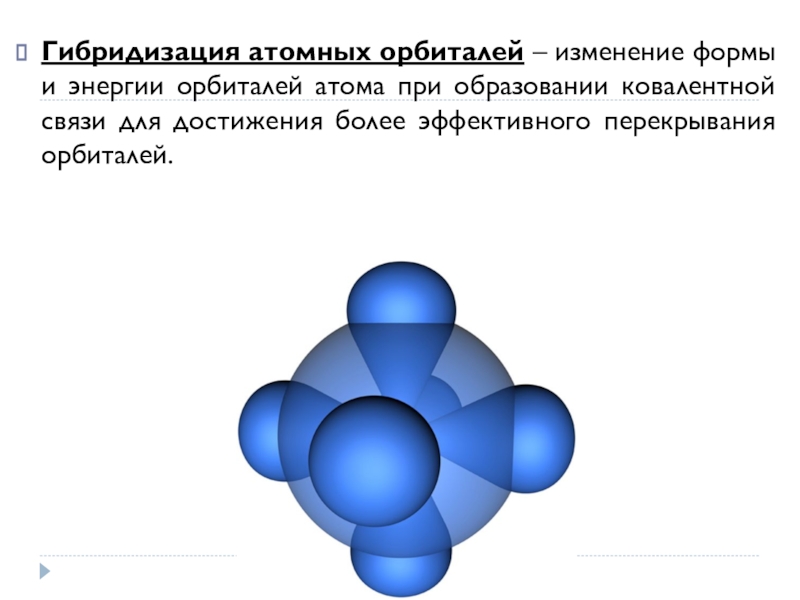
- 11. Гибридизация атомных орбиталей – изменение формы и энергии
- 12. Слайд 12
- 13. Форма гибридной орбитали за счет комбинации s- и p-атомных
- 14. Органогены в химии:Органогенами называют химические элементы, из
- 15. Понятие о функциональной группе:Функциональная группа-это группа атомов,
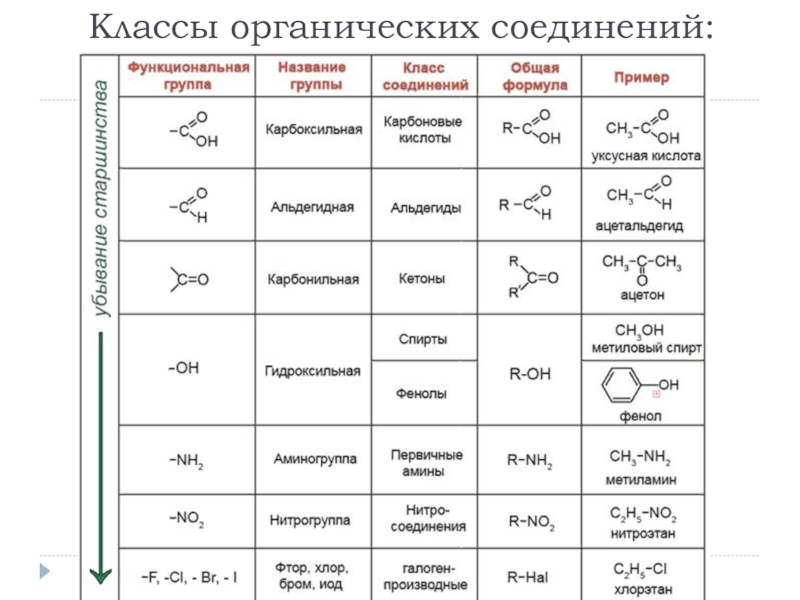
- 16. Классы органических соединений:
- 17. Теория строения Бутлерова Теория химического строения органических
- 18. Положения теории:1. Атомы в молекулах органических веществ соединены
- 19. Формулы строения: а) структурная формула - описывает
- 20. Формулы строения:б) молекулярная (брутто) формула показывает только,
- 21. 2. Свойства органических веществ зависят не только от
- 22. Изомерия:Способность атомов углерода соединяться в различном порядке
- 23. Виды изомерии:Существует два основных типа изомерии –
- 24. Различают три вида структурной изомерии: • вид изомерии,
- 25. • вид изомерии, связанный с изменением места расположения
- 26. • межклассовая изомерия. Изомеры имеют одинаковую молекулярную формулу,
- 27. Пространственная изомерия:Пространственная изомерия обусловливается различным расположением атомов
- 28. б)Оптическая (зеркальная), она возможна при наличии ассиметричного атома углерода (при атоме углерода 4 разных заместителя)
- 29. Теория строения Бутлерова:3. Молекула каждого вещества обладает определенным
- 30. Теория строения Бутлерова:4. Атомы или группы атомов, образующие
- 31. Значение теории Бутлерова:Теория Бутлерова явилась научным фундаментом
Проблемные вопросы:Почему углерод называют элементом жизни?Какие вещества относятся к органическим?Какие теории химии вам уже известны, какое значение они дали для изучения химии?
Слайд 1 Лекция 1. Предмет органической химии
ОБЛАСТНОЕ ГОСУДАРСТВЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«РЯЗАНСКИЙ МЕДИЦИНСКИЙ
Слайд 2Проблемные вопросы:
Почему углерод называют элементом жизни?
Какие вещества относятся к органическим?
Какие теории
химии вам уже известны, какое значение они дали для изучения химии?
Слайд 3Возникновение органической химии как науки-1807 год Йенс Якобс Берцелиус
По Берцелиусу
органические вещества нельзя получить в лаборатории, как неорганические. Они создаются организмами под влиянием «жизненной силы»
Слайд 4История развития органической химии :
1824г. – синтезирована щавелевая кислота (Ф.Вёллер);
1828г. –
синтезирована мочевина (Ф.Вёллер);
1842г. – синтезирован анилин (Н.Н.Зинин);
1845г. – синтезирована уксусная кислота (А.Кольбе);
1847г. – синтезированы карбоновые кислоты (А.Кольбе);
1854г. – синтезированы жиры (М.Бертло);
1861г. – синтезированы сахаристые вещества (А. Бутлеров)
1842г. – синтезирован анилин (Н.Н.Зинин);
1845г. – синтезирована уксусная кислота (А.Кольбе);
1847г. – синтезированы карбоновые кислоты (А.Кольбе);
1854г. – синтезированы жиры (М.Бертло);
1861г. – синтезированы сахаристые вещества (А. Бутлеров)
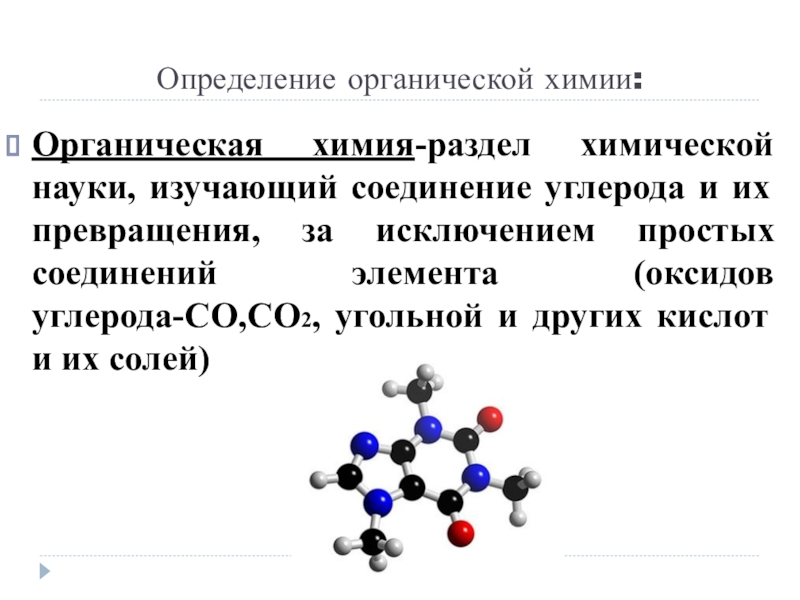
Слайд 6Определение органической химии:
Органическая химия-раздел химической науки, изучающий соединение углерода и их
превращения, за исключением простых соединений элемента (оксидов углерода-CO,CO2, угольной и других кислот и их солей)
Слайд 7Предмет органической химии
Предметом органической химии являются вещества, их строение и свойства,
химические реакции, в которых проявляются химические свойства, закономерности превращения, методы изучения и получения, а также возможные области практического применения этих веществ.
Слайд 8Причины выделения в самостоятельную дисциплину органическую химию:
Многообразие органических соединений
Специфическое строение и
свойства органических соединений
Большое практическое значение соединений углерода: нефть и способы её переработки
Большое практическое значение соединений углерода: нефть и способы её переработки
Слайд 9Признаки органических веществ:
Содержат углерод в валентности 4
Горят или разлагаются с образованием
углеродсодержащих продуктов
Связь в молекуле, как правило, ковалентные
Связь в молекуле, как правило, ковалентные
Слайд 11Гибридизация атомных орбиталей – изменение формы и энергии орбиталей атома при образовании
ковалентной связи для достижения более эффективного перекрывания орбиталей.
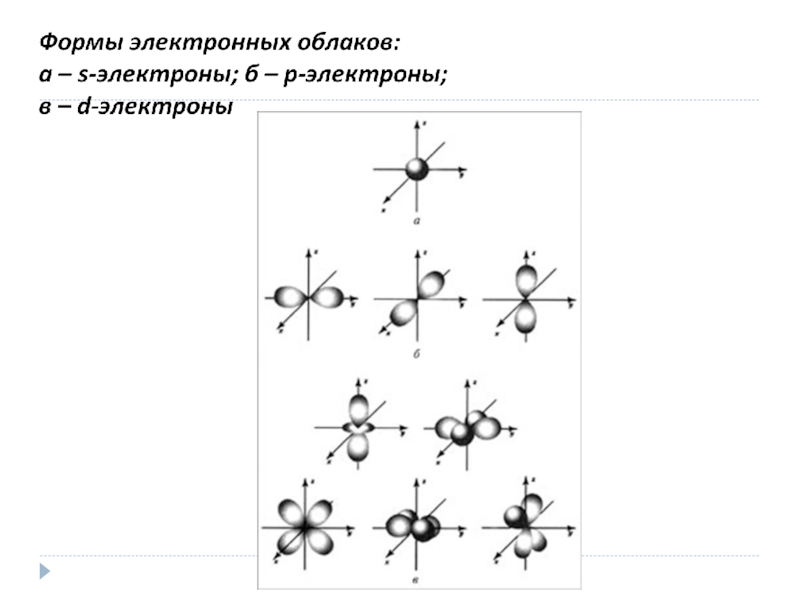
Слайд 13Форма гибридной орбитали за счет комбинации s- и p-атомных орбиталей
гибридная орбиталь больше вытянута
по одну сторону ядра, чем по другую
увеличивается её перекрывание с электронными облаками взаимодействующего атома
образуется более прочная химическая связь
выделяется дополнительная энергия, которая компенсирует затраты энергии на гибридизацию.
увеличивается её перекрывание с электронными облаками взаимодействующего атома
образуется более прочная химическая связь
выделяется дополнительная энергия, которая компенсирует затраты энергии на гибридизацию.
Слайд 14Органогены в химии:
Органогенами называют химические элементы, из атомов которых образованы молекулы
органических веществ, составляющих основу жизни: белков, жиров, углеводов, нуклеиновых кислот, витаминов и др. (C,H,N,P,O,S)
Слайд 15Понятие о функциональной группе:
Функциональная группа-это группа атомов, которая обуславливает характерные химические
свойства (функции) определенного класса органических соединений, ее содержащих.
Слайд 17Теория строения Бутлерова
Теория химического строения органических соединений раскрывает закономерности и
порядок связи атомов друг с другом в молекулах. Разработана А.М. Бутлеровым в 1861г.
Слайд 18Положения теории:
1. Атомы в молекулах органических веществ соединены между собой химическими связями
в определенной последовательности согласно их валентности. Углерод в органических соединениях всегда четырехвалентен.
Слайд 19Формулы строения:
а) структурная формула - описывает порядок соединения атомов в
молекуле, т.е. ее химическое строение. Химические связи в структурной формуле изображают черточками. Связь между водородом и другими атомами обычно не указывается (такие формулы называются сокращенными структурными).
Слайд 20Формулы строения:
б) молекулярная (брутто) формула показывает только, какие элементы и в
каком соотношении входят в состав вещества (т.е. качественный и количественный элементный состав), но не отражает порядка связывания атомов.
Слайд 212. Свойства органических веществ зависят не только от их качественного и количественного
состава, но и от порядка их расположения атомов в молекуле, т.е. от химического строения молекулы.
Например, н-бутан и изобутан имеют одну молекулярную формулу, но разную последовательность связей
Например, н-бутан и изобутан имеют одну молекулярную формулу, но разную последовательность связей
Слайд 22Изомерия:
Способность атомов углерода соединяться в различном порядке друг с другом и
с атомами других элементов, обусловливает явление изомерии.
Вещества, имеющие одинаковый количественный и качественный состав молекул, но различное химическое строение и свойства называются изомерами.
Вещества, имеющие одинаковый количественный и качественный состав молекул, но различное химическое строение и свойства называются изомерами.
Слайд 23Виды изомерии:
Существует два основных типа изомерии – структурная и пространственная.
Структурная изомерия
определяется различным порядком соединения атомов в молекуле.
Слайд 24Различают три вида структурной изомерии:
• вид изомерии, связанный с изменение строения
углеродной цепи, называется изомерией углеродного скелета (изомерией цепи). Например, пентан имеет следующие изомеры:
Слайд 25• вид изомерии, связанный с изменением места расположения кратной связи и /или
атомов и групп атомов (галогенов, гидроксо-, нитрогрупп и др.), заместивших атомы водорода в углеродной цепи, называется изомерией положения. Например,
Слайд 26• межклассовая изомерия. Изомеры имеют одинаковую молекулярную формулу, но относятся к разным
классам органических соединений. Например, этиловый спирт и диметиловый эфир отвечают формуле С2Н6О:
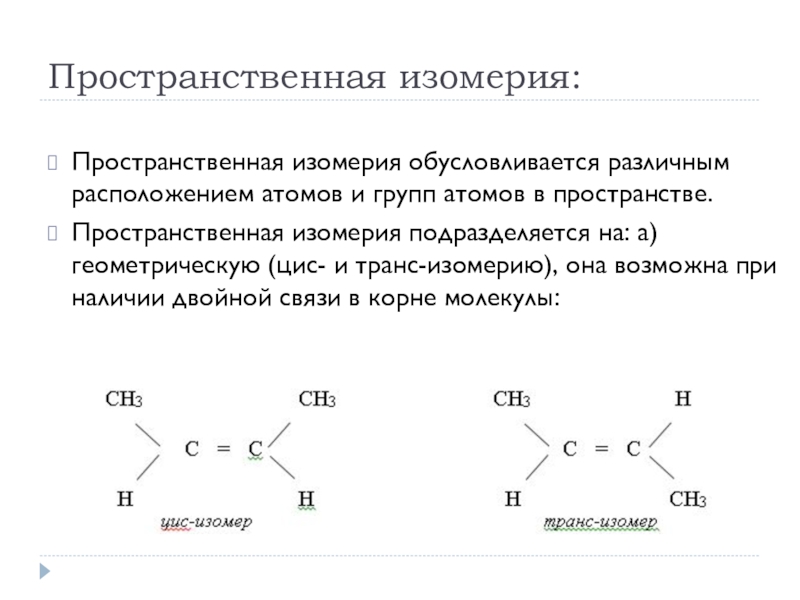
Слайд 27Пространственная изомерия:
Пространственная изомерия обусловливается различным расположением атомов и групп атомов в
пространстве.
Пространственная изомерия подразделяется на: а)геометрическую (цис- и транс-изомерию), она возможна при наличии двойной связи в корне молекулы:
Пространственная изомерия подразделяется на: а)геометрическую (цис- и транс-изомерию), она возможна при наличии двойной связи в корне молекулы:
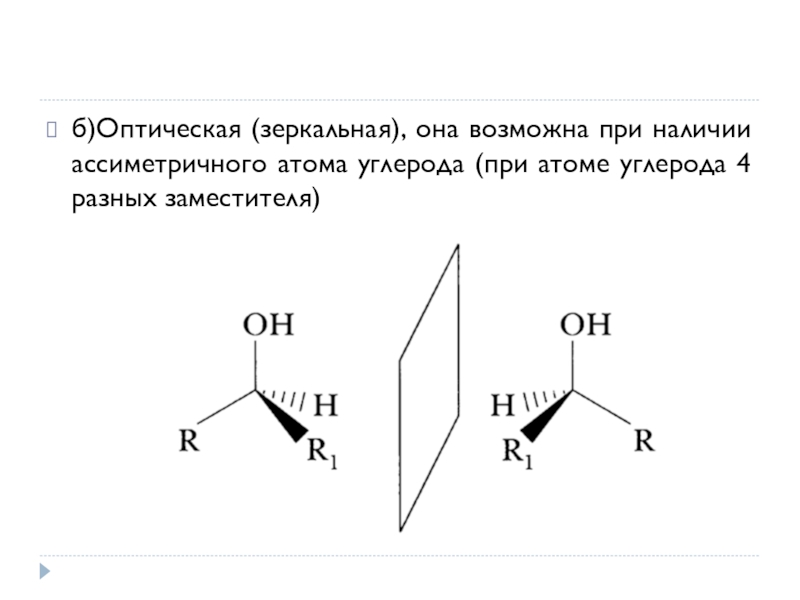
Слайд 28б)Оптическая (зеркальная), она возможна при наличии ассиметричного атома углерода (при атоме
углерода 4 разных заместителя)
Слайд 29Теория строения Бутлерова:
3. Молекула каждого вещества обладает определенным химическим строением, которое может
быть установлено химическими методами. Изучая свойства вещества можно определить химическое строение его молекулы, а по строению молекулы - предвидеть свойства вещества.
Гомологи – вещества этого ряда, или органические вещества, сходные по строению, но отличающиеся друг от друга по составу на одну или несколько групп – СН2 -. Группа – СН2 – называется гомологическая разность.
Гомологи – вещества этого ряда, или органические вещества, сходные по строению, но отличающиеся друг от друга по составу на одну или несколько групп – СН2 -. Группа – СН2 – называется гомологическая разность.
Слайд 30Теория строения Бутлерова:
4. Атомы или группы атомов, образующие молекулу, взаимно влияют друг
на друга, от чего зависят и химические свойства соединения.
Слайд 31Значение теории Бутлерова:
Теория Бутлерова явилась научным фундаментом органической химии и способствовала
быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.