Алканолы
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Предельные одноатомные спирты. Алканолы.
Содержание
- 1. Предельные одноатомные спирты. Алканолы.
- 2. Определение спиртовКлассификация спиртовНоменклатураИзомерияФизические свойстваАномалии у спиртовХимические свойстваФизиологическое действие спиртовПрименение спиртовПолучение спиртовПодведем итогиСодержание
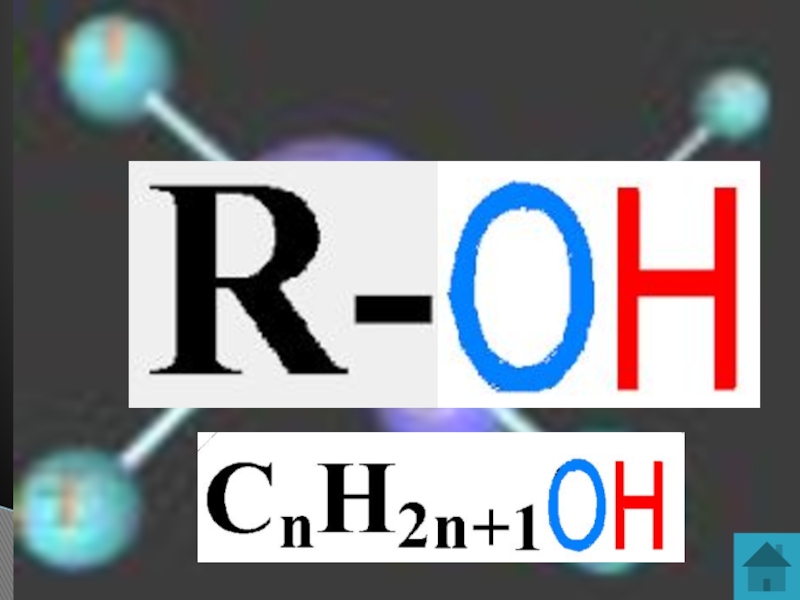
- 3. Спиртами называются органические вещества, молекулы которых содержат
- 4. По характеру углеводородного радикала:СН3СН2ОН спиртыалифатическиеалициклическиеароматическиециклогексанол
- 5. По числу гидроксильных групп: СН3 – ОНметанол
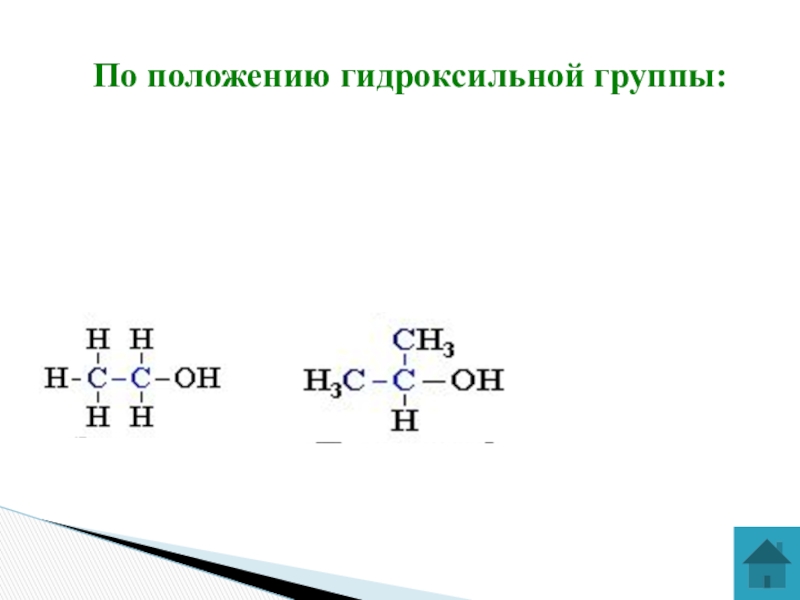
- 6. По положению гидроксильной группы:
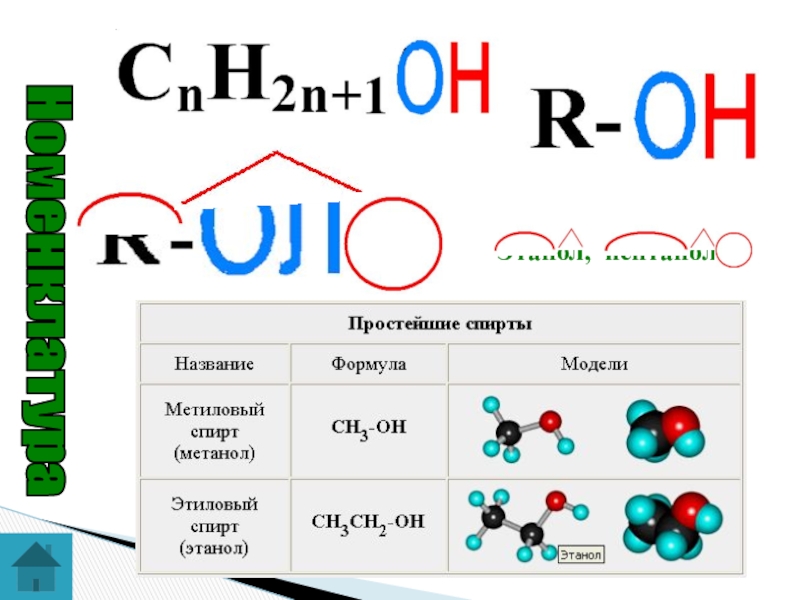
- 7. Этанол, пентанол-2Номенклатура
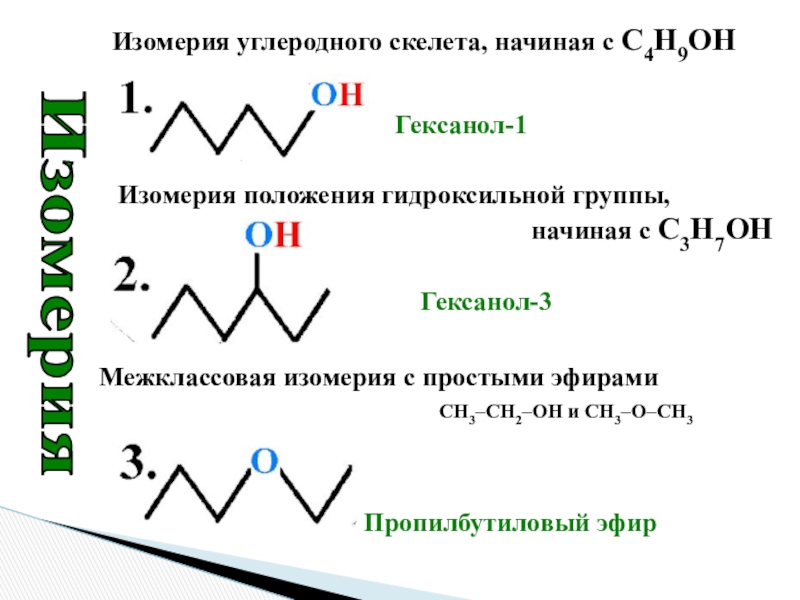
- 8. Гексанол-1Гексанол-3Пропилбутиловый эфирИзомерия Изомерия углеродного скелета, начиная с
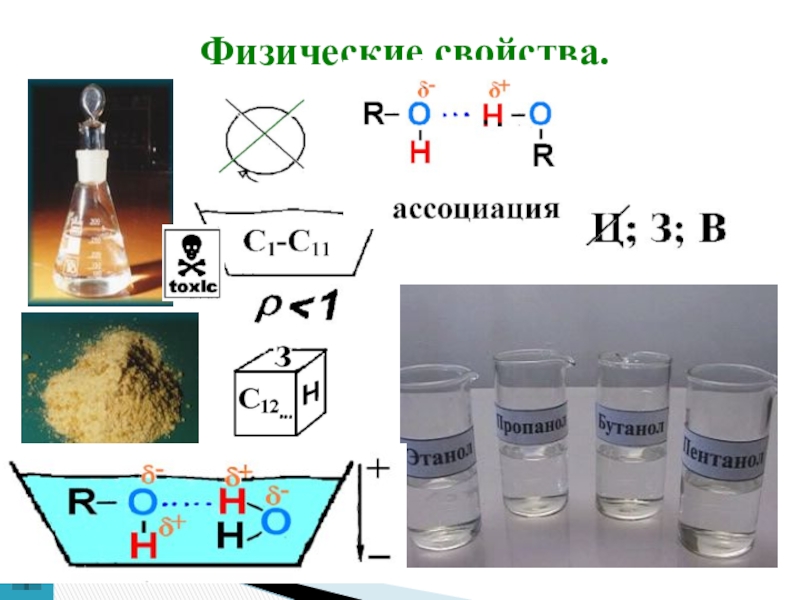
- 9. Физические свойства.
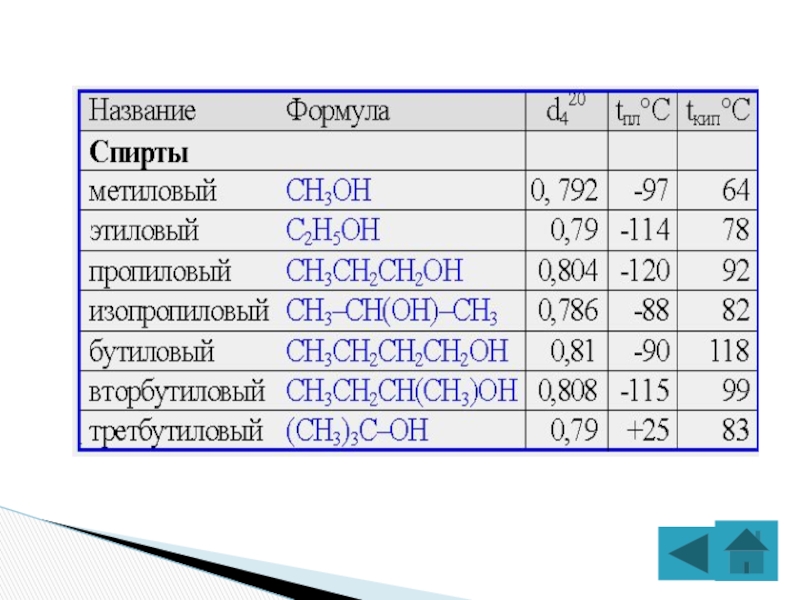
- 10. Слайд 10
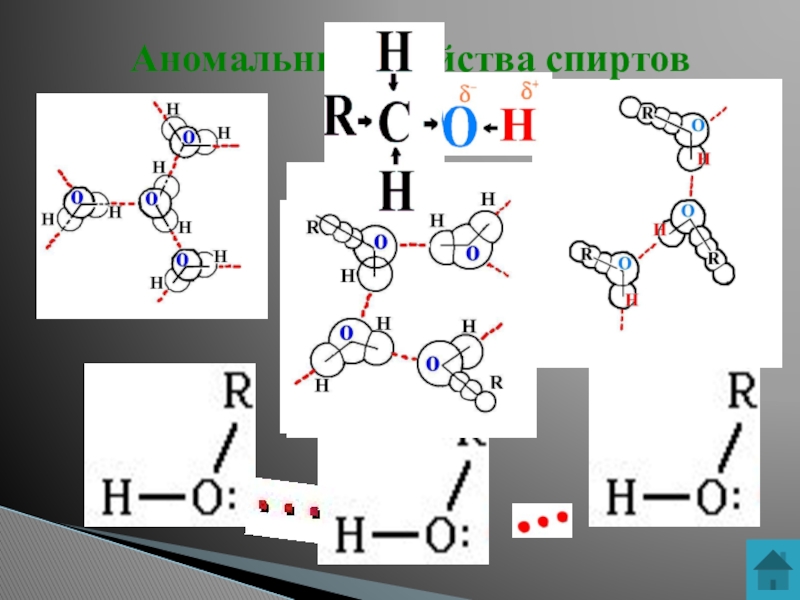
- 11. Аномальные свойства спиртов
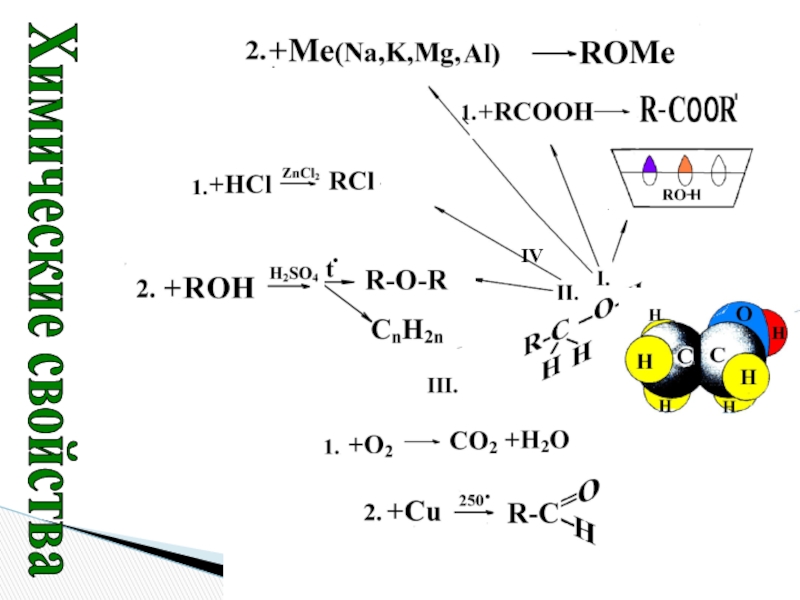
- 12. Химические свойства
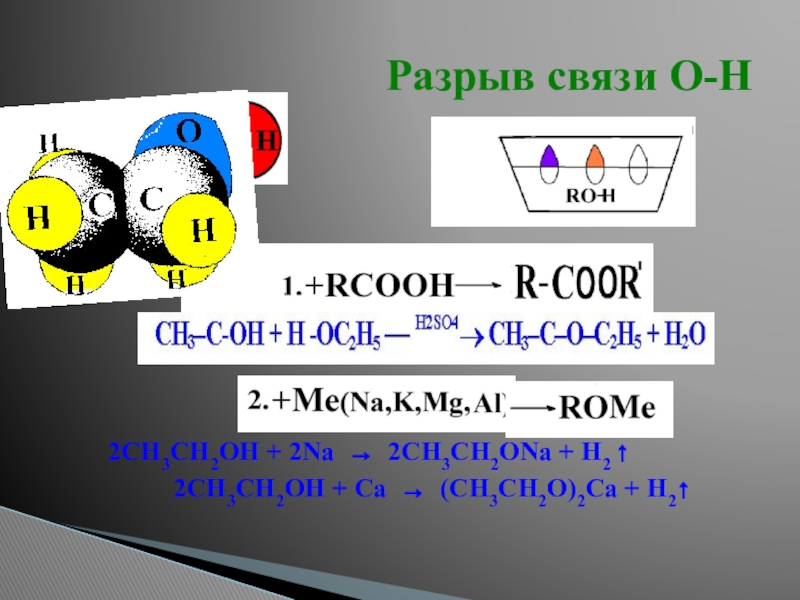
- 13. Разрыв связи О-Н2СH3CH2OH + 2Na ® 2СH3CH2ONa + H2 2СH3CH2OH + Сa ® (СH3CH2O)2Ca + H2
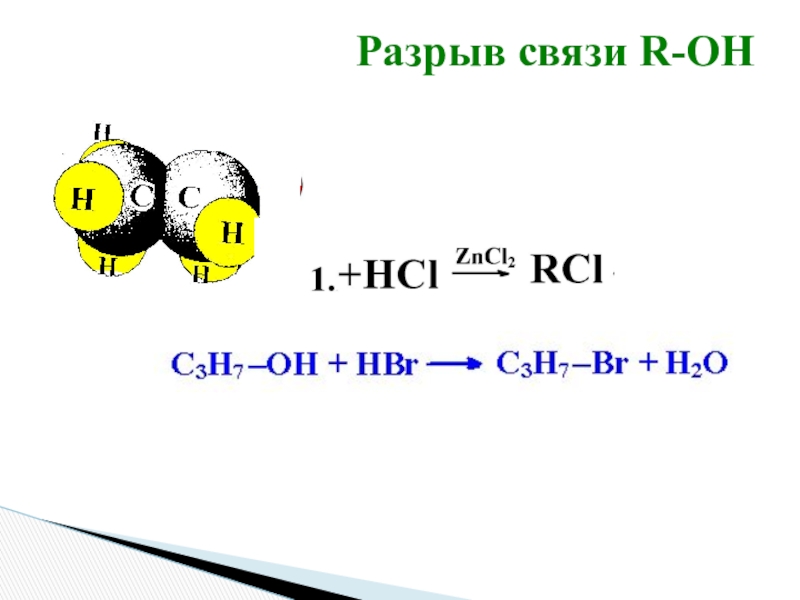
- 14. Разрыв связи R-ОН
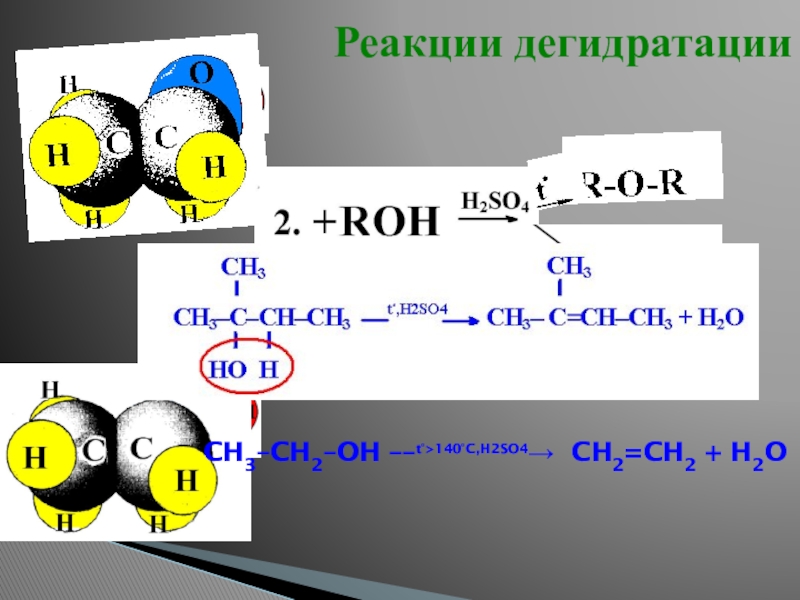
- 15. Реакции дегидратацииCH3–CH2–OH ––t°>140°C,H2SO4→ CH2=CH2 + H2O
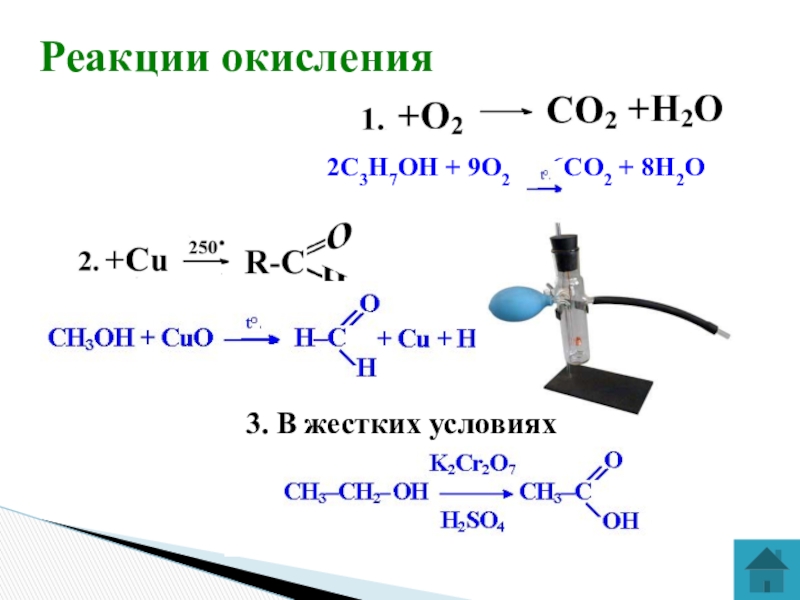
- 16. Реакции окисления2С3H7ОH + 9O2 6СO2 + 8H2O 3. В жестких условиях
- 17. Получение спиртов1. Гидролиз галогенопроизводных углеводородов: СH3–СH2–Br +
- 18. Применение спиртов
- 19. Метанол
- 20. Физиологическое действие В Древней Греции существовал
- 21. Действие вина разнообразно: оно повышает настроение, развязывает
- 22. Возникает ситуация, когда структуры головного мозга уже
- 23. Метиловый спирт - бесцветная жидкость,
- 24. В.Маковский. «Не пущу!»Горький пропойца губит не только
- 25. Шинкарь. ТранковскийА.И. 1879. Мальчика послали
- 26. Слайд 26
- 27. http://realab.kiev.ua/index.php?page=1-25http://www.journals.ru/journals_comments.php?id=2745559http://forum.hq4u.org/topic/29719/page__pid__68942__st__0&http://video.yandex.ru/search.xml?text=%D0%BC%D0%B5%D1%82%D0%B0%D0%BD%D0%BE%D0%BB%20%D0%BF%D1%80%D0%B8%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5&where=all&id=81039460-00http://schools.keldysh.ru/sch1216/students/canis_major/maira.htmХимия . 7-11 класс. Рудзитис Г.Е., Фельдман Ф.Г.(2-х
Слайд 1
Предельные одноатомные спирты
Анисимова И.В. – учитель химии
МБОУ СОШ №2
г.Заринск,
Слайд 2Определение спиртов
Классификация спиртов
Номенклатура
Изомерия
Физические свойства
Аномалии у спиртов
Химические свойства
Физиологическое действие спиртов
Применение спиртов
Получение спиртов
Подведем
Содержание
Слайд 3Спиртами называются органические вещества, молекулы которых содержат одну или несколько функциональных
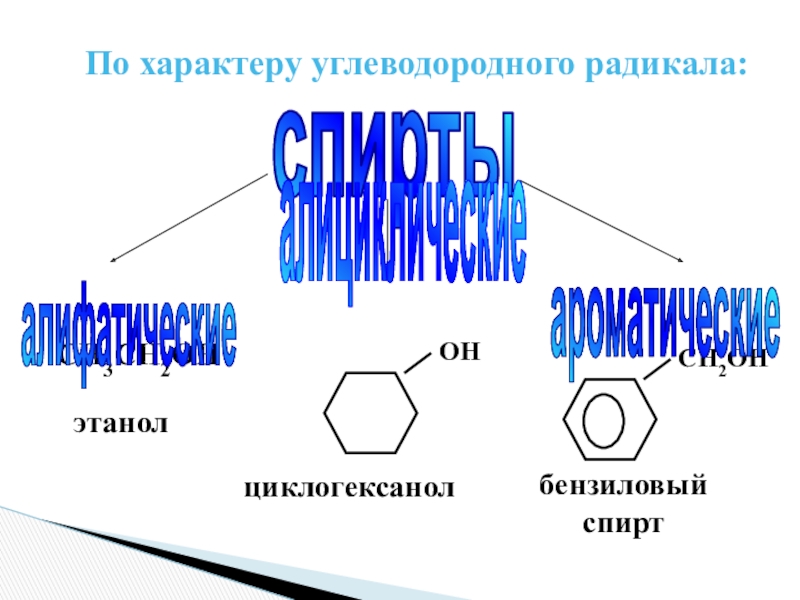
Слайд 4По характеру углеводородного радикала:
СН3СН2ОН
спирты
алифатические
алициклические
ароматические
циклогексанол
этанол
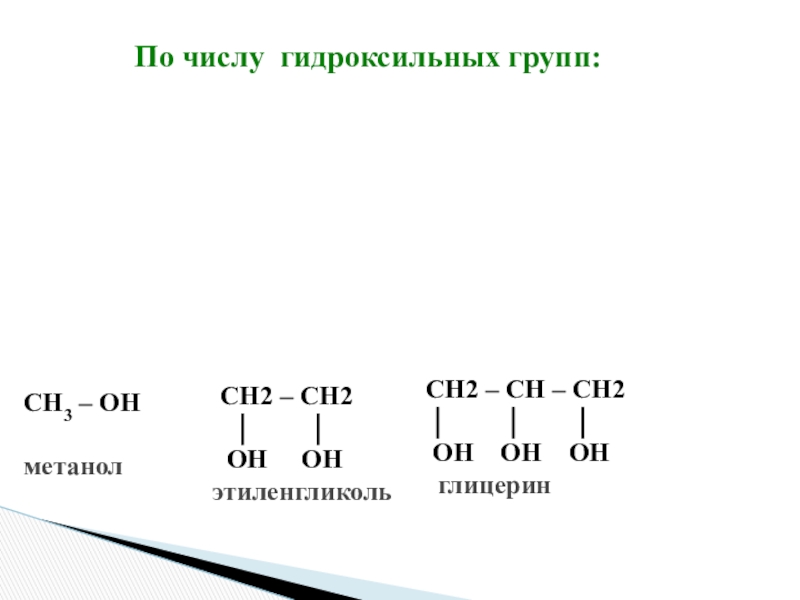
Слайд 5По числу гидроксильных групп:
СН3 – ОН
метанол
СН2 – СН
ОН ОН ОН глицерин
СН2 – СН2
ОН ОН
этиленгликоль
Слайд 8Гексанол-1
Гексанол-3
Пропилбутиловый эфир
Изомерия
Изомерия углеродного скелета, начиная с C4H9OH
Изомерия положения гидроксильной
начиная с С3Н7ОН
Межклассовая изомерия с простыми эфирами
СН3–СН2–ОН и СН3–О–СН3
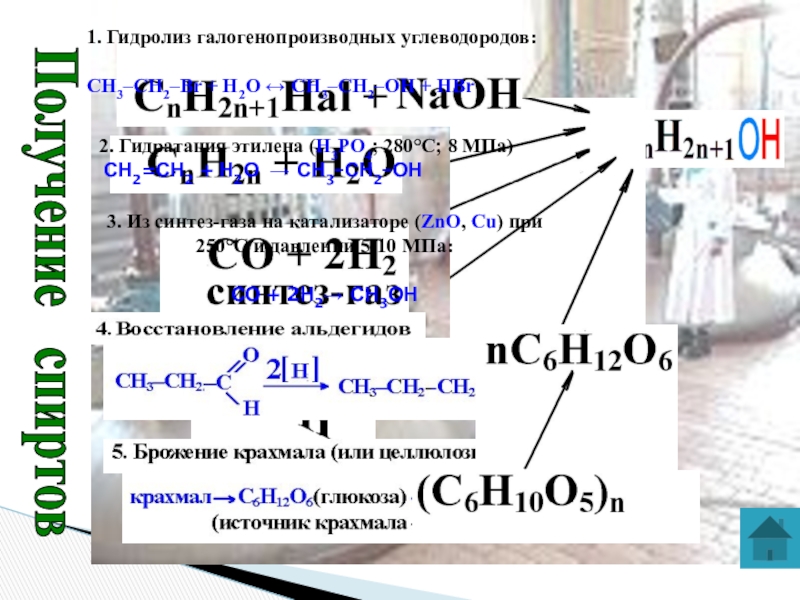
Слайд 17Получение спиртов
1. Гидролиз галогенопроизводных углеводородов:
СH3–СH2–Br + H2O ↔ СH3–CH2–OH +
2. Гидратация этилена (Н3РО4; 280°C; 8 МПа)
СН2=СН2 + Н2О → СН3–СН2–ОН
3. Из синтез-газа на катализаторе (ZnO, Сu) при 250°C и давлении 5-10 МПа:
СО + 2Н2→ СН3ОН
Слайд 20Физиологическое действие
В Древней Греции существовал бог виноделия - Дионис,
В римской мифологии Дионис носил имя Вакх.
Слайд 21Действие вина разнообразно: оно повышает настроение, развязывает языки, иногда вызывает агрессию
Часто пьяный человек засыпает и, если спит достаточно просыпается трезвым.
« Крестьянская пирушка»
Адриан Браувер, Фландрия, 17 в.
Слайд 22Возникает ситуация, когда структуры головного мозга уже не могут функционировать без
а печень не способна его перерабатывать
Этиловый спирт-наркотик , который вследствие высокой растворимости быстро всасывается в кровь.
Слайд 23 Метиловый спирт - бесцветная жидкость, кипящая при температуре 65˚
5 –10 мл метанола вызывают слепоту и сильное отравление организма, а 30 мл могут привести к смертельному исходу.
СН3ОН
МЕТАНОЛ
Слайд 24В.Маковский.
«Не пущу!»
Горький пропойца губит не только свою жизнь, но и
Слайд 25Шинкарь.
ТранковскийА.И. 1879.
Мальчика послали за водкой в шинок. Тогда еще
Постановление Правительства РФ
от
19 августа 1999г. №987
Слайд 27http://realab.kiev.ua/index.php?page=1-25
http://www.journals.ru/journals_comments.php?id=2745559
http://forum.hq4u.org/topic/29719/page__pid__68942__st__0&
http://video.yandex.ru/search.xml?text=%D0%BC%D0%B5%D1%82%D0%B0%D0%BD%D0%BE%D0%BB%20%D0%BF%D1%80%D0%B8%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5&where=all&id=81039460-00
http://schools.keldysh.ru/sch1216/students/canis_major/maira.htm
Химия . 7-11 класс. Рудзитис Г.Е., Фельдман Ф.Г.(2-х частях). М., Просвещение 1985.
Герасимова Н.Ф., Базаева М.В., Супоницкая И.И. Использование опорных конспектов на практических занятиях. //Химия в школе, 1995, №5, с.59-60.
Источники используемого материала