- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Материал презентации использую на факультативе: пока смотрим презентацию придумайте коварную задачку для учителя.
Содержание
- 1. Материал презентации использую на факультативе: пока смотрим презентацию придумайте коварную задачку для учителя.
- 2. Главное меню презентации (Нажимайте на квадратики!!!) Строение
- 3. Строение атомов металловВ настоящее время известно 105
- 4. Плотная кристаллическая структура. Характерный металлический блеск. Высокая
- 5. Все металлы и сплавы, применяемые в настоящее
- 6. Ко второй группе относят цветные металлы и
- 7. Алюминий Калий Золото Нажимайте сюда
- 8. Физические свойства металлов С внешней стороны
- 9. Очень важным свойством металлов является их сравнительно
- 10. Наличием свободных электронов обусловливается и высокая теплопроводность
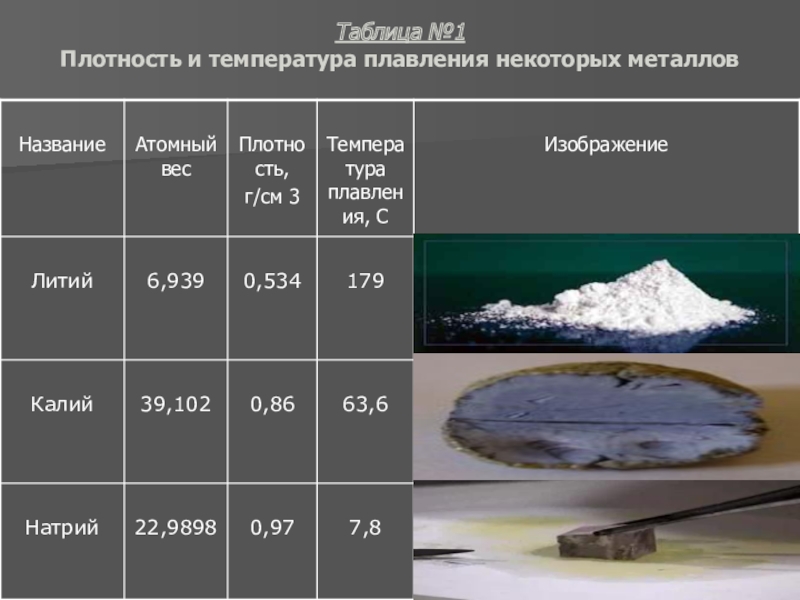
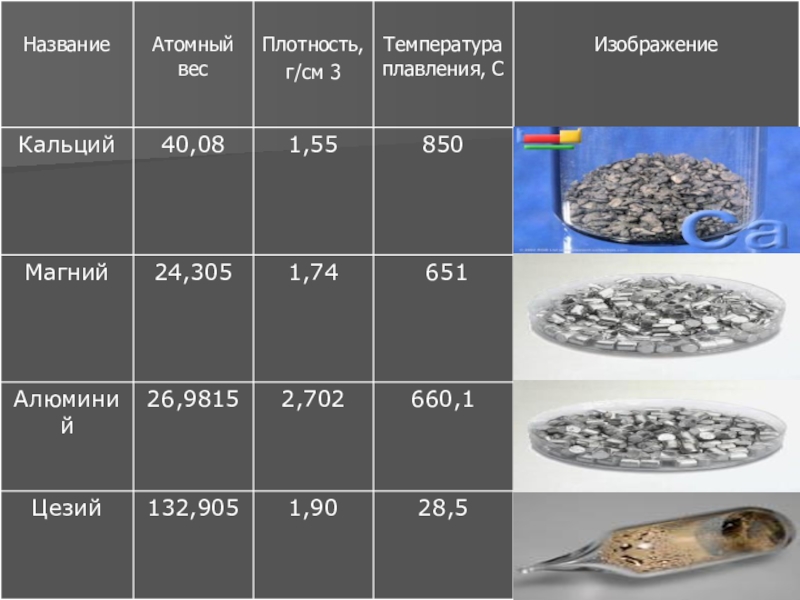
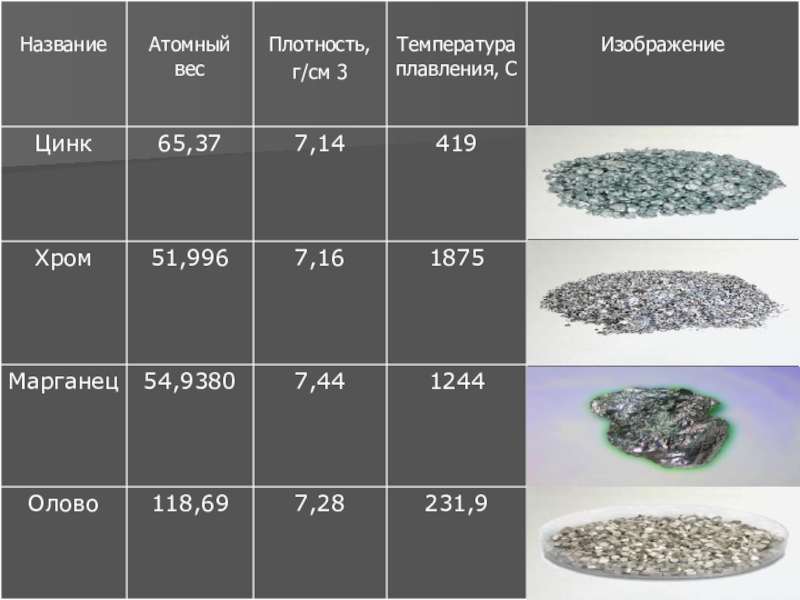
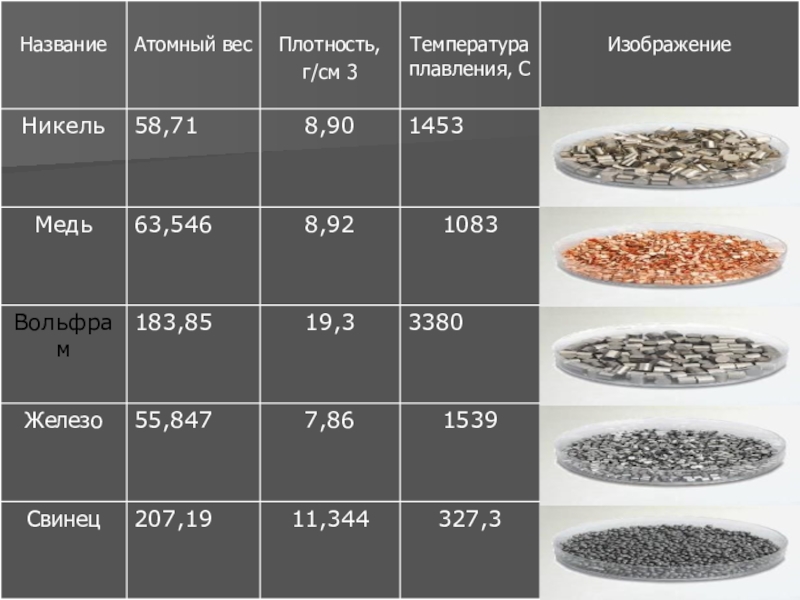
- 11. Таблица №1 Плотность и температура плавления некоторых металлов
- 12. Слайд 12
- 13. Слайд 13
- 14. Слайд 14
- 15. Нажимайте сюда
- 16. Химические свойства металлов Основным химическим свойством
- 17. Из уравнения следует, что эта реакция является
- 18. Ряд напряжений характеризует химические свойства металлов: Чем
- 19. Необходимо отметить, что представленный ряд характеризует поведение
- 20. Коррозия металлов Почти все металлы, приходя в
- 21. Слайд 21
- 22. Слайд 22
- 23. Чистые металлы в большинстве случаев почти не
- 24. Вывод!!!Нужно делать детали для машин (и не только) из золота, платины, серебра, и.т.д.Нажмите!!!
- 25. Понятие о сплавах Характерной особенностью металлов
- 26. Способы получения металлов Огромное большинство металлов находится
- 27. Спасибо за внимание!!!Если вы желаете просмотреть презентацию ещё раз то нажмите на кнопку:
Главное меню презентации (Нажимайте на квадратики!!!) Строение атомов металлов Физические свойства металлов Таблица №1 Коррозия металлов Понятие о сплавах Способы получения металлов Химические свойства металлов Посмотреть ещё раз23456701
Слайд 2Главное меню презентации (Нажимайте на квадратики!!!)
Строение атомов металлов
Физические
свойства металлов
Таблица №1
Коррозия металлов
Понятие о сплавах
Способы получения металлов
Химические свойства металлов
Посмотреть ещё раз
Таблица №1
Коррозия металлов
Понятие о сплавах
Способы получения металлов
Химические свойства металлов
Посмотреть ещё раз
2
3
4
5
6
7
0
1
Слайд 3Строение атомов металлов
В настоящее время известно 105 химических элементов, большинство из
них - металлы. Последние весьма распространены в природе и встречаются в виде различных соединений в недрах земли, водах рек, озер, морей, океанов, составе тел животных, растений и даже в атмосфере.
По своим свойствам металлы резко отличаются от неметаллов. Впервые это различие металлов и неметаллов определил М. В. Ломоносов. “Металлы, - писал он, - тела твердые, ковкие блестящие”.
Причисляя тот или иной элемент к разряду металлов, мы имеем в виду наличие у него определенного комплекса свойств:
По своим свойствам металлы резко отличаются от неметаллов. Впервые это различие металлов и неметаллов определил М. В. Ломоносов. “Металлы, - писал он, - тела твердые, ковкие блестящие”.
Причисляя тот или иной элемент к разряду металлов, мы имеем в виду наличие у него определенного комплекса свойств:
Слайд 4Плотная кристаллическая структура.
Характерный металлический блеск.
Высокая теплопроводность и электрическая проводимость.
Уменьшение электрической проводимости с ростом температуры.
Низкие значения потенциала ионизации, т.е. способность легко отдавать электроны.
Ковкость и тягучесть.
Способность к образованию сплавов.
Слайд 5Все металлы и сплавы, применяемые в настоящее время в технике, можно
разделить на две основные группы. К первой из них относят черные металлы - железо и все его сплавы, в которых оно составляет основную часть. Этими сплавами являются чугуны и стали. В технике часто используют так называемые легированные стали. К ним относятся стали, содержащие хром, никель, вольфрам, молибден, ванадий, кобальт, титан и другие металлы. Иногда в легированные стали входят 5-6 различных металлов. Методом легирования получают различные ценные стали, обладающие в одних случаях повышенной прочностью, в других - высокой сопротивляемостью к истиранию, в третьих - коррозионной устойчивостью, т.е. способностью не разрушаться под действием внешней среды.
Слайд 6Ко второй группе относят цветные металлы и их сплавы. Они получили
такое название потому, что имеют различную окраску. Например, медь светло-красная, никель, олово, серебро - белые, свинец - голубовато-белый, золото -желтое. Из сплавов в практике нашли большое применение: бронза - сплав меди с оловом и другими металлами, латунь - сплав меди с цинком, баббит - сплав олова с сурьмой и медью и др.
Это деление на черные и цветные металлы условно.
Наряду с черными и цветными металлами выделяют еще группу благородных металлов: серебро, золото, платину, рутений и некоторые другие. Они названы так потому, что практически не окисляются на воздухе даже при повышенной температуре и не разрушаются при действии на них растворов кислот и щелочей.
Это деление на черные и цветные металлы условно.
Наряду с черными и цветными металлами выделяют еще группу благородных металлов: серебро, золото, платину, рутений и некоторые другие. Они названы так потому, что практически не окисляются на воздухе даже при повышенной температуре и не разрушаются при действии на них растворов кислот и щелочей.
Слайд 8Физические свойства металлов
С внешней стороны металлы, как известно, характеризуются прежде
всего особым “металлическим” блеском, который обусловливается их способностью сильно отражать лучи света. Однако этот блеск наблюдается обыкновенно только в том случае, когда металл образует сплошную компактную массу. Правда, магний и алюминий сохраняют свой блеск, даже будучи превращенными в порошок, но большинство металлов в мелкораздробленном виде имеет черный или темно-серый цвет. Затем типичные металлы обладают высокой тепло- и электропроводностью, причем по способности проводить тепло и ток располагаются в одном и том же порядке: лучшие проводники - серебро и медь, худшие - свинец и ртуть. С повышением температуры электропроводность падает, при понижении температуры, наоборот, увеличивается.
Слайд 9Очень важным свойством металлов является их сравнительно легкая механическая деформируемость. Металлы
пластичны, они хорошо куются, вытягиваются в проволоку, прокатываются в листы и т.п.
Характерные физические свойства металлов находятся в связи с особенностями их внутренней структуры. Согласно современным воззрениям, кристаллы металлов состоят из положительно заряженных ионов и свободных электронов, отщепившихся от соответствующих атомов. Весь кристалл можно себе представить в виде пространственной решетки, узлы которой заняты ионами, а в промежутках между ионами находятся легкоподвижные электроны. Эти электроны постоянно переходят от одних атомов к другим и вращаются вокруг ядра то одного, то другого атома. Так как электроны не связаны с определенными ионами, то уже под влиянием небольшой разности потенциалов они начинают перемещаться в определенном направлении, т.е. возникает электрический ток.
Характерные физические свойства металлов находятся в связи с особенностями их внутренней структуры. Согласно современным воззрениям, кристаллы металлов состоят из положительно заряженных ионов и свободных электронов, отщепившихся от соответствующих атомов. Весь кристалл можно себе представить в виде пространственной решетки, узлы которой заняты ионами, а в промежутках между ионами находятся легкоподвижные электроны. Эти электроны постоянно переходят от одних атомов к другим и вращаются вокруг ядра то одного, то другого атома. Так как электроны не связаны с определенными ионами, то уже под влиянием небольшой разности потенциалов они начинают перемещаться в определенном направлении, т.е. возникает электрический ток.
Слайд 10Наличием свободных электронов обусловливается и высокая теплопроводность металлов. Находясь в непрерывном
движении, электроны постоянно сталкиваются с ионами и обмениваются с ними энергией. Поэтому колебания ионов, усилившиеся в данной части металла вследствие нагревания, сейчас же передаются соседним ионам, от них - следующим и т.д., и тепловое состояние металла быстро выравнивается; вся масса металла принимает одинаковую температуру.
По плотности металлы условно подразделяются на две большие группы: легкие металлы, плотность которых не больше 5 г/см 3 , и тяжелые металлы - все остальные. Плотность, а также температуры плавления некоторых металлов приведены в таблице №1.
По плотности металлы условно подразделяются на две большие группы: легкие металлы, плотность которых не больше 5 г/см 3 , и тяжелые металлы - все остальные. Плотность, а также температуры плавления некоторых металлов приведены в таблице №1.
Слайд 16Химические свойства металлов
Основным химическим свойством металлов является способность их атомов
легко отдавать свои валентные электроны и переходить в положительно заряженные ионы. Типичные металлы никогда не присоединяют электронов; их ионы всегда заряжены положительно.
Легко отдавая при химических реакциях свои валентные электроны, типичные металлы являются энергичными восстановителями.
Способность к отдаче электронов проявляется у отдельных металлов далеко не в одинаковой степени. Чем легче металл отдает свои электроны, тем он активнее, тем энергичнее вступает во взаимодействие с другими веществами.
Опустим кусочек цинка в раствор какой-нибудь свинцовой соли. Цинк начинает растворяться, а из раствора выделяется свинец. Реакция выражается уравнением:
Zn + Pb(NO 3 ) 2 = Pb + Zn(NO 3 ) 2
Легко отдавая при химических реакциях свои валентные электроны, типичные металлы являются энергичными восстановителями.
Способность к отдаче электронов проявляется у отдельных металлов далеко не в одинаковой степени. Чем легче металл отдает свои электроны, тем он активнее, тем энергичнее вступает во взаимодействие с другими веществами.
Опустим кусочек цинка в раствор какой-нибудь свинцовой соли. Цинк начинает растворяться, а из раствора выделяется свинец. Реакция выражается уравнением:
Zn + Pb(NO 3 ) 2 = Pb + Zn(NO 3 ) 2
Слайд 17Из уравнения следует, что эта реакция является типичной реакцией окисления-восстановления. Сущность
ее сводится к тому, что атомы цинка отдают свои валентные электроны ионам двухвалентного свинца, тем самым превращаясь в ионы цинка, а ионы свинца восстанавливаются и выделяются в виде металлического свинца. Если поступить наоборот, то есть погрузить кусочек свинца в раствор цинковой соли, то никакой реакции не произойдет. Это показывает, что цинк более активен, чем свинец, что его атомы легче отдают, а ионы труднее присоединяют электроны, чем атомы и ионы свинца.
Вытеснение одних металлов из их соединений другими металлами впервые было подробно изучено русским ученым Бекетовым, расположившим металлы по их убывающей химической активности в так называемый “вытеснительный ряд”. В настоящее время вытеснительный ряд Бекетова носит название ряда напряжений.
В таблице №2 представлены значения стандартных электродных потенциалов некоторых металлов. Символом Me + /Me обозначен металл Me, погруженный в раствор его соли. Стандартные потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-”, а знаком “+” отмечены стандартные потенциалы электродов, являющихся окислителями
Вытеснение одних металлов из их соединений другими металлами впервые было подробно изучено русским ученым Бекетовым, расположившим металлы по их убывающей химической активности в так называемый “вытеснительный ряд”. В настоящее время вытеснительный ряд Бекетова носит название ряда напряжений.
В таблице №2 представлены значения стандартных электродных потенциалов некоторых металлов. Символом Me + /Me обозначен металл Me, погруженный в раствор его соли. Стандартные потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-”, а знаком “+” отмечены стандартные потенциалы электродов, являющихся окислителями
Слайд 18Ряд напряжений характеризует химические свойства металлов:
Чем меньше электродный потенциал металла,
тем больше его восстановительная способность.
Каждый металл способен вытеснять(восстанавливать) из растворов солей те металлы, которые стоят в ряду напряжений после него.
Все металлы, имеющие отрицательный стандартный электродный потенциал, то есть находящиеся в ряду напряжений левее водорода, способны вытеснять его из растворов кислот.
Каждый металл способен вытеснять(восстанавливать) из растворов солей те металлы, которые стоят в ряду напряжений после него.
Все металлы, имеющие отрицательный стандартный электродный потенциал, то есть находящиеся в ряду напряжений левее водорода, способны вытеснять его из растворов кислот.
Слайд 19Необходимо отметить, что представленный ряд характеризует поведение металлов и их солей
только в водных растворах и при комнатной температуре. Кроме того, нужно иметь ввиду, что высокая электрохимическая активность металлов не всегда означает его высокую химическую активность. Например, ряд напряжений начинается литием, тогда как более активные в химическом отношении рубидий и калий находятся правее лития. Это связано с исключительно высокой энергией процесса гидратации ионов лития по сравнению с ионами других щелочных металлов.
Нажмите сюда
Слайд 20Коррозия металлов
Почти все металлы, приходя в соприкосновение с окружающей их
газообразной или жидкой средой, более или менее быстро подвергаются с поверхности разрушению. Причиной его является химическое взаимодействие металлов с находящимися в воздухе газами, а также водой и растворенными в ней веществами.
Всякий процесс химического разрушения металлов под действием окружающей среды называют коррозией.
Проще всего протекает коррозия при соприкосновении металлов с газами. На поверхности металла образуются соответствующие соединения: оксиды, сернистые соединения, основные соли угольной кислоты, которые нередко покрывают поверхность плотным слоем, защищающим металл от дальнейшего воздействия тех же газов.
Иначе обстоит дело при соприкосновении металла с жидкой средой - водой и растворенными в ней веществами. Образующиеся при этом соединения могут растворяться, благодаря чему коррозия распространяется дальше вглубь металла. Кроме того, вода, содержащая растворенные вещества, является проводником электрического тока, вследствие чего постоянно возникают электрохимические процессы, которые являются одним из главных факторов, обуславливающих и ускоряющих коррозию.
Всякий процесс химического разрушения металлов под действием окружающей среды называют коррозией.
Проще всего протекает коррозия при соприкосновении металлов с газами. На поверхности металла образуются соответствующие соединения: оксиды, сернистые соединения, основные соли угольной кислоты, которые нередко покрывают поверхность плотным слоем, защищающим металл от дальнейшего воздействия тех же газов.
Иначе обстоит дело при соприкосновении металла с жидкой средой - водой и растворенными в ней веществами. Образующиеся при этом соединения могут растворяться, благодаря чему коррозия распространяется дальше вглубь металла. Кроме того, вода, содержащая растворенные вещества, является проводником электрического тока, вследствие чего постоянно возникают электрохимические процессы, которые являются одним из главных факторов, обуславливающих и ускоряющих коррозию.
Слайд 23Чистые металлы в большинстве случаев почти не подвергаются коррозии. Даже такой
металл, как железо, в совершенно чистом виде почти не ржавеет. Но обыкновенные технические металлы всегда содержат различные примеси, что создает благоприятные условия для коррозии.
Убытки, причиняемые коррозией металлов, огромны. Вычислено, например, что вследствие коррозии ежегодно гибнет такое количество стали, которое равно приблизительно четверти всей мировой добычи его за год. Поэтому изучению процессов коррозии и отысканию наилучших средств ее предотвращения уделяется очень много внимания.
Способы борьбы с коррозией чрезвычайно разнообразны. Наиболее простой из них заключается в защите поверхности металла от непосредственного соприкосновения с окружающей средой путем покрытия масляной краской, лаком, эмалью или, наконец, тонким слоем другого металла. Особый интерес с теоретической точки зрения представляет покрытие одного металла другим.
К ним относятся: катодное покрытие, когда защищающий металл стоит в ряду напряжений правее защищающего (типичным примером может служить луженая, то есть покрытая оловом, сталь); анодное покрытие, например, покрытие стали цинком.
Убытки, причиняемые коррозией металлов, огромны. Вычислено, например, что вследствие коррозии ежегодно гибнет такое количество стали, которое равно приблизительно четверти всей мировой добычи его за год. Поэтому изучению процессов коррозии и отысканию наилучших средств ее предотвращения уделяется очень много внимания.
Способы борьбы с коррозией чрезвычайно разнообразны. Наиболее простой из них заключается в защите поверхности металла от непосредственного соприкосновения с окружающей средой путем покрытия масляной краской, лаком, эмалью или, наконец, тонким слоем другого металла. Особый интерес с теоретической точки зрения представляет покрытие одного металла другим.
К ним относятся: катодное покрытие, когда защищающий металл стоит в ряду напряжений правее защищающего (типичным примером может служить луженая, то есть покрытая оловом, сталь); анодное покрытие, например, покрытие стали цинком.
Слайд 24Вывод!!!
Нужно делать детали для машин (и не только) из золота, платины,
серебра, и.т.д.
Нажмите!!!
Слайд 25Понятие о сплавах
Характерной особенностью металлов является их способность образовывать друг
с другом или с неметаллами сплавы. Чтобы получить сплав, смесь металлов обычно подвергают плавлению, а затем охлаждают с различной скоростью, которая определяется природой компонентов и изменением характера их взаимодействия в зависимости от температуры. Иногда сплавы получают спеканием тонких порошков металлов, не прибегая к плавлению (порошковая металлургия). Итак сплавы - это продукты химического взаимодействия металлов.
Кристаллическая структура сплавов во многом подобна чистым металлам, которые, взаимодействуя друг с другом при плавлении и последующей кристаллизации, образуют: а) химические соединения, называемые интерметаллидами; б) твердые растворы; в) механическую смесь кристаллов компонентов.
Тот или иной тип взаимодействия определяется соотношением энергии взаимодействия разнородных и однородных частиц системы, то есть соотношением энергий взаимодействия атомов в чистых металлах и сплавах.
Современная техника использует огромное число сплавов, причем в подавляющем большинстве случаев они состоят не из двух, а из трех, четырех и большего числа металлов. Интересно, что свойства сплавов часто резко отличаются от свойств индивидуальных металлов, которыми они образованы. Так, сплав, содержащий 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия, плавится всего при 60,5 градусах Цельсия, в то время как компоненты сплава имеют соответственно температуры плавления 271, 327, 232 и 321 градус Цельсия. Твердость оловянной бронзы (90% меди и 10% олова) втрое больше, чем у чистой меди, а коэффициент линейного расширения сплавов железа и никеля в 10 раз меньше, чем у чистых компонентов.
Кристаллическая структура сплавов во многом подобна чистым металлам, которые, взаимодействуя друг с другом при плавлении и последующей кристаллизации, образуют: а) химические соединения, называемые интерметаллидами; б) твердые растворы; в) механическую смесь кристаллов компонентов.
Тот или иной тип взаимодействия определяется соотношением энергии взаимодействия разнородных и однородных частиц системы, то есть соотношением энергий взаимодействия атомов в чистых металлах и сплавах.
Современная техника использует огромное число сплавов, причем в подавляющем большинстве случаев они состоят не из двух, а из трех, четырех и большего числа металлов. Интересно, что свойства сплавов часто резко отличаются от свойств индивидуальных металлов, которыми они образованы. Так, сплав, содержащий 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия, плавится всего при 60,5 градусах Цельсия, в то время как компоненты сплава имеют соответственно температуры плавления 271, 327, 232 и 321 градус Цельсия. Твердость оловянной бронзы (90% меди и 10% олова) втрое больше, чем у чистой меди, а коэффициент линейного расширения сплавов железа и никеля в 10 раз меньше, чем у чистых компонентов.
Слайд 26Способы получения металлов
Огромное большинство металлов находится в природе в виде
соединений с другими элементами.
Только немногие металлы встречаются в свободном состоянии, и тогда они называются самородными. Золото и платина встречаются почти исключительно в самородном виде, серебро и медь - отчасти в самородном виде; иногда попадаются также самородные ртуть, олово и некоторые другие металлы.
Добывание золота и платины производится или посредством механического отделения их от той породы, в которой они заключены, например промывкой воды, или путем извлечения их из породы различными реагентами с последующим выделением металла из раствора. Все остальные металлы добываются химической переработкой их природных соединений.
Минералы и горные породы, содержащие соединения металлов и пригодные для получения этих металлов заводским путем, носят название руд. Главными рудами являются оксиды, сульфиды и карбонаты металлов.
Важнейший способ получения металлов из руд основан на восстановлении их оксидов углем
Только немногие металлы встречаются в свободном состоянии, и тогда они называются самородными. Золото и платина встречаются почти исключительно в самородном виде, серебро и медь - отчасти в самородном виде; иногда попадаются также самородные ртуть, олово и некоторые другие металлы.
Добывание золота и платины производится или посредством механического отделения их от той породы, в которой они заключены, например промывкой воды, или путем извлечения их из породы различными реагентами с последующим выделением металла из раствора. Все остальные металлы добываются химической переработкой их природных соединений.
Минералы и горные породы, содержащие соединения металлов и пригодные для получения этих металлов заводским путем, носят название руд. Главными рудами являются оксиды, сульфиды и карбонаты металлов.
Важнейший способ получения металлов из руд основан на восстановлении их оксидов углем