- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Карбоновые кислоты - презентация мой шедевр:) на все времена:)
Содержание
- 1. Карбоновые кислоты - презентация мой шедевр:) на все времена:)
- 2. План.ВведениеИзомерия и номенклатура Нахождение в природеПолучениеФизические свойстваХимические свойстваПрименение
- 3. Слайд 3
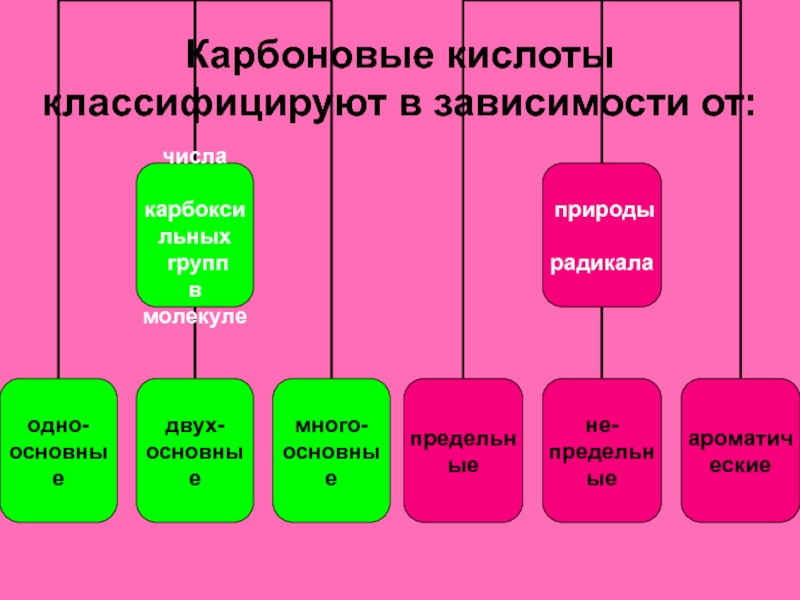
- 4. Карбоновые кислоты классифицируют в зависимости от:
- 5. Изомерия и номенклатура.Для карбоновых кислот характерна изомерия
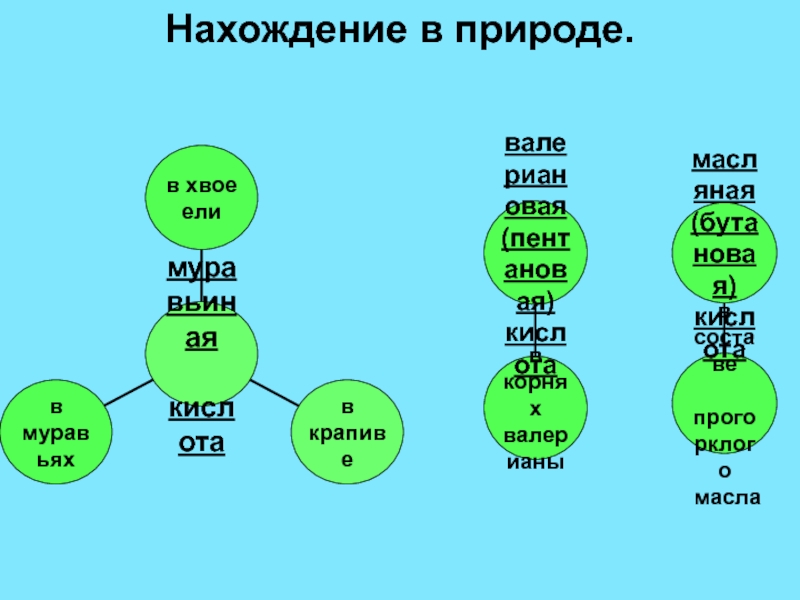
- 6. Нахождение в природе.
- 7. в лаборатории в промышленностиПолучение.из солей, действуяна них
- 8. Физические свойства.Низшие карбоновые кислоты
- 9. Химические свойства.Взаимодействие с металлами (до водорода)
- 10. Применение
- 11. CH3COOH (уксусная кислота)получение лекарствполучение солейполучение ацетатного шелкадля
- 12. Слайд 12
- 13. catcat, pcat, t1.+ O2catR C
Слайд 2План.
Введение
Изомерия и номенклатура
Нахождение в природе
Получение
Физические свойства
Химические свойства
Применение
Слайд 3
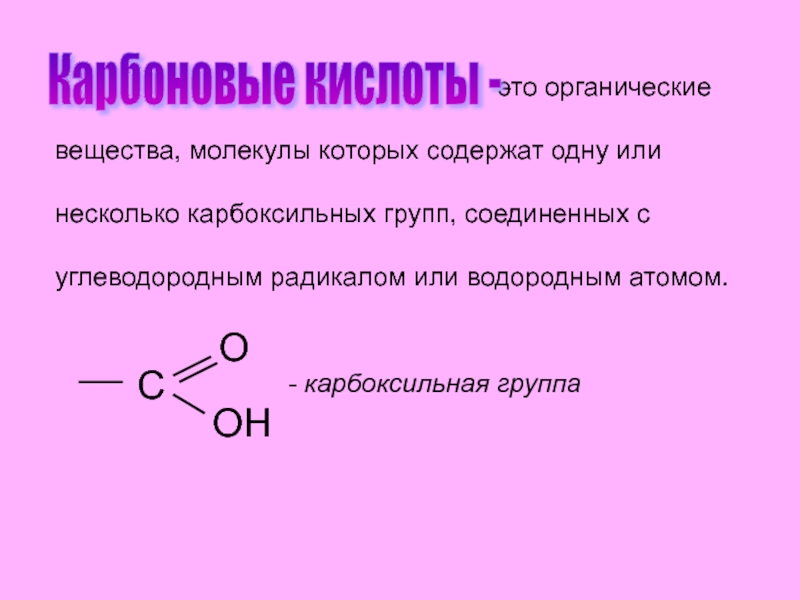
вещества, молекулы которых содержат одну или
несколько карбоксильных групп, соединенных с
углеводородным радикалом или водородным атомом.
Карбоновые кислоты -
С
O
OH
- карбоксильная группа
Слайд 5Изомерия и номенклатура.
Для карбоновых кислот характерна изомерия углеводородного радикала. Он может
По международной номенклатуре названия кислот образуются от названия соответствующих углеводородов с прибавлением окончания –овая и слова «кислота»
название
кислоты
+ -овая «кислота»
название
углеводорода
=
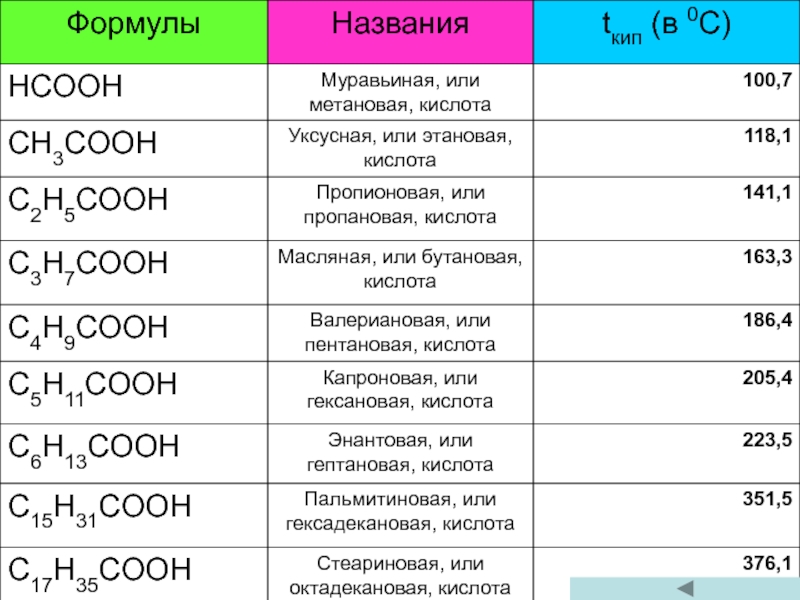
Важнейшие одноосновные предельные кислоты
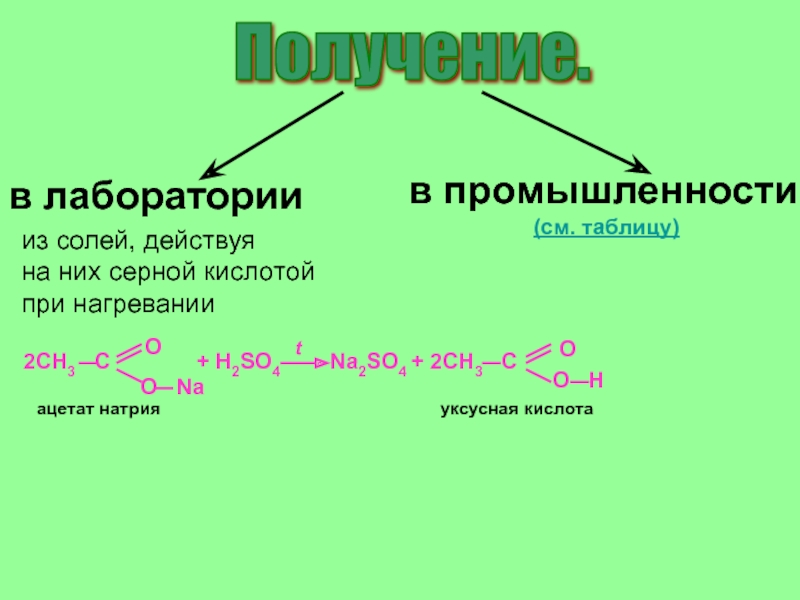
Слайд 7в лаборатории
в промышленности
Получение.
из солей, действуя
на них серной кислотой
при нагревании
2CH3
O
O Na
O H
O
t
ацетат натрия
уксусная кислота
(см. таблицу)
Слайд 8Физические свойства.
Низшие карбоновые кислоты
- хорошо растворимые в воде
- с ↑ относ. молекул. массы растворимость ↓,
а tкип ↑
Высшие кислоты (начиная с пеларгоновой (нонановой) CH3 – (CH2)7 – COOH )
- твердые вещества
- без запаха
- нерастворимые в воде
Слайд 9Химические свойства.
Взаимодействие с
металлами (до водорода)
основными и амфотерными оксидами
2HCOOH + MgO (HCOO)2Mg + H2O
основаниями и амфотерными гидроксидами
2HCOOH + Mg(OH)2 (HCOO)2Mg + 2H2O
солями
2HCOOH + Na2SiO3 2HCOONa + H2SiO3↓
2CH3COOH + Na2CO3 2CH3COONa + H2O + CO2↑
Органические кислоты вступают в реакцию этерификациии со спиртами,
образуя сложные эфиры, согласно уравнению
R C + H OR′ = R C + H2O
O
OH
O
O R′
кислота спирт сложный эфир
CH3COOH + C2H5OH = CH3COOC2H5 + H2O
уксусная кислота этиловый спирт этилацетат
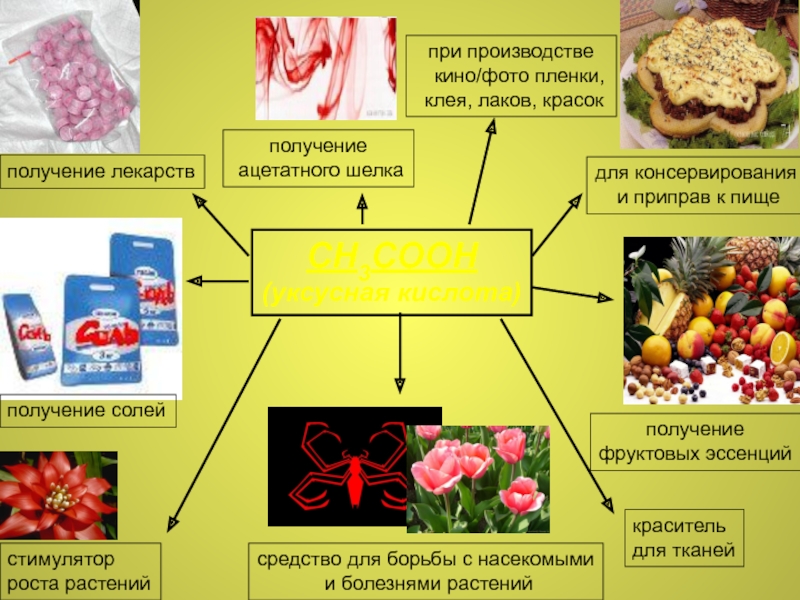
Слайд 11CH3COOH
(уксусная кислота)
получение лекарств
получение солей
получение
ацетатного шелка
для консервирования
и приправ к
получение
фруктовых эссенций
средство для борьбы с насекомыми
и болезнями растений
стимулятор
роста растений
краситель
для тканей
при производстве
кино/фото пленки,
клея, лаков, красок
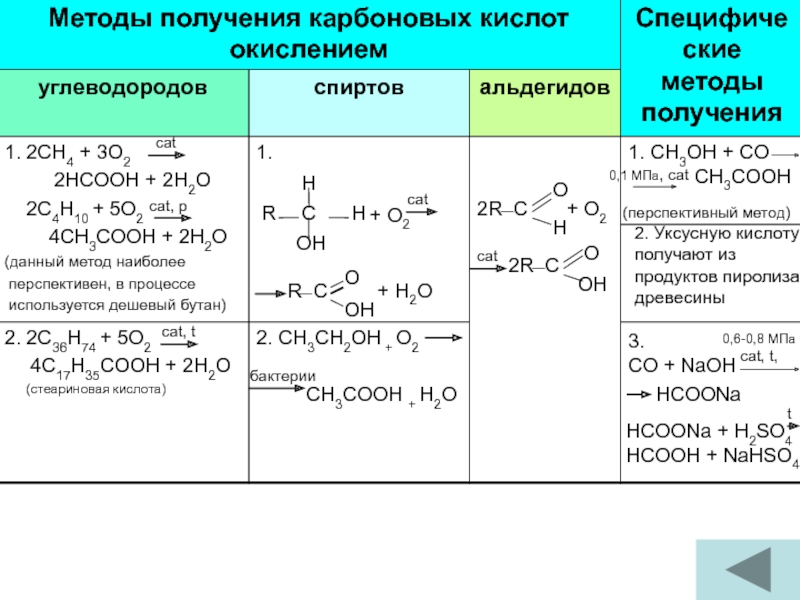
Слайд 13cat
cat, p
cat, t
1.
+ O2
cat
R C + H2O
O
OH
бактерии
2R
O
H
cat
2R C
O
OH
0,1 МПа, cat
(перспективный метод)
0,6-0,8 МПа
cat, t,
HCOONa + H2SO4
HCOOH + NaHSO4
t
3.
2. Уксусную кислоту
получают из
продуктов пиролиза
древесины