- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Карбоновые кислоты, когда переходила на другой учебник
Содержание
- 1. Карбоновые кислоты, когда переходила на другой учебник
- 2. Содержание.1.Карбо́новые кисло́ты.2.Классификация.3.Химические свойства.4.Физические свойства.5.Применение.
- 3. Карбо́новые кисло́тыКарбо́новые кисло́ты — класс органических соединений, молекулы
- 4. Классификация. В зависимости от радикала, связанного
- 5. Характерные химические реакции.Наиболее важные химические свойства, характерные
- 6. 2) Карбоновые кислоты в присутствии кислого катализатора
- 7. Физические свойства. Низшие карбоновые кислоты — жидкости с
Содержание.1.Карбо́новые кисло́ты.2.Классификация.3.Химические свойства.4.Физические свойства.5.Применение.
Слайд 2Содержание.
1.Карбо́новые кисло́ты.
2.Классификация.
3.Химические свойства.
4.Физические свойства.
5.Применение.
Слайд 3Карбо́новые кисло́ты
Карбо́новые кисло́ты — класс органических соединений, молекулы которого содержат одну или
несколько функциональных карбоксильных групп -COOH. Кислые свойства объясняются тем, что данная группа может сравнительно легко отщеплять протон. За редкими исключениями карбоновые кислоты являются слабыми. Например, уксусная кислота CH3COOH.
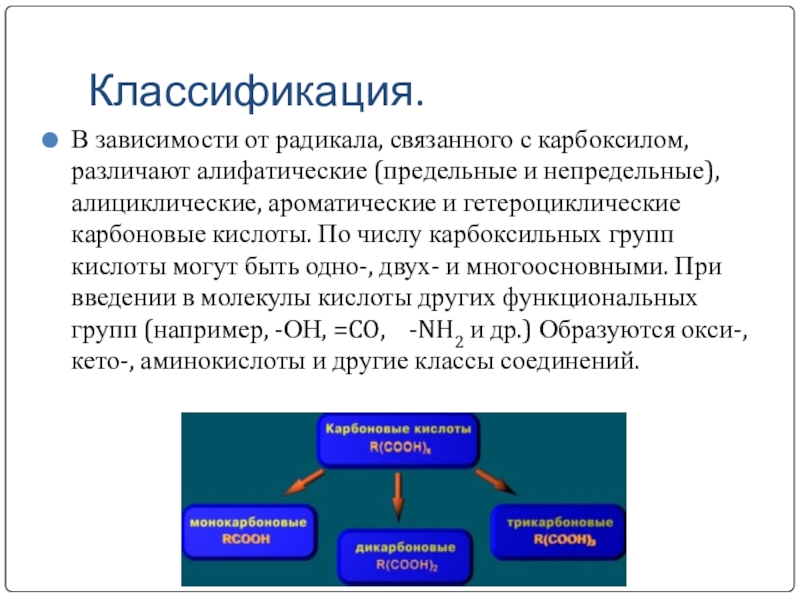
Слайд 4Классификация.
В зависимости от радикала, связанного с карбоксилом, различают алифатические
(предельные и непредельные), алициклические, ароматические и гетероциклические карбоновые кислоты. По числу карбоксильных групп кислоты могут быть одно-, двух- и многоосновными. При введении в молекулы кислоты других функциональных групп (например, -ОН, =CO, -NH2 и др.) Образуются окси-, кето-, аминокислоты и другие классы соединений.
Слайд 5Характерные химические реакции.
Наиболее важные химические свойства, характерные для большинства карбоновых кислот:
1)
Карбоновые кислоты при реакции с металлами или их осно́вными гидроксидами дают соли соответствующих металлов:
2 CH3COOH + Mg = (CH3COO)2Mg + H2
CH3COOH + NaOH = CH3COONa + H2O
Также карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
CH3COOH + NaHCO3 = CH3COONa + H2O + CO2
2 CH3COOH + Mg = (CH3COO)2Mg + H2
CH3COOH + NaOH = CH3COONa + H2O
Также карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
CH3COOH + NaHCO3 = CH3COONa + H2O + CO2
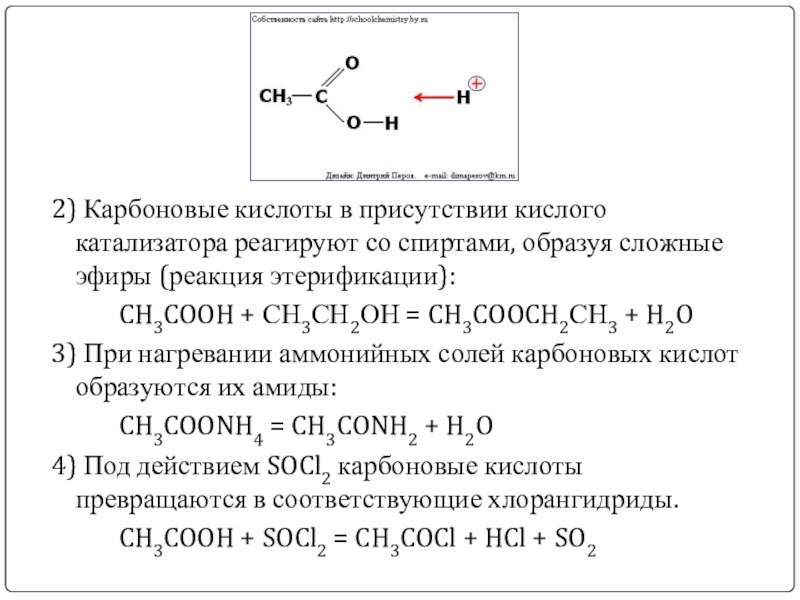
Слайд 62) Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя
сложные эфиры (реакция этерификации):
CH3COOH + СН3СН2ОН = CH3COOCH2СН3 + H2O
3) При нагревании аммонийных солей карбоновых кислот образуются их амиды:
CH3COONH4 = CH3CONH2 + H2O
4) Под действием SOCl2 карбоновые кислоты превращаются в соответствующие хлорангидриды.
CH3COOH + SOCl2 = CH3COCl + HCl + SO2
CH3COOH + СН3СН2ОН = CH3COOCH2СН3 + H2O
3) При нагревании аммонийных солей карбоновых кислот образуются их амиды:
CH3COONH4 = CH3CONH2 + H2O
4) Под действием SOCl2 карбоновые кислоты превращаются в соответствующие хлорангидриды.
CH3COOH + SOCl2 = CH3COCl + HCl + SO2
Слайд 7Физические свойства.
Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые
в воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой (н-нонановой) СН3-(СН2)7-СООН, — твердые вещества, без запаха, нерастворимые в воде. Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота.