Подготовила: Шамина Виктория Викторовна
учитель химии
МОУ «Грицовский ЦО им.Д.С.Сидорова»
Веневский район, Тульская область
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Использование заданий повышенной сложности по теме Строение атома при подготовке к ЕГЭ
Содержание
- 1. Использование заданий повышенной сложности по теме Строение атома при подготовке к ЕГЭ
- 2. Методика обучения школьников теме «Строение атома» на
- 3. Формы разработанных заданий:1. множественный выбор (один вопрос,
- 4. Основные цели создания тестов:1. закрепление сформированных на
- 5. Тест 1 Состав ядра атома. Изотопы. 1.
- 6. Слайд 6
- 7. 4.
- 8. 8. Установите соответствие.
- 9. Тест 2 Строение электронной оболочки
- 10. 4. Выберите правильные ответы.
- 11. Слайд 11
- 12. 4. Максимально возможное число электронов на
- 13. 4. Заполните пропуски: Составьте схемы электронного
- 14. 6. Установите соответствие.
- 15. Тест 4 Ионы. 1.
- 16. 2. Впишите обозначения
- 17. 5. Выберите правильные ответы из предложенных
- 18. Спасибо за внимание!!!
Слайд 1Презентация на тему: «Использование заданий повышенной сложности по теме «Строение атома» при
Слайд 2Методика обучения школьников теме «Строение атома» на углубленном уровне включает в
1. набор исследовательских заданий, выполняя которые учащийся
открывает для себя теоретические знания;
2. нестандартизированный набор заданий для формирования
предметных умений, рассчитанный на участие учителя в
организации контроля и оценки правильности выполнения;
3. стандартизированные наборы тестовых заданий, позволяющие
автоматизировать контроль и оценку, установить
своевременную обратную связь с целью последующей
коррекции знаний и умений.
Слайд 3Формы разработанных заданий:
1. множественный выбор (один вопрос, список возможных ответов,
2. выбор правильных ответов из списков (для каждого вопроса свой список
возможных ответов, в каждом списке для каждого вопроса только один
правильный ответ);
3. заполнение пропусков в тексте или схеме (используются в основном в
случае, если ответы формулируются в виде чисел);
4. составление последовательности (расположение объектов в порядке
роста или убывания значения некоторого свойства);
5. установление соответствия между элементами двух множеств (часто
количества элементов во множествах не совпадают – в этом случае
сложность задания возрастает);
6. выбор области (следует отметить на рисунке или в таблице объекты,
соответствующие некоторому условию, например указать в Периодической
системе клетки с элементами, обладающими какими-либо свойствами);
7. перетаскивание объектов (например, заполнение соответствующих ячеек
таблицы)
Слайд 4Основные цели создания тестов:
1. закрепление сформированных на предыдущем этапе (при работе
пособием) знаний и умений, перевод некоторых действий в умственный
план. Формирование умения мысленно представлять электронно-
графическую формулу внешнего энергетического уровня атома любого s-,
p- или d-элемента в основном, возбужденном и гибридизированном
состоянии для того, чтобы впоследствии не только эффективно выполнять
соответствующие задания ЕГЭ, но и быстро определять возможные
значения валентностей и степеней окисления;
2. минимизирование участия преподавателя в организации обратной связи.
При использовании компьютерной версии тестов учитель вообще не
участвует в контроле и оценке; при использовании бумажной версии из-за
стандартизированной формы заданий деятельность по контролю и оценке
формализована и не требует значительных ресурсов.
Слайд 5Тест 1
Состав ядра атома. Изотопы.
1. Выберите правильные ответы из предложенных вариантов.
ядра, протонов, нуклонов, элементарных частиц) с положительным зарядом и
__________ (нуклонов, протонов, электронов и протонов, электронной
оболочки, ядра, элементарных частиц) с отрицательным зарядом.
2. Заряд атома равен _______ (числу протонов, заряду ядра, нулю, заряду
электронной оболочки, массовому числу, массе атома).
3. Число протонов в ядре атома равно ________ (порядковому номеру элемента в
ПС, номеру периода, массовому числу ядра атома) и равно ______ (числу
нуклонов в ядре, числу электронов в оболочке, числу нейтронов в ядре, номеру
группы в ПС) и обозначается буквой ________ (р, Р, N, Z, n, A, Э).
4. Массовое число (ядра) атома – это сумма числа ________ (нуклонов, протонов,
электронов, нуклидов, элементарных частиц) и числа ________(электронов,
нейронов, изотопов, нейтронов, радионуклидов) в ядре атома, обозначается
буквой _________ (М, Э, N, A, Z, a, Я).
Слайд 6
2. Выберите правильные ответы.
одинаковое число протонов
одинаковый заряд ядра
одинаковое массовое число
разная масса атома
разное число электронов
одинаковое число нейтронов
одинаковая масса атома
разное число нейтронов
одинаковая сумма числа протонов и электронов
3. Выберите правильные ответы.
Если два атома изотопны друг другу, значит, у них:
а) число протонов _______(одинаковое/различное);
б) заряд ядра ___________ (одинаковый/ различный);
в) число нейтронов ______(одинаковое/ различное);
г) массовое число _______ (одинаковое/ различное);
д) заряд атома __________ (одинаковый/ различный);
е) число электронов______(одинаковое/ различное);
ж) масса атома __________(одинаковая/ различная);
з) заряд электронной оболочки _________(одинаковый/ различный);
и) число нуклонов в ядре _____________ (одинаковое/различное);
Слайд 7
4. Расположите зашифрованные частицы в
22Y0 31X+ 74Dn+1 73Z+
5. Расположите зашифрованные частицы в порядке роста массы.
31Б 2Д2 4В2+ 116А4- 146Е4+ 147Ж2 16Г2-
6. Выберите правильные ответы. 7. Выберите правильные ответы.
Число нейтронов одинаково у следующих У атомов XС и X+1N:
пар частиц: . одинаковое число протонов
16О, 15N . одинаковое число нейтронов
14N, 14C . разный заряд ядра
12C, 10B . одинаковая масса атома
11B, 12C . разное массовое число атома
19F, 18O . одинаковое число электронов
16O, 14N . разное число нейтронов
13C, 14N . одинаковый заряд
13C, 10B
Слайд 8
8. Установите соответствие.
Сопоставьте обозначения
Обозначения частиц: а) 44Sc
б) 37Сl
в) 44Тi
г) 40К
д) 40Са
е) 40Аr
Описание частиц: 1) 19 электронов в электронной оболочке атома;
2) 22 протона в ядре;
3) заряд ядра + 20;
4) 17 электронов в электронной оболочке;
5) 22 нейтрона в ядре;
6) заряд электронной оболочки -21;
7) суммарное число протонов, нейтронов и электронов 24.
Слайд 9 Тест 2 Строение электронной оболочки атома. Число уровней и число электронов на
1. Выберите правильные ответы из предложенных вариантов.
1. Общее число электронов в оболочке равно ______ (порядковому номеру, номеру группы,
номеру периода).
2. Число уровней в электронной оболочке атома равно________(номеру группы, атомному
номеру, порядковому номеру, номеру периода).
3. Число электронов на внешнем уровне для элементов главных подгрупп (А-групп) равно
_____(номеру периода, атомному номеру, от 1 до 7, номеру группы, массовому числу), а для
элементов побочных подгрупп (В-групп) равно ______(номеру группы, числу протонов,
от 0 до 2, от 1 до 2, от 1 до 8, больше 0).
2. Расположите названия элементов в порядке роста числа уровней в электронной
оболочке: цинк, гелий, уран, магний, лантан, углерод.
3. Отметьте в Периодической системе элементы, в атомах которых на внешнем
уровне 1 электрон.
Слайд 10 4. Выберите правильные ответы.
Отметьте строчки с
2 электрона: Fe, Co, Ni Ag, Au, Pt Ca, Sr, Ba Be, V , W
Cu, Sr, Ra Au, C, Tc Pb, Cd, Zn Co, Sr, S
Zn, Be, Sn Si, C,O He, Hg, Sc
Sc, Ti, Ca Cr, Ba, Fe Mg, Ca, Ge
5. Выберите правильные ответы.
Укажите строчки с символами элементов, атомы которых содержат на внешнем уровне
одинаковое число электронов.
F, Br, Cl K, Li, Rb Cr, Mo, W Co, Ni, Ba C, Si, Ge
P, As, N K, Cu, Au Te, S, O Al, Ga, B Cu, Ag, Cr
6. Выберите правильные ответы.
Одинаковое число электронов на внешнем уровне имеют атомы:
галогенов (F, Cl, Br, I, At) элементов II группы
халькогенов (O, S, Se, Te, Po) элементов III группы
благородных газов (He, Ne, Ar, Kr. Xe, Rn) неметаллов IV группы
щелочных металлов (Li, Na, K, Rb, Cs, Fr) металлов VII группы четных периодов
щелочно-земельных металлов (Ca, Sr, Ba, Ra) металлов VI группы
благородных металлов (Ag, Au, Ru, Rh, Pd, Os, Ir, Pt) элементов VIII-B группы
элементов VI –го периода металлов VIII-A группы четных периодов
элементов I группы
Слайд 11 7. Расположите элементы в порядке роста числа электронов на внешнем уровне:
Тест 3
Схема электронного строения атома
1. Выберите правильные ответы из предложенных вариантов.
1. Заряд ядра атома равен ______ (порядковому номеру, номеру периода, номеру группы,
массовому числу).
2. Общее число электронов в атоме равно ________(порядковому номеру, числу нейтронов,
массовому числу, номеру группы).
3. Число электронов на внешнем уровне для элементов главных подгрупп (А-групп) равно ____
(номеру периода, номеру группы, порядковому номеру, атомному номеру, от 0 до 8), а для
элементов побочных подгрупп (В-групп) равно _____ (2, номеру периода, номеру группы,
порядковому номеру, атомному номеру, от 0 до 8, от 0 до 2).
Слайд 12 4. Максимально возможное число электронов на уровне можно рассчитать по
(n2, 2n, (2n)2, 2n2, 8n, 2(n-8)2), где n - ______(номер уровня, номер периода, номер подуровня,
орбитальное квантовое число, спин электрона, порядковый номер, любое натуральное число).
2. Установите соответствие.
Сопоставьте символы элементов и число уровней в электронной оболочке их атомов.
Символы элементов Число уровней в электронной оболочке
А) Be 1) 1 уровень 6) 6 уровней
Б) Al 2) 2 уровня 7) 7 уровней
В) As 3) 3 уровня
Г) I 4) 4 уровня
Д) Au 5) 5 уровней
3. Установите соответствие.
Сопоставьте строки:
А) Максимальное число электронов на 1-ом уровне 1) 1
Б) Число элементов, в атомах которых на внешнем уровне 0 е- 2) 2
В) Число элементов, в атомах которых на внешнем уровне 8 е- 3) 3
Г) Максимальное число электронов на 2-м уровне 4) 5
Д) Число элементов, в электронной оболочке атомов которых 4 уровня 5) 6
Е) Число неметаллов, в атомах которых на внешнем уровне 5 е- 6) 8
7) 18
Слайд 13 4. Заполните пропуски:
Составьте схемы электронного строения атомов (укажите число
5В ____ е- ____ е- ; 47Ag _____ e- ____ e-____ e- ____ e- ____ e-;
15Р ____ е- _____ е- _____е- ; 53I _____ e- ____ e- ____ e- ____ e- ____ e- ;
20Са ____ е- ____ е- _____ е- ____е- ; 42Mo ____ e- ____ e- ____ e- ____ e- ____ e- ;
16S _____e- ____ e- ____ e- ; 51Sb ____ e- ____ e- ____ e- ____ e- ____ e- ;
30Zn ____ e- ____ e- _____ e- ____ e- ; 18Ar ____ e- ____ e- ____ e- ;
8O _____ e- ____ e- ;
5. Установите соответствие:
Сопоставьте символы элементов и схемы их электронного строения.
Символы элементов Схемы электронного строения
А) 19F 1) ?е- 5е-
Б) 35Cl 2) ?е- 2е-
В) 14N 3) 2е- 7е-
Г) 9Be 4) ?е- ?е- 7 е-
Д) 24Mg 5) 2е- ?е- 5е-
Е) 31P 6) 2е- ?е- 2е-
7) 2е- ?е- 4е-
Слайд 14 6. Установите соответствие.
Сопоставьте символы
Символы элементов Схемы электронного строения
А) He 1) ?е- ?е- ?е- 4е-
Б) Cd 2) ?е- ?е- 4е-
В) Mg 3) 2е- ?е-
Г) Ge 4) ?е- ?е- ?е- 2е-
Д) C 5) ?е-
Е) Be 6) ?е- ?е- 2е-
Ж) Ca 7) ?е- 4е-
З) Si 8) ?е- ?е- ?е- ?е- ?е-
7. Установите соответствие.
Сопоставьте символы элементов и фрагменты схем их электронного строения.
Символы элементов Схемы электронного строения
А) 29Сu 1) … 8е- 1е-
Б) 24Cr 2) … 18е- 1е-
В) 17Cl 3) … 18е- 7е-
Г) 19K 4) … 13е- 2е-
Д) 12Mg 5) … 13е- 1е-
Е) 35Br 6) … 8е- 7е-
Ж) 43Tc 7) … 8е- 2е- 8) … 18е- 2е-
Слайд 15
Тест 4
Ионы.
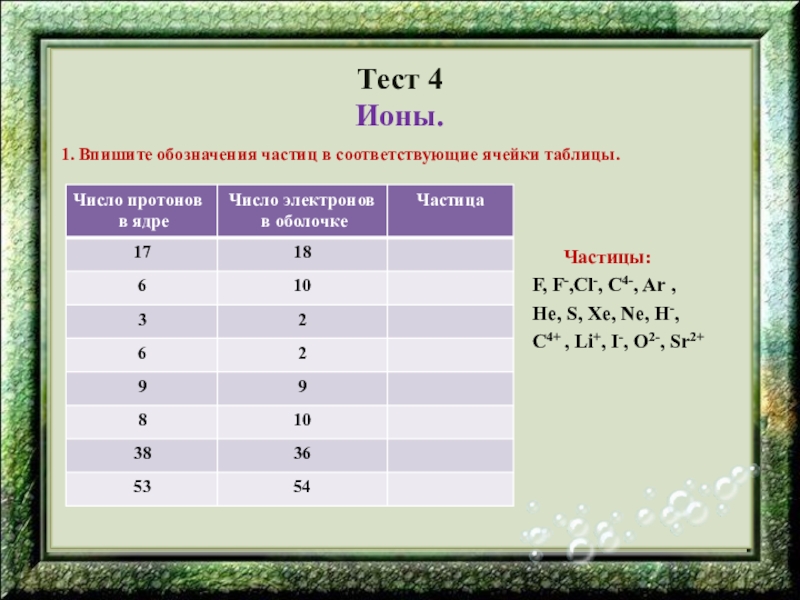
1. Впишите обозначения частиц в соответствующие ячейки таблицы.
Частицы:
F, F-,Cl-, C4-, Ar ,
He, S, Xe, Ne, H-,
C4+ , Li+, I-, O2-, Sr2+
Слайд 16
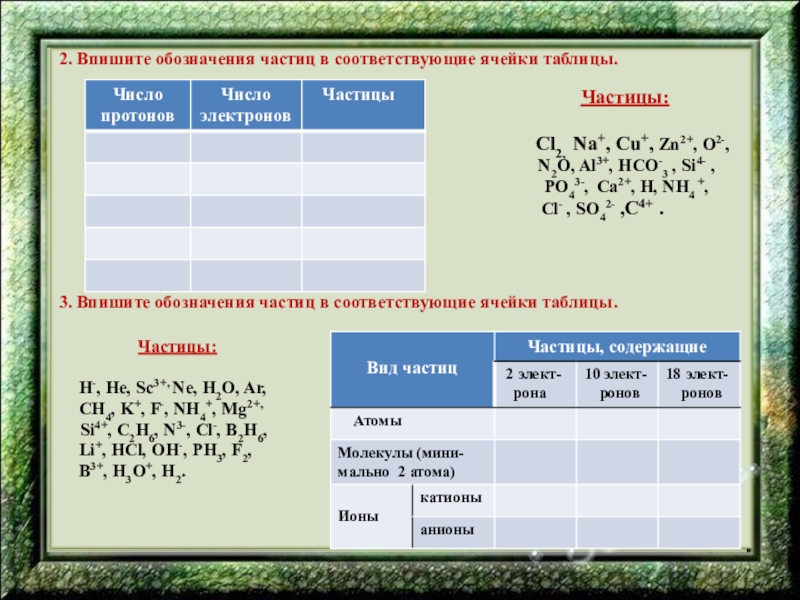
2. Впишите обозначения частиц в соответствующие
Частицы:
Cl2, Na+, Cu+, Zn2+, O2-,
N2O, Al3+, HCO-3 , Si4- ,
PO43-, Ca2+, H, NH4 +,
Cl- , SO42- ,C4+ .
3. Впишите обозначения частиц в соответствующие ячейки таблицы.
Частицы:
H-, He, Sc3+, Ne, H2O, Ar,
CH4, K+, F-, NH4+, Mg2+,
Si4+, C2H6, N3-, Cl-, B2H6,
Li+, HCl, OH-, PH3, F2,
B3+, H3O+, H2.
Слайд 17 5. Выберите правильные ответы из предложенных вариантов.
фтора, хлора, инертных газов). Только принимают электроны атомы ____ (металлов,
неметаллов, фтора, хлора, инертных газов). И отдают, и принимают электроны
атомы ______ (металлов, неметаллов, фтора, инертных газов), за исключением
атомов _____ (галогенов, халькогенов, инертных газов) и _____(фтора, хлора, брома).
2. Катионы образуются при отдаче всех или части валентных электронов атомами
_______ (металлов и неметаллов, галогенов, инертных газов) (исключения см. выше).
Анионы образуются при присоединении электронов к атомам _______ (металлов,
неметаллов, фтора, хлора, инертных газов) чаще всего до устойчивой конфигурации
_______ (ns2, np5, 2n2, 2n22p3, ns2np6).
6. Отметьте на фрагменте Периодической системы (см.ниже) клетки с символами
элементов, атомы которых могут образовать:
а) только анионы; б) как катионы, так и анионы; в) ионы только с зарядом 2+;
г) ионы как с зарядом 4+, так и с зарядом 4-;
д) ионы как с зарядом 1-, так и с зарядом 7+.