- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Интеллектуально – творческая игра по неорганической химии
Содержание
- 1. Интеллектуально – творческая игра по неорганической химии
- 2. Первый раунд
- 3. Этот химический элемент поддерживает работу сердечной мышцы,
- 4. Роль этого химического элемента в жизнедеятельности
- 5. Соединения этого элемента регулируют процессы возбуждения
- 6. Этот жизненно важный химический элемент
- 7. Этот элемент академик А.Е.Ферсман назвал «элементом жизни и мысли»ответ
- 8. Что в переводе с греческого означает слово «галогены»?ответ
- 9. Без 0,2% - ного соединения этого галогена практически прекращается процесс переваривания пищи.ответ
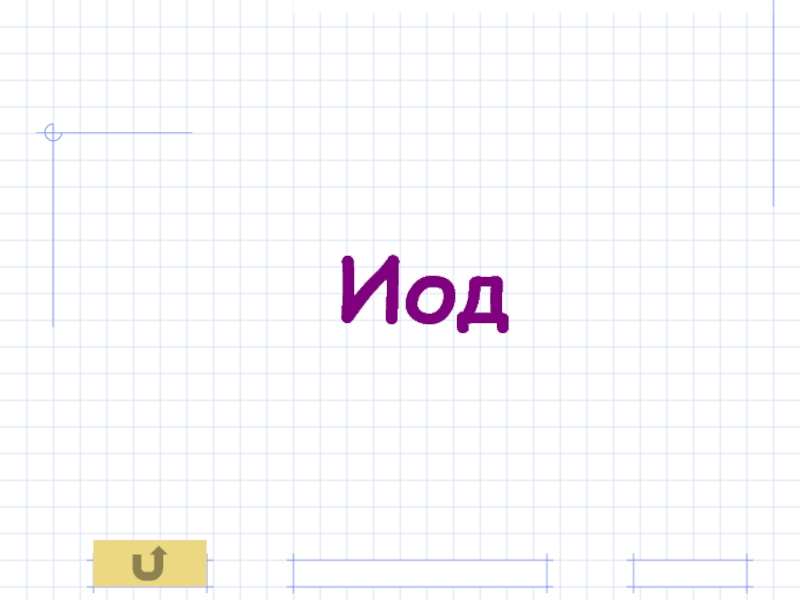
- 10. Недостаток этого галогена в
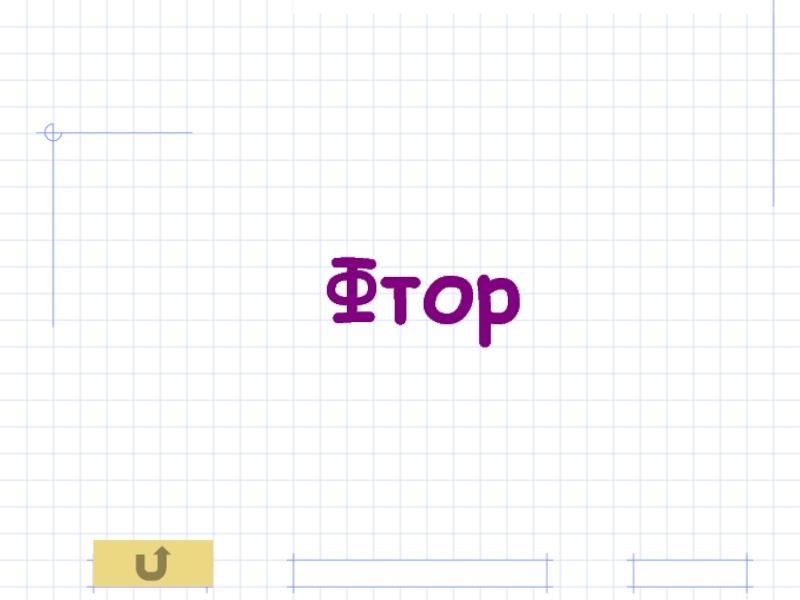
- 11. Тефлон (покрытие сковородок) - пластмасса, содержащая этот галоген. ответ
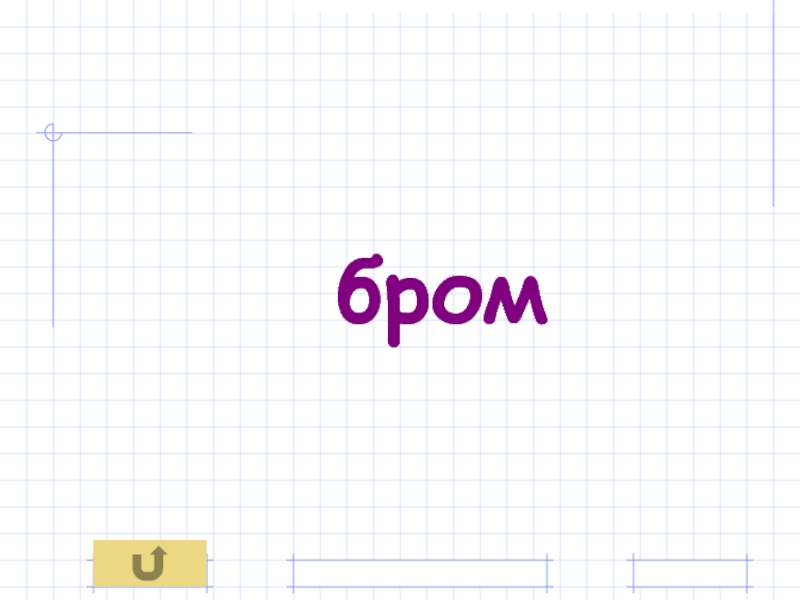
- 12. При обычных условиях этот галоген представляет собой жидкость красно-бурого цвета.ответ
- 13. Сплав этого металла и меди (бронза) изготовлялся еще в 3-м тысячелетии до н.э..ответ
- 14. Название этого металла произошло
- 15. На некоторых древних языках этот металл именуется «небесным камнем».ответ
- 16. В 1854 г. стоимость
- 17. Из соли этого металла
- 18. Алхимики писали: «Крепкая водка пожирает луну.
- 19. Твердое, очень тугоплавкое вещество.
- 20. Тугоплавкое вещество, при смешивании
- 21. Бесцветный газ с
- 22. Этот оксид окрашивает стекло в зеленый цвет. ответ
- 23. Этот гениальный химик XIX в. родился
- 24. Итальянский ученый.В 1811 г. открыл закон о газах, позже названный его именемответ
- 25. Выдающийся английский физик и химик, основоположник
- 26. Великий русский ученый-энциклопедист, первый русский академик.
- 27. Русский химик-органик, академик АН СССР
- 28. Реакция, в результате которой из двух
- 29. Самопроизвольное разрушение металлов и сплавов под влиянием окружающей средыответ
- 30. Реакция, в результате которой из одного
- 31. Реакция, в результате которой происходит ряд последовательных превращений.ответ
- 32. Реакция, протекающая между простыми и сложными
- 33. калий
- 34. железо
- 35. бром
- 36. Сера
- 37. Фосфор
- 38. Солероды
- 39. Соединение хлора –соляная кислота
- 40. Иод
- 41. Фтор
- 42. Бром
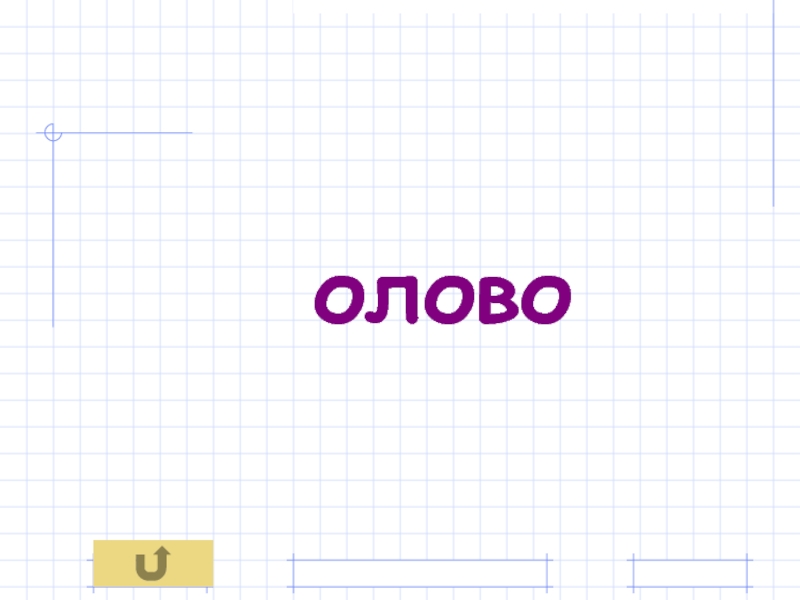
- 43. олово
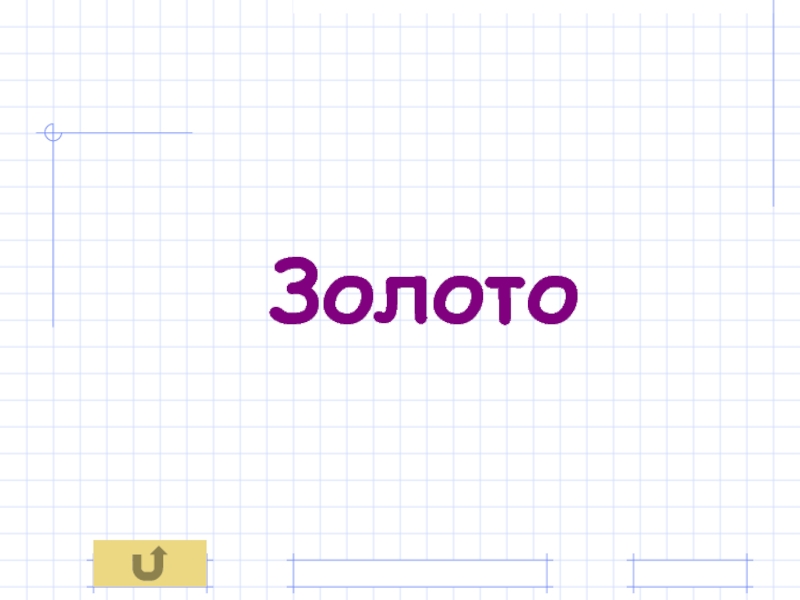
- 44. Золото
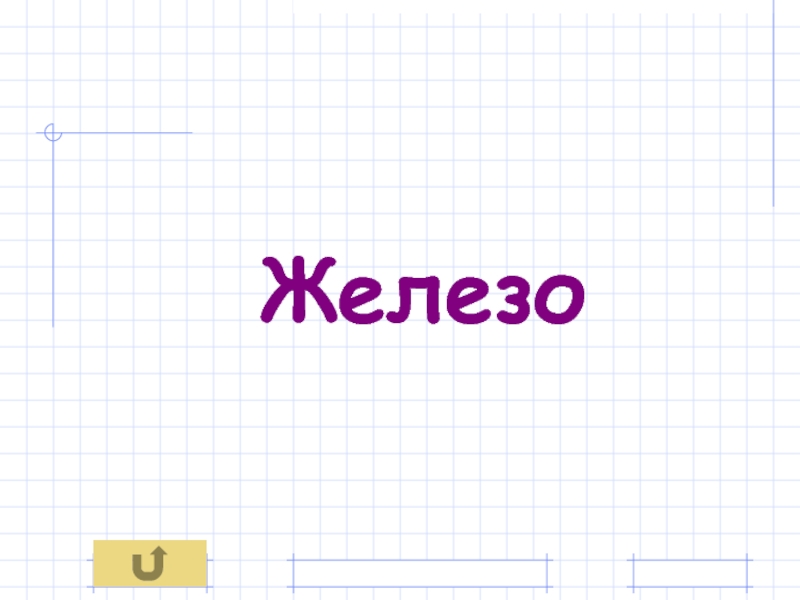
- 45. Железо
- 46. Алюминий
- 47. соли кальция – карбонаты (мрамор)
- 48. Оксид азота (IV) – бурый газ
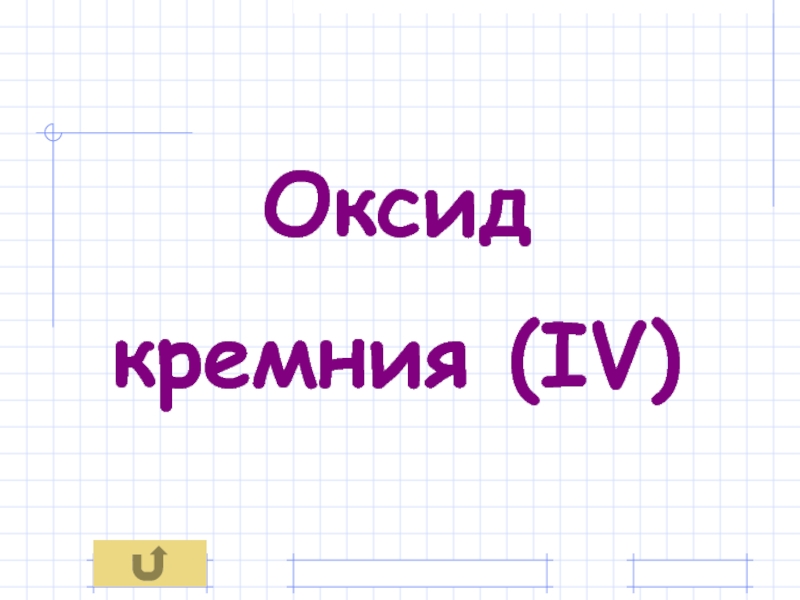
- 49. Оксид кремния (IV)
- 50. Оксид кальция
- 51. Оксид серы (IV)
- 52. Оксид хрома (III)
- 53. Д.И.Менделеев
- 54. Авогадро
- 55. Дальтон
- 56. М.В.Ломоносов
- 57. Николай Дмитриевич Зелинский
- 58. Реакция соединения
- 59. коррозия
- 60. Реакция разложения
- 61. Цепная реакция
- 62. Реакция замещения
- 63. Второй раунд
- 64. Первенство открытия этого химического элемента принадлежит
- 65. Этот химический элемент был обнаружен
- 66. Этот английский физик в 1911
- 67. Впервые этот элемент был открыт английским
- 68. В поисках «философского камня» гамбургский
- 69. Бесцветный газ с характерным запахом тухлых яиц.
- 70. Бесцветный газ, тяжелее воздуха, при сильном
- 71. Газ без цвета, запаха и вкуса,
- 72. Бесцветный газ, от которого перехватывает дыхание, раствор этого газа окрашивает фенолфталеин в малиновый цвет.
- 73. Этот газ впервые был применен в
- 74. В концентрированном виде имеет красно-бурый цвет
- 75. Бесцветная маслянистая жидкость, очень гигроскопична. Представляет
- 76. Смесь концентрированных азотной и соляной кислот
- 77. Очень слабая кислота, нерастворима в воде.
- 78. Бесцветная жидкость с запахом горького миндаля.
- 79. Эта соль применяется в производстве соды,
- 80. Эту соль калия применяют в стекольном
- 81. Соль кальция, применяется как наполнитель для
- 82. Эту соль бария «съедают» для проведения рентгенодиагностики для диагностики заболеваний ЖКТ .
- 83. Эти соли называют растворимым стеклом.
- 84. Этот неметалл издавна употребляли для
- 85. Второй элемент после кислорода по
- 86. Название этого неметалла в переводе с латинского означает «безжизненный».
- 87. С помощью этого неметалла
- 88. Этот газ нашел применение в
- 89. Заряженные частицы, в которые превращаются
- 90. Вид химической связи, образованной одинаковыми атомами элементов неметаллов .
- 91. Разновидности атомов одного и того
- 92. Свойство атомов данного элемента оттягивать на себя электроны других атомов элементов, входящих в соединение.
- 93. Процесс присоединения электронов.
Слайд 1
Турнир химиков-неоргаников
МБОУ «СОШ №2» г.Югорск
учитель химии : Воронцова
Елена
Слайд 3Этот химический элемент поддерживает работу сердечной мышцы, поэтому нехватка его в
Больше всего этого элемента содержится в кураге и изюме.
ответ
Слайд 4 Роль этого химического элемента в жизнедеятельности организмов очень велика.
Элемент входит
ответ
Слайд 5 Соединения этого элемента регулируют процессы возбуждения и торможения центральной нервной
ответ
Слайд 6 Этот жизненно важный химический элемент входит в состав белков.
Является составной частью витаминов и гормонов.
ответ
Слайд 9 Без 0,2% - ного соединения
этого галогена
практически прекращается
переваривания пищи.
ответ
Слайд 10 Недостаток этого галогена в в воде и пище
снижает выработку гормона щитовидной железы
и приводит к заболеванию эндемическим зобом.
ответ
Слайд 14 Название этого металла произошло от латинского словосочетания
«утренняя
Из металла можно
изготовить фольгу толщиной всего 0,003 мм.
ответ
Слайд 16 В 1854 г.
стоимость 1 кг этого металла
то есть в 270 раз дороже серебра,
а в 1899 г. – 1 рубль.
ответ
Слайд 17 Из соли этого металла
созданы стены всемирно известного
из него же облицованы многие станции московского метро
ответ
Слайд 18 Алхимики писали: «Крепкая водка пожирает луну. Выпуская лисий хвост…»
Крепкая
Пожирает – растворяет
Лисий хвост – это ……
ответ
Слайд 19 Твердое, очень тугоплавкое вещество. В природе встречается в
ответ
Слайд 20 Тугоплавкое вещество,
при смешивании с водой
оно соединяется
что вода закипает.
Куски этого оксида, впитывая воду, разбухают и рассыпаются, превращаясь в гашеную известь.
ответ
Слайд 21 Бесцветный газ с характерным резким запахом горелых
Так, у красной розы, опущенной в этот газ, окраска пропадает, и она становится белой.
Этот газ убивает микроорганизмы. Применяется для беления соломы, шелка, шерсти
ответ
Слайд 23 Этот гениальный химик XIX в.
родился в Тобольске.
В его
в 1887 г. один на аэростате он поднялся выше облаков наблюдать солнечное затмение, а приземлился в другой губернии.
Суеверные люди подумали, что это снизошел на землю всевышний.
ответ
Слайд 25 Выдающийся английский
физик и химик,
основоположник атомных представлений в химии.
Впервые ввел понятие «атомный вес» и составил таблицу относительных атомных и молекулярных масс, приняв атомную массу водорода за единицу.
ответ
Слайд 26 Великий русский ученый-энциклопедист, первый русский академик.
Одно из его достижений
общая формулировка
закона сохранения массы веществ и движения
ответ
Слайд 27 Русский химик-органик, академик АН СССР (с 1929) совместно с
создал
противогаз (1915), используя свойства
активированного угля
ответ
Слайд 28 Реакция, в результате которой из двух или нескольких простых или
ответ
Слайд 30 Реакция,
в результате которой
из одного сложного вещества получаются
два
простых или сложных веществ.
ответ
Слайд 32 Реакция,
протекающая между простыми и сложными веществами,
при которой
атомы
атомы одного из элементов
в сложном веществе.
ответ
Слайд 64
Первенство открытия этого химического элемента принадлежит китайскому ученому VIII в.
Слайд 65
Этот химический элемент был обнаружен
немецким ученым Парацельсом в
когда он погружал железо в серную кислоту.
Слайд 66
Этот английский физик в 1911 г.
Слайд 67
Впервые этот элемент был открыт английским ученым Д.Резерфордом в 1772
Слайд 68
В поисках «философского камня» гамбургский алхимик Х.Брандт в
Слайд 69Бесцветный газ с характерным запахом тухлых яиц. Постоянный спутник всего живого,
Слайд 70 Бесцветный газ, тяжелее воздуха, при сильном охлаждении превращается в твердую
Слайд 71 Газ без цвета, запаха и вкуса, продукт неполного окисления углеродного