- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химия 8 класс Кислород
Содержание
- 1. Химия 8 класс Кислород
- 2. 1. Элемент кислород находится в VI группе,
- 3. 4. В земной коре его 49% по
- 4. Газ - без цвета, вкуса и
- 5. С неметалламиC + O2 → CO2S +
- 6. Промышленный способ (перегонка жидкого воздуха).Лабораторный способ (разложение
- 7. перманганата калия при нагревании:2KMnO4 –t°→ K2MnO4 +
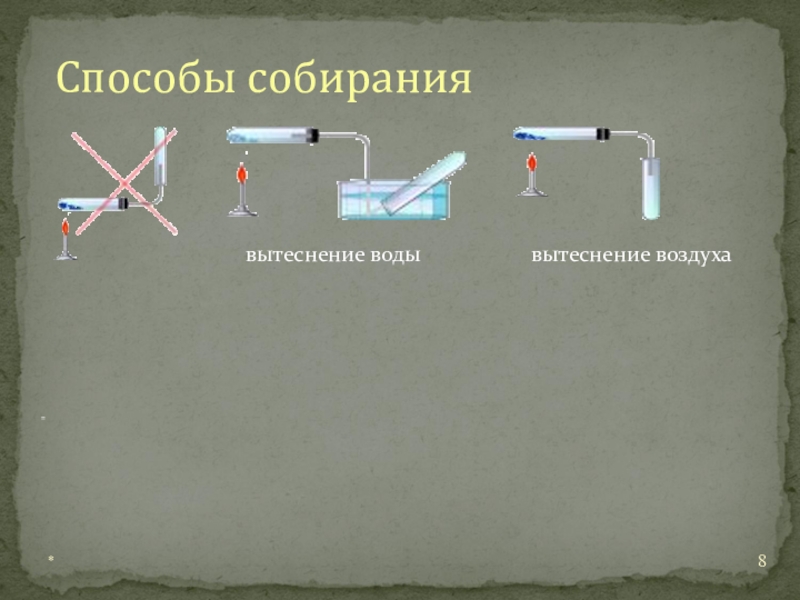
- 8. *Способы собирания
- 9. Находит широкое применение в медицине и промышленности.При
Слайд 21. Элемент кислород находится в VI группе, главной подгруппе, II периоде,
Ar = 16.
2. Строение атома:
P11 = 8; n01 = 8; ē = 8
валентность II, степень окисления -2
(редко +2; +1; -1).
3. Входит в состав оксидов, оснований, солей, кислот, органических веществ, в том числе живых организмов- до 65% по массе.
Кислород как элемент.
Слайд 34. В земной коре его 49% по массе, в гидросфере –
5. В составе воздуха (в виде простого вещества) – 20-21% по объёму.
Состав воздуха:
О2 – 20-21 %; N2 – 78%; CO2 – 0,03%,
остальное приходится на инертные газы, пары воды, примеси.
Кислород как элемент (продолжение).
Кислород является самым распространённым элементом нашей планеты. По весу на его долю приходится примерно половина общей массы всех элементов земной коры.
Слайд 4 Газ - без цвета, вкуса и запаха; в 100V H2O
t°кип= -183°С; t°пл = -219°C; d по воздуху = 1,1.
При давлении 760 мм. рт.ст. и температуре
–183 °С кислород сжижается
Физические свойства
Слайд 5С неметаллами
C + O2 → CO2
S + O2 → SO2
2H2 +
5
Химические свойства
Со сложными веществами
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2H2S + 3O2 → 2SO2 + 2H2O
CH4 + 2O2 → CO2 + 2H2O
С металлами
2Mg + O2 → 2MgO
2Cu + O2 –t°→ 2CuO
Взаимодействие веществ с кислородом называется окислением.
С кислородом реагируют все элементы, кроме Au, Pt, He, Ne и Ar, во всех реакциях (кроме взаимодействия со фтором) кислород - окислитель.
1. Неустойчив: O3 → O2 + O
2. Сильный окислитель: 2KI + O3 + H2O → 2KOH + I2 + O2
Обесцвечивает красящие вещества, отражает УФ - лучи, уничтожает микроорганизмы.
Слайд 6Промышленный способ (перегонка жидкого воздуха).
Лабораторный способ (разложение некоторых кислородосодержащих веществ)
2H2O2 –MnO2→ 2H2O + O2↑
Получение 3O2 → 2O3
Во время грозы (в природе), (в лаборатории) в озонаторе
*
6
Способы получения
Слайд 7перманганата калия при нагревании:
2KMnO4 –t°→ K2MnO4 + MnO2 + O2↑
Разложение этой
выше 2000 С.
Нагрев 2KMnO4 Проверка собравшегося
кислорода
*
Способы получения кислорода (продолжение).
Слайд 9Находит широкое применение в медицине и промышленности.
При высотных полётах лётчиков снабжают
При многих лёгочных и сердечных заболеваниях, а также при операциях дают вдыхать кислород из кислородных подушек.
Кислородом в баллонах снабжают подводные лодки.
Горение рыхлого горючего материала, пропитанного жидким кислородом, сопровождается взрывом, что даёт возможность применять кислород при взрывных работах.
Жидкий кислород применяют в реактивных двигателях, в автогенной сварке и резке металлов, даже под водой.
*
Применение кислорода: