- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химические связи в соединениях веществ.
Содержание
- 1. Химические связи в соединениях веществ.
- 2. Под химической связью понимают такое взаимодействие
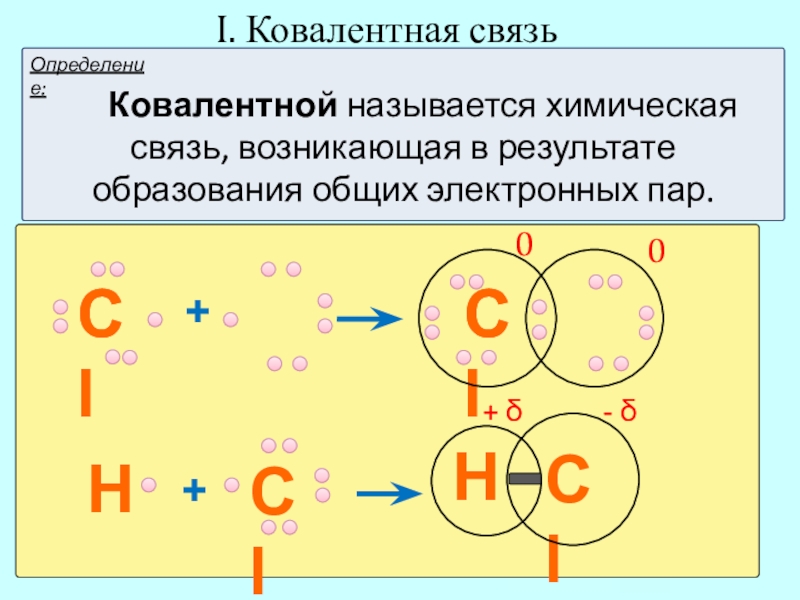
- 3. I. Ковалентная связьCl+ClClCl00
- 4. Полярность ковалентной связистепень смещения общих электронных пар
- 5. Ряд неметалловF, O, N, Cl, Br, S,
- 6. Ковалентная полярная связь. Ряд неметалловF, O, N,
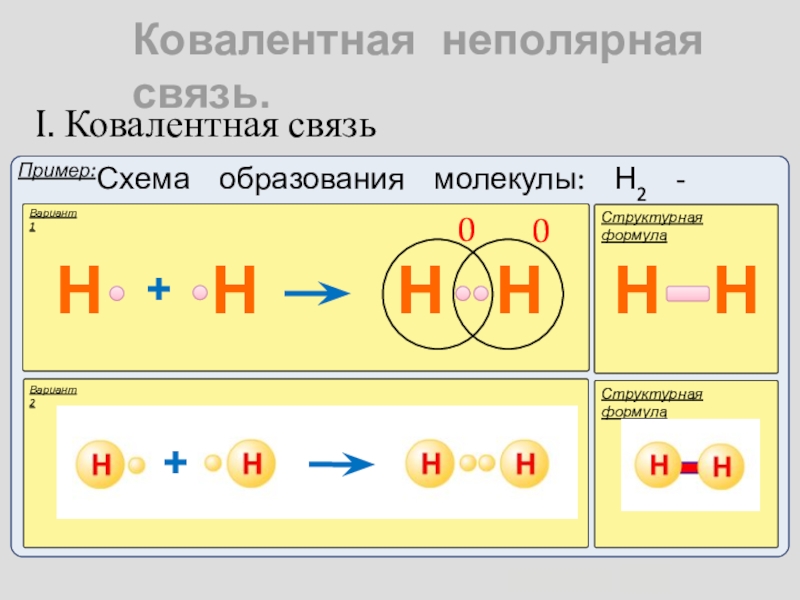
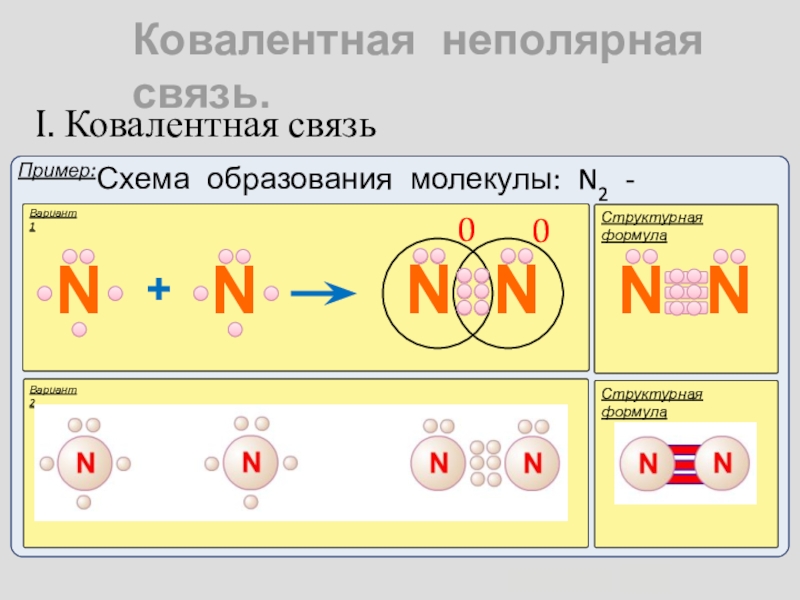
- 7. Ковалентная неполярная связь. I. Ковалентная связьВариант 1Структурная формулаНН
- 8. Ковалентная неполярная связь. I. Ковалентная связьВариант 1Структурная формула
- 9. I. Ионная связь
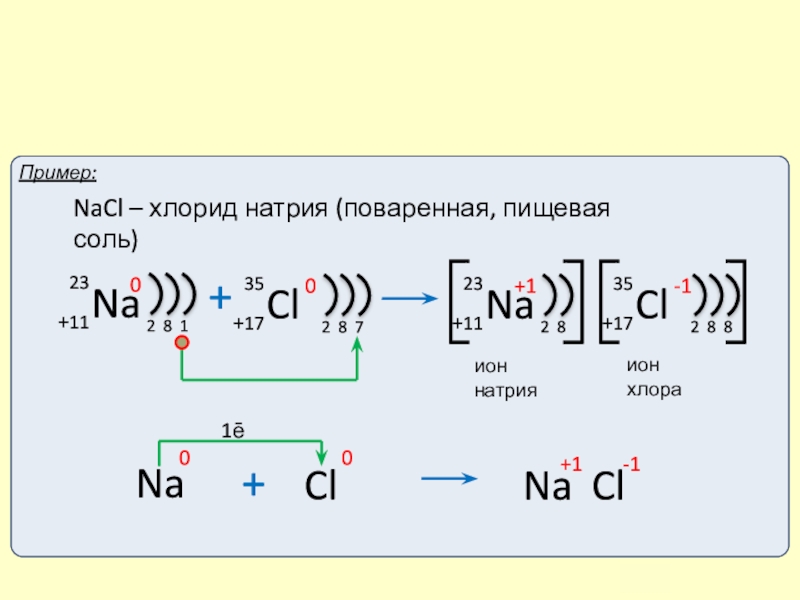
- 10. Ионы и ионная химическая связь. 1ē
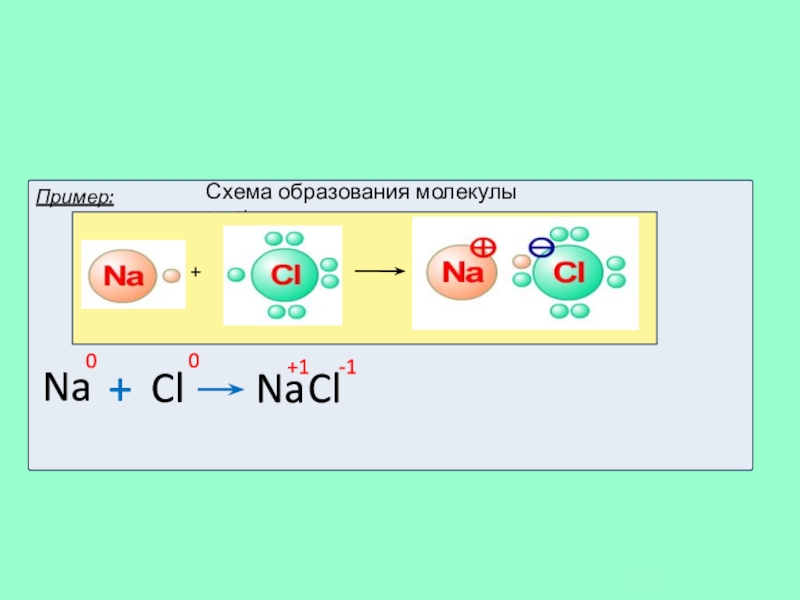
- 11. Ионы и ионная химическая связь. Схема образования молекулы NaCl
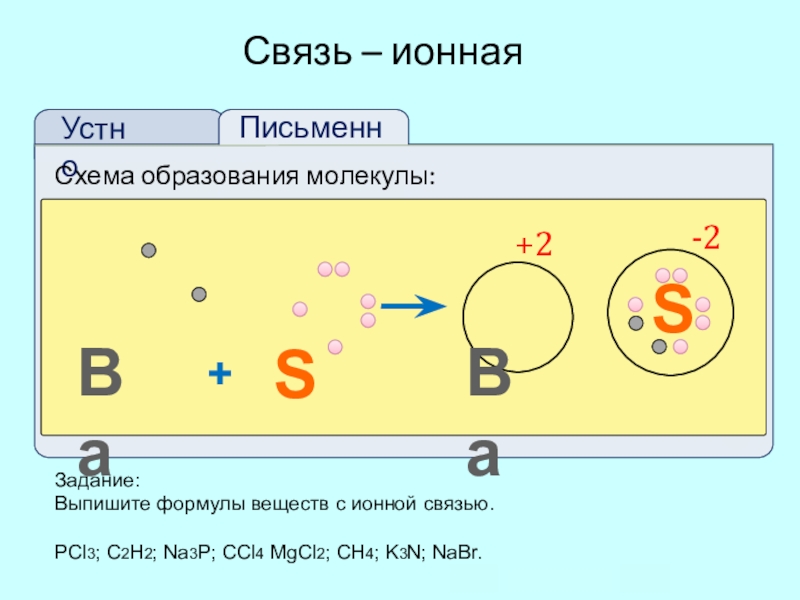
- 12. Схема образования молекулы: BaSBa+SСвязь – ионная Ba+2-2Задание:
- 13. Типы химических связей.
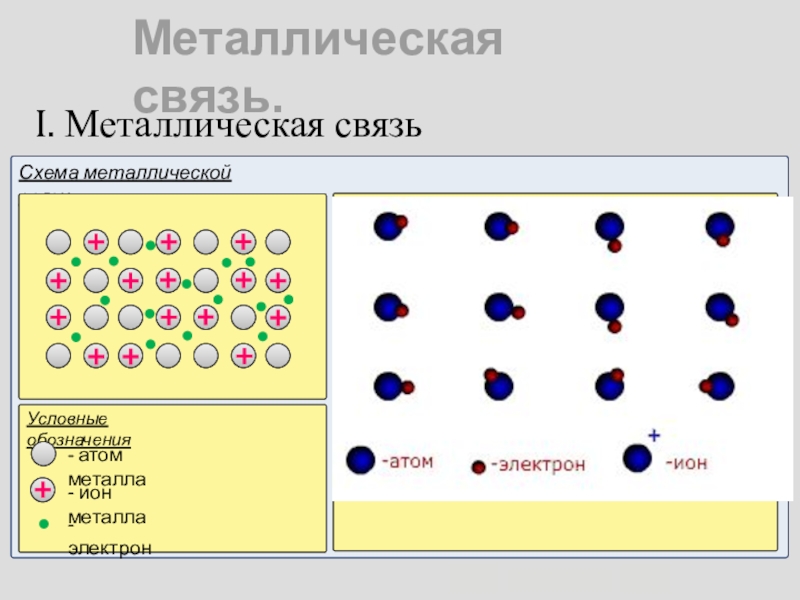
- 14. I. Металлическая связьСхема металлической связи: Металлическая связь. Условные обозначения- атом металла- ион металла- электрон
- 15. Металлическая связьсвязь в металлах и сплавах, которую
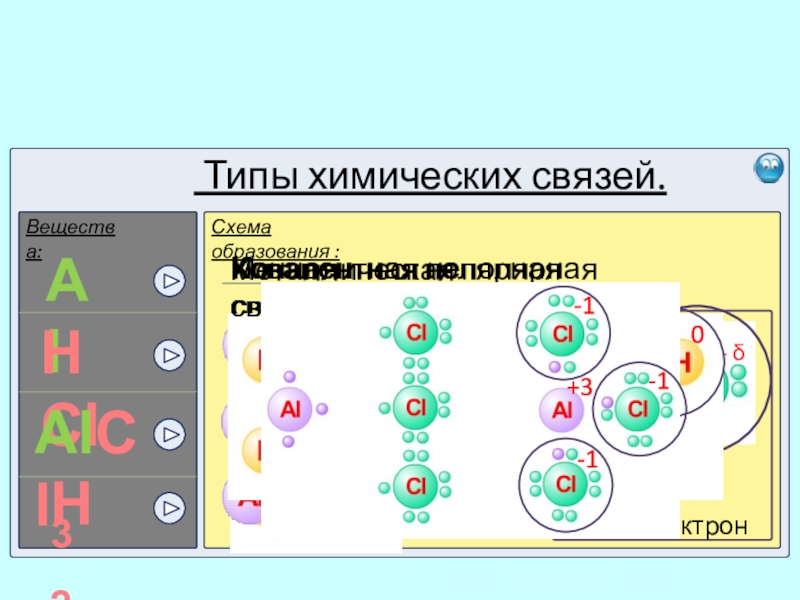
- 16. Типы химических связей.Вещества:Схема образования :AlHClAlCl3H2
- 17. Самостоятельная работаОпределите типы химических связей между атомами
- 18. Источники информации.Подборку материала и заданий составила: Судницына
Слайд 2Под химической связью понимают такое взаимодействие атомов, которое связывает их в
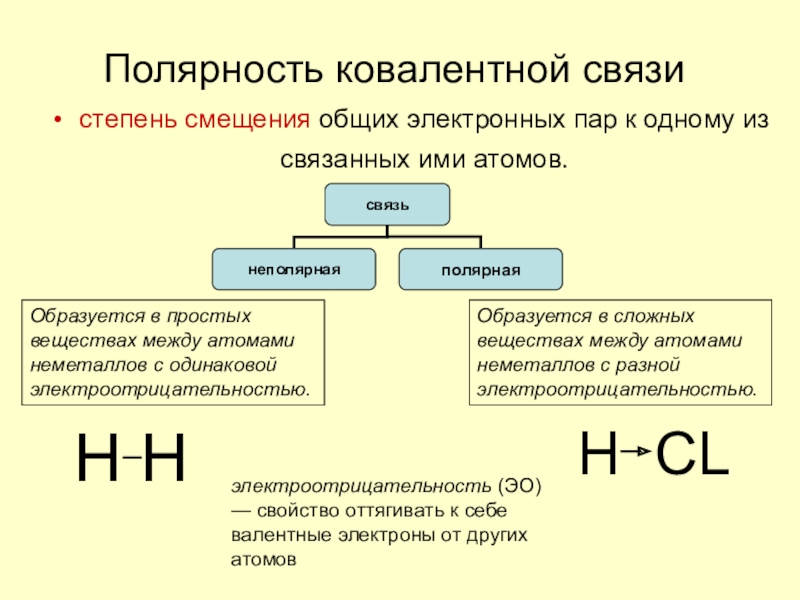
Слайд 4Полярность ковалентной связи
степень смещения общих электронных пар к одному из связанных
электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов
Образуется в простых веществах между атомами неметаллов с одинаковой электроотрицательностью.
Образуется в сложных
веществах между атомами неметаллов с разной электроотрицательностью.
H H
H СL
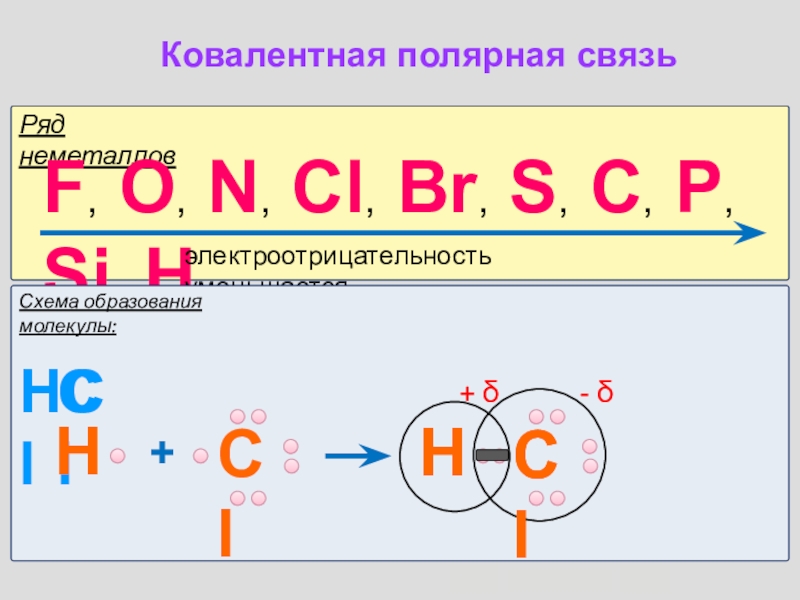
Слайд 5
Ряд неметаллов
F, O, N, Cl, Br, S, C, P, Si, H.
электроотрицательность
Схема образования молекулы:
HCl
H
Cl
Ковалентная полярная связь
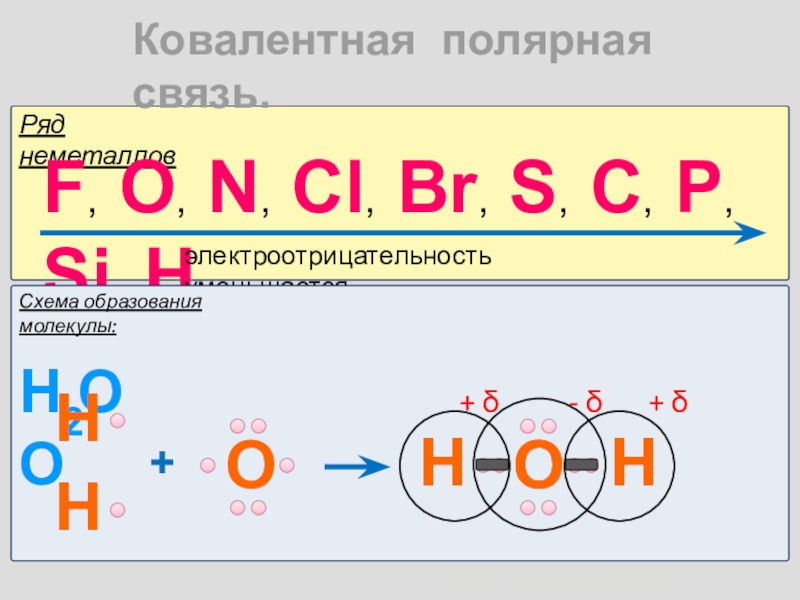
Слайд 6
Ковалентная полярная связь.
Ряд неметаллов
F, O, N, Cl, Br, S, C,
электроотрицательность уменьшается
Схема образования молекулы:
H2O
H
O
H
Слайд 12
Схема образования молекулы:
BaS
Ba
+
S
Связь – ионная
Ba
+2
-2
Задание:
Выпишите формулы веществ с
РСl3; С2Н2; Na3P; ССl4 MgCl2; СН4; K3N; NaBr.
Слайд 13
Типы химических связей.
Для каждого вещества химической
2Al + 6HCl ? 2AlCl3 + 3H2
Слайд 14
I. Металлическая связь
Схема металлической связи:
Металлическая связь.
Условные обозначения
- атом металла
-
- электрон
Слайд 15Металлическая связь
связь в металлах и сплавах, которую выполняют относительно свободные электроны
Задание:
Выпишите формулы веществ, в которых присутствует металлическая связь:
Na, KF, NH3, C2H2, CH3-COOH, H2S, AL, NaCL.
Слайд 17Самостоятельная работа
Определите типы химических связей между атомами в веществах.
CaВг2; НСl;
SO2; LiNО3; S2; C2H2; Na; HCОOК.
Слайд 18Источники информации.
Подборку материала и заданий составила: Судницына Г.В.
В презентации использовался материал
http://www.uchportal.ru/,
Учебник Рудзитиса Г.Е. и Фельдмана Ф.Г.