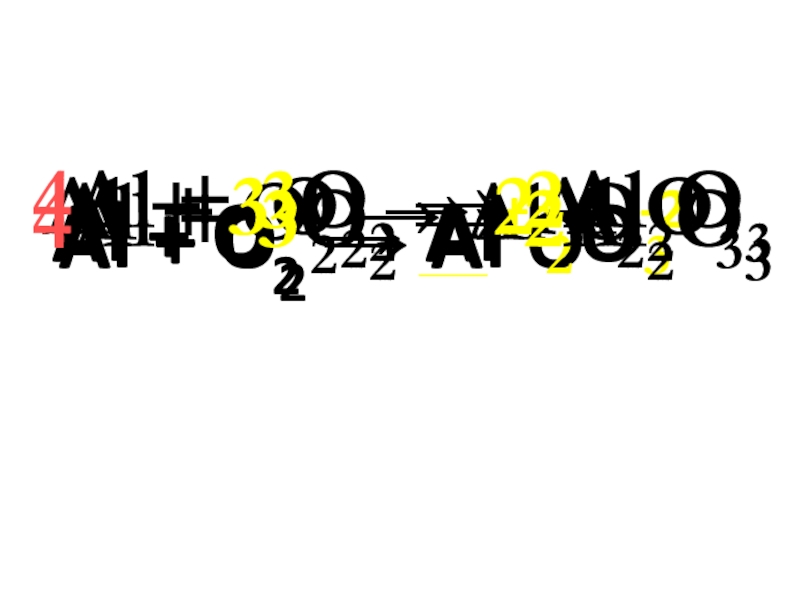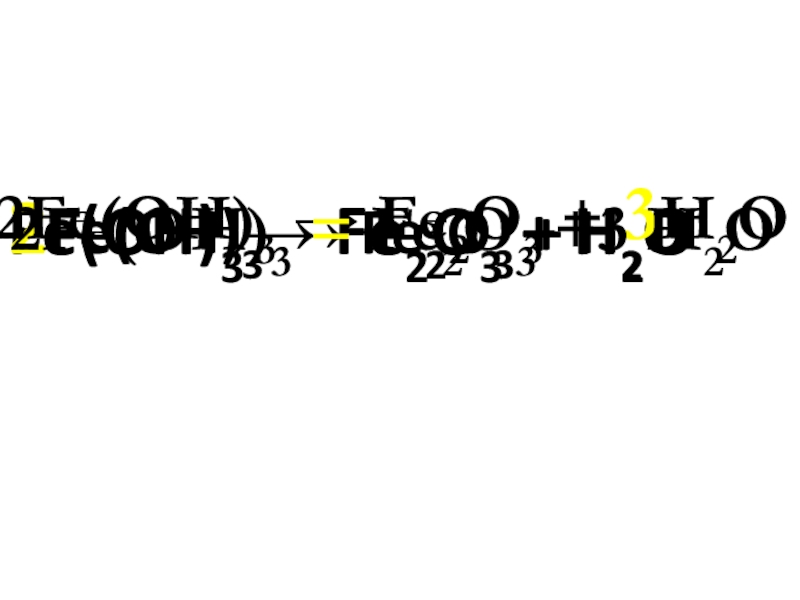- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химические реакции. Составление уравнений химических реакций
Содержание
- 1. Химические реакции. Составление уравнений химических реакций
- 2. Проблема Является ли закон сохранения массы веществ основой для составления уравнений химических реакций
- 3. Железо + сера → сульфид железа (II ) Fe + S → FeS
- 4. Al + O2 → Al OAl +
- 5. Слайд 5
- 6. Fe(OH)3→ Fe2O3 + H2O2Fe(OH)3 → Fe2O3 + H2O2Fe(OH)3 → Fe2O3 + 3H2O2Fe(OH)3 = Fe2O3 +3 H2O
- 7. Алгоритм расстановки коэффициентов в уравнениях химических реакций
- 8. Проблема Является ли закон сохранения массы веществ основой для составления уравнений химических реакций
- 9. Согласны ли вы,что:1.В реакции Ca + Cl2→
Слайд 2Проблема
Является ли закон сохранения массы веществ основой для составления уравнений
Слайд 4Al + O2 → Al O
Al + O2 → Al+3 O-2
Al
Al + 3O2 → 2Al2O3
4Al + 3O2 → 2Al2O3
4Al + 3O2 → 2Al2O3
Слайд 7Алгоритм расстановки коэффициентов в уравнениях химических реакций
Подсчитать количество атомов каждого элемента
Определить, у какого элемента количество атомов меняется, найти НОК.
Разделить НОК на индексы – получить коэффициенты. Поставить их перед формулами.
Пересчитать количество атомов, при необходимости действие повторить.
Последним проверить количество атомов кислорода.
Слайд 8Проблема
Является ли закон сохранения массы веществ основой для составления уравнений
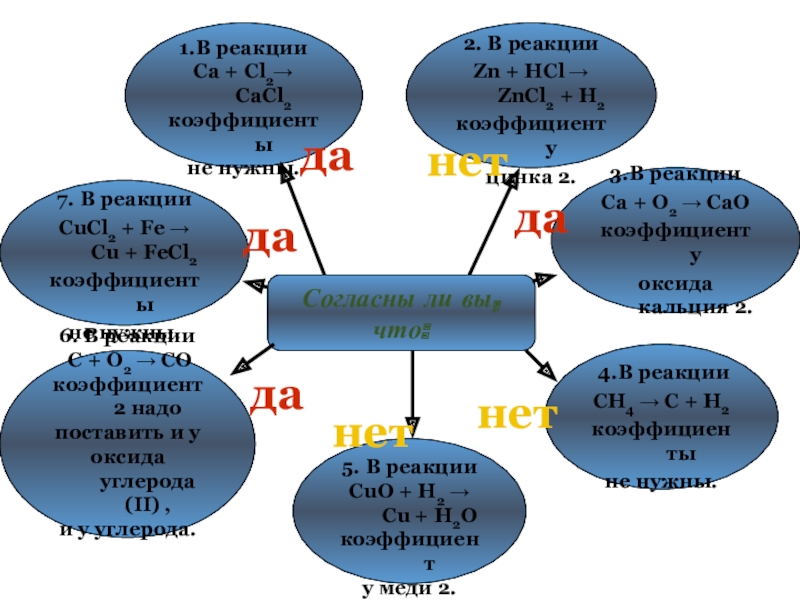
Слайд 9Согласны ли вы,
что:
1.В реакции
Ca + Cl2→ CaCl2
коэффициенты
не нужны.
2.
Zn + HCl → ZnCl2 + H2
коэффициент у
цинка 2.
3.В реакции
Ca + O2 → CaO
коэффициент у
оксида кальция 2.
4.В реакции
CH4 → C + H2
коэффициенты
не нужны.
5. В реакции
CuO + H2 → Cu + H2O
коэффициент
у меди 2.
6. В реакции
C + O2 → CO
коэффициент 2 надо
поставить и у
оксида углерода (II) ,
и у углерода.
7. В реакции
CuCl2 + Fe → Cu + FeCl2
коэффициенты
не нужны.
да
нет
нет
нет
да
да
да