- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему ЭЛЕКТРОЛИЗ ПРЕЗЕНТАЦИЯ (10 КЛАСС)
Содержание
- 1. ЭЛЕКТРОЛИЗ ПРЕЗЕНТАЦИЯ (10 КЛАСС)
- 2. А) білімділік: Оқушылардың тотығу дәрежесі және тотығу-тотықсыздану
- 3. Слайд 3
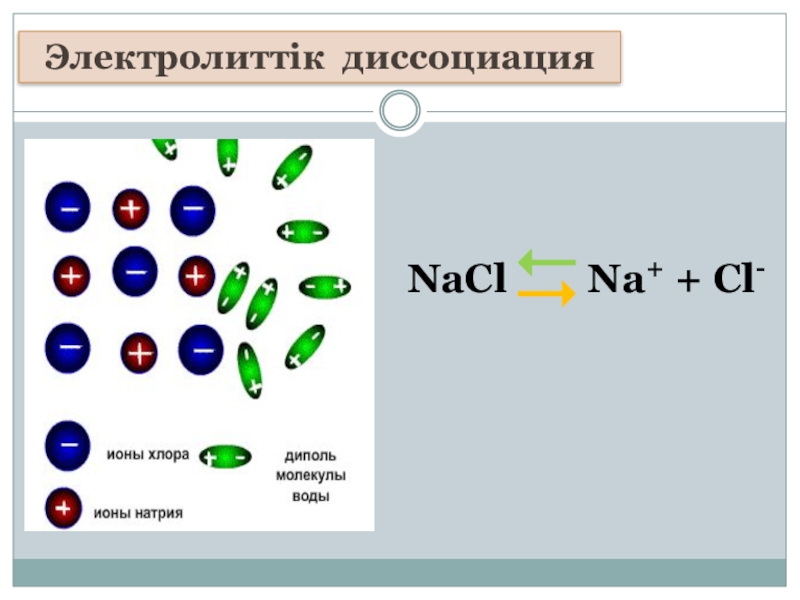
- 4. NaCl Na+ + Cl-Электролиттік диссоциация
- 5. Na ClNa+Cl-Ас тұзының электролиттік диссоциациясы NaCl →
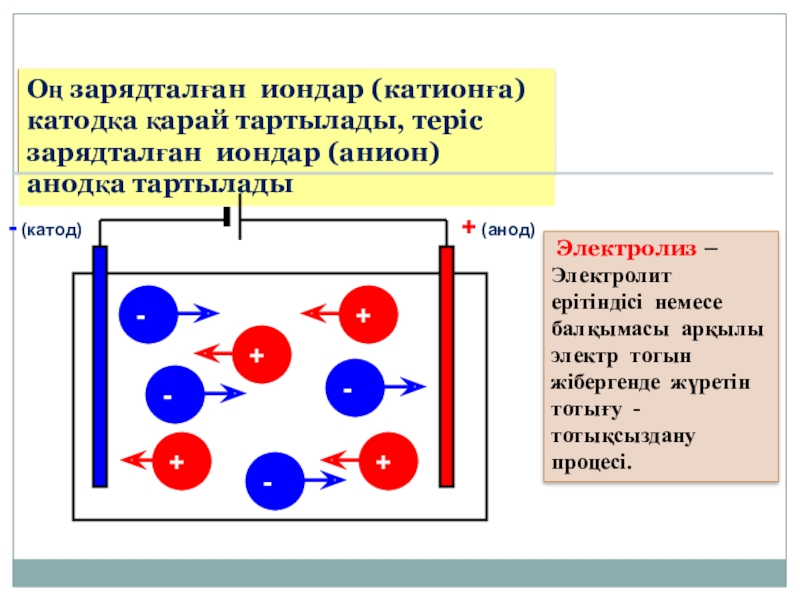
- 6. + (анод)- (катод)+++---+- Электролиз – Электролит ерітіндісі
- 7. Блиц сұрақтар1. Электролиттік диссоциация дегеніміз не?
- 8. Жауабы:Ерітінділер мен балқымаларда заттардың иондарға ыдырауы. Кері
- 9. 2 сұрақ Электролизге анықтама беріңіз?
- 10. Жауабы:Электролиз - тотығу – тотықсыздану реакциясының әсерінен электродтарда таза заттардың алыну процесі.
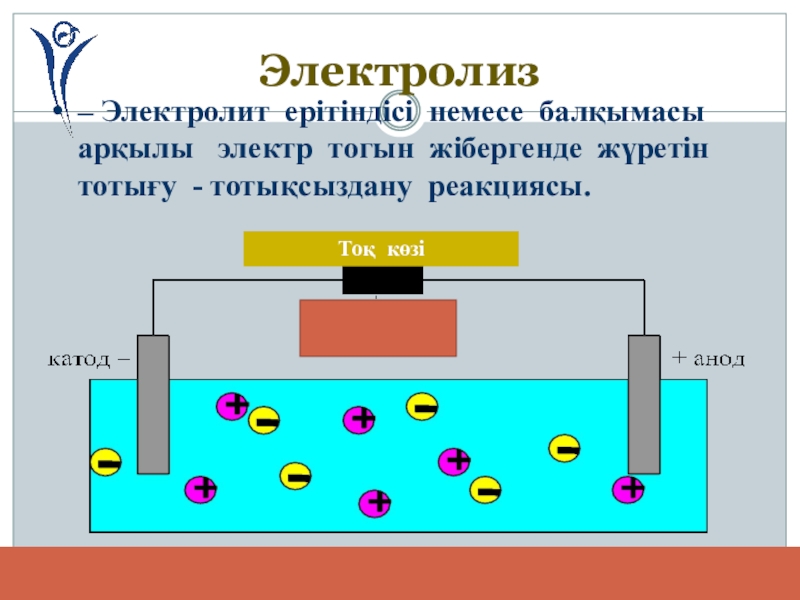
- 11. Электролиз– Электролит ерітіндісі немесе балқымасы арқылы электр тогын жібергенде жүретін тотығу - тотықсыздану реакциясы.Тоқ көзі
- 12. 1834 жылы ағылшын ғалымы Майкл Фарадей
- 13. Ғылымға үлесі 1820 ж. – магнетизмді
- 14. Электролиздің екінші заңы Электр тогының бірдей мөлшерінде
- 15. Слайд 15
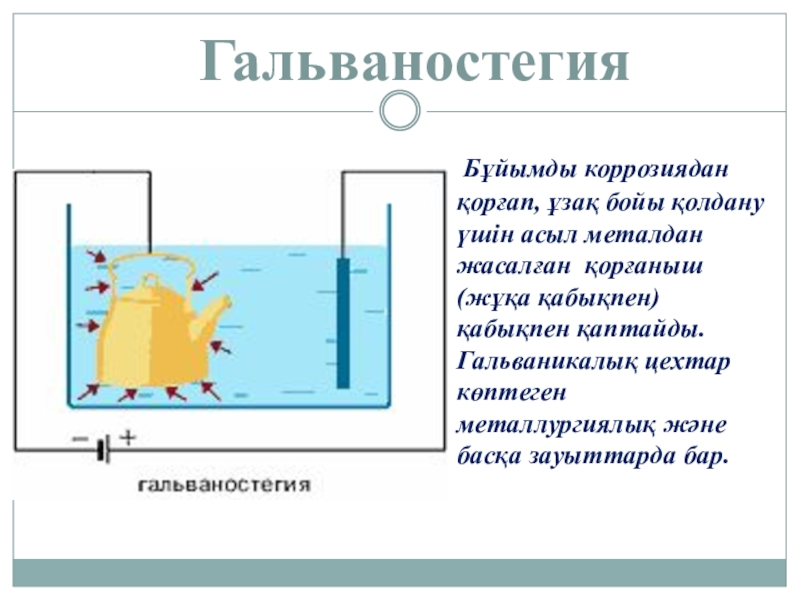
- 16. Гальваностегия Бұйымды коррозиядан қорғап, ұзақ бойы
- 17. Бұйымдарды асыл металдан жасалған қорғаныш қабықпен қаптау
- 18. Слайд 18
- 19. Слайд 19
- 20. ГАЛЬВАНОПЛАСТИКА Электрлік әдіспен қалың қабатты (бірнеше миллиметрге дейін) көшірмелер алу.Гальванопластика әдісімен алынған барельефа, көшірмесі
- 21. Медаль мен тиындар жасау үшін қолданылады
- 22. Қысқы сарай
- 23. Үлкен театр
- 24. Типографияға қажетті бұйымдар
- 25. Пресс-формы из пластмассы, резины, металла
- 26. Пластмасса, резеңке, металдан жасалған пресс-формалар
- 27. Жаттығу Сулы ерітінділер электролизында инертті
- 28. Жауабы:Сулы ерітінділер электролизында инертті
- 29. Жаттығу :Сулы ерітінділер электролизында инертті
- 30. Жаттығу :Сулы ерітінділер электролизында инертті
- 31. Үй тапсырмасы 1. Кальций хлориді балқымасының
- 32. Пайдаланған әдебиеттер мен ақпарат көздері
Слайд 2А) білімділік: Оқушылардың тотығу дәрежесі және тотығу-тотықсыздану реакция жайындағы білімдерін жүйелеу
Б) дамытушылық: экспериментті орындауда техникалық машықты қалыптастыру,ерітінді және балқыма электролиздеріне байланысты есепті шығара білу.
В) тәрбиелілік: пәнге деген ынтасын арттыру, өз бетімен жұмыс жасауды үйрету.
Сабақтың мақсаты:
Слайд 5
Na Cl
Na+
Cl-
Ас тұзының электролиттік диссоциациясы
NaCl → Na+ + Cl-
Диссоциация
CuSO4 → Cu 2+ + SO42-
HCl → H + + Cl-
H2SO4 → H+ + H+ + SO42-
CaCl2 → Ca 2+ + Cl- + Cl-
Диссоциация кезінде металл және сутек иондары үнемі оң зарядталады, ал қышқыл қалдықтары радикалдары мен ОН тобы - теріс зарядталады
Слайд 6
+ (анод)
- (катод)
+
+
+
-
-
-
+
-
Электролиз – Электролит ерітіндісі немесе балқымасы арқылы
Слайд 8Жауабы:
Ерітінділер мен балқымаларда заттардың иондарға ыдырауы. Кері процесс рекомбинациялану деп аталады).
Слайд 10Жауабы:
Электролиз - тотығу – тотықсыздану реакциясының әсерінен электродтарда таза заттардың алыну
Слайд 11
Электролиз
– Электролит ерітіндісі немесе балқымасы арқылы электр тогын жібергенде жүретін
Тоқ көзі
Слайд 12 1834 жылы ағылшын ғалымы Майкл Фарадей электролиз зерттеп, оның заңдылықтарын
Майкл Фарадей (1791 – 1867)
Электролиздің бірінші заңы
Электролиз кезінде электродта бөлінген заттың массасы электролит арқылы өткен зарядтың мәніне тура пропорционал
k – заттың электрохимиялық эквиваленті
(электролит арқылы 1Кл заряд өткен кезде бөлініп шыққан заттың массасына тең
«Электролит», «электрод», «анод», «катод» терминдерін енгізді.
Слайд 13
Ғылымға үлесі
1820 ж. – магнетизмді зерттеді.
1821 ж. –
1831 ж. – тәжірибе арқылы электр күштерін, индуктивті электр тоғын зерттеді.
1832 ж. – химиялық және электрохимиялық құбылыстар арасындағы байланысты зерттеді.
1837 ж. – индукция құбылысын ашты. 1845 ж. – тоқтың әсерінен электрленген сұйықтыққа полярланған жарықтың әсерін түсіндірді
Слайд 14Электролиздің екінші заңы
Электр тогының бірдей мөлшерінде (электролит арқылы өткен электр
M – бөлінген заттың массасы
k – электрохимиялық эквивалент М – заттың молярлық массасы
z –заттың валенттілігі
Барлық электролиттер үшін бірдей 1 моль затты бөлуге арналған заряд. Ол F Фарадей саны деп аталады.
Электрохимиялық эквивалент пен Фарадей саны қатынаспен байланысты
Слайд 16Гальваностегия
Бұйымды коррозиядан қорғап, ұзақ бойы қолдану үшін асыл
Слайд 20ГАЛЬВАНОПЛАСТИКА
Электрлік әдіспен қалың қабатты (бірнеше миллиметрге дейін) көшірмелер
Гальванопластика әдісімен алынған барельефа, көшірмесі
Слайд 27Жаттығу
Сулы ерітінділер электролизында инертті электродтарды қолданған
Заттың формуласы Анодтағы өнімдер
А) NaCl 1) Cl2
B) NaClO4 2) Cl2 , O2
C) NaOH 3) O2
D) NaBr 4) H2 , Br2
5) O2, Br2
6) Br2
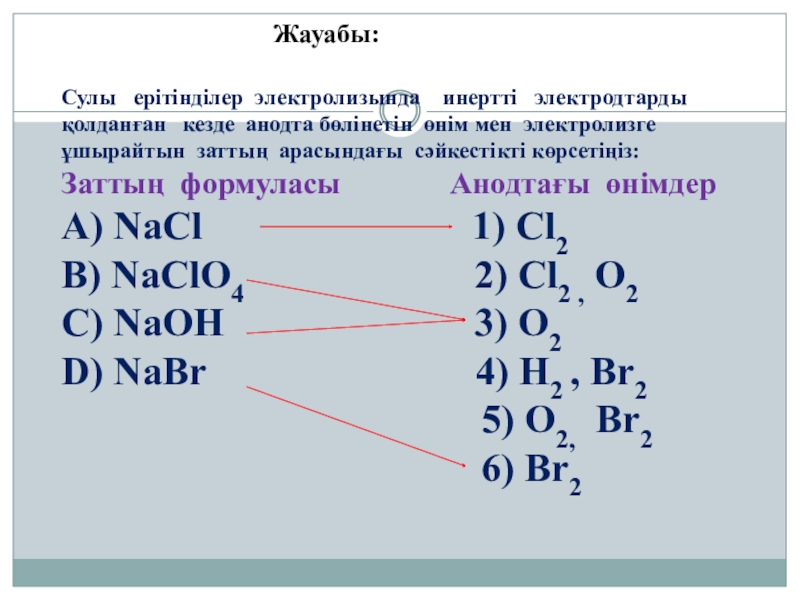
Слайд 28Жауабы:
Сулы ерітінділер электролизында инертті электродтарды қолданған кезде
Заттың формуласы Анодтағы өнімдер
А) NaCl 1) Cl2
B) NaClO4 2) Cl2 , O2
C) NaOH 3) O2
D) NaBr 4) H2 , Br2
5) O2, Br2
6) Br2
Слайд 29Жаттығу :
Сулы ерітінділер электролизында инертті электродтарды қолданған
Заттың формуласы Анодтағы өнімдер
А) HgSO4 1) F2
B) KF 2) O2
C) HgCl2 3) Hg
D) RbOH 4) H2
5) Cl2
6) H2, O2
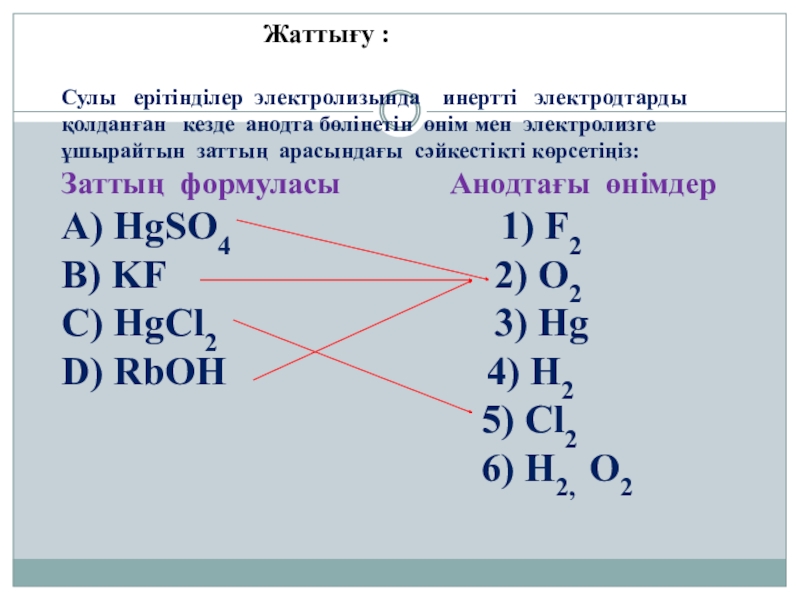
Слайд 30Жаттығу :
Сулы ерітінділер электролизында инертті электродтарды қолданған
Заттың формуласы Анодтағы өнімдер
А) HgSO4 1) F2
B) KF 2) O2
C) HgCl2 3) Hg
D) RbOH 4) H2
5) Cl2
6) H2, O2
Слайд 31Үй тапсырмасы
1. Кальций хлориді балқымасының электролизі теңдеуін
2. Темірдің (ІІ) хлориді ерітіндісінің электролизі теңдеуін жазып, катод пен анодта бөлінетін өнімдерді көрсетіңіз.
3. Электронды баланс әдісін қолданып реакция теңдеуін аяқтаңыз.
Есеп
Күміс нитратының электролит ерітіндісі арқылы 30 минут уақыт бойы 6 A тоқ күшін жұмсаған кезде ерітіндіден бөлініп шыққан металл күмістің массасын анықтаңыз.
Слайд 32Пайдаланған әдебиеттер мен ақпарат көздері
1. Габриелян О.С. Химия: пособие для
2. Слета Л.А. Химия: Справочник. – Харьков: Фолио; М.: ООО «Издательство АСТ», 2000
3. Новошинский И.И., Новошинская Н.С. Переходные металлы. – Краснодар: «Советская Кубань», 2006
4.http://www1.ege.edu.ru/
5. httphttp://http://wwwhttp://www.http://www.ithttp://www.it-http://www.it-nhttp://www.it-n.http://www.it-n.ru (сообщества «Химоза» и «Подготовка к ЕГЭ по химии»)
Н.Л. Глинка. Задачи и упражнения Общей химии
Ленинград * «Химия» 1980