- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Благородные металлы - 9 класс
Содержание
- 1. Благородные металлы - 9 класс
- 2. AuSnAgHgCu До XVIII века считалось, что существует всего семь металловFePb
- 3. Но почему именно этим металлам выпала честь называться блогородными? ? ???
- 4. Взаимодействие металлов с кислородом4Na + O2 =
- 5. Взаимодействие металлов с водойНатрий + вода =
- 6. Слайд 6
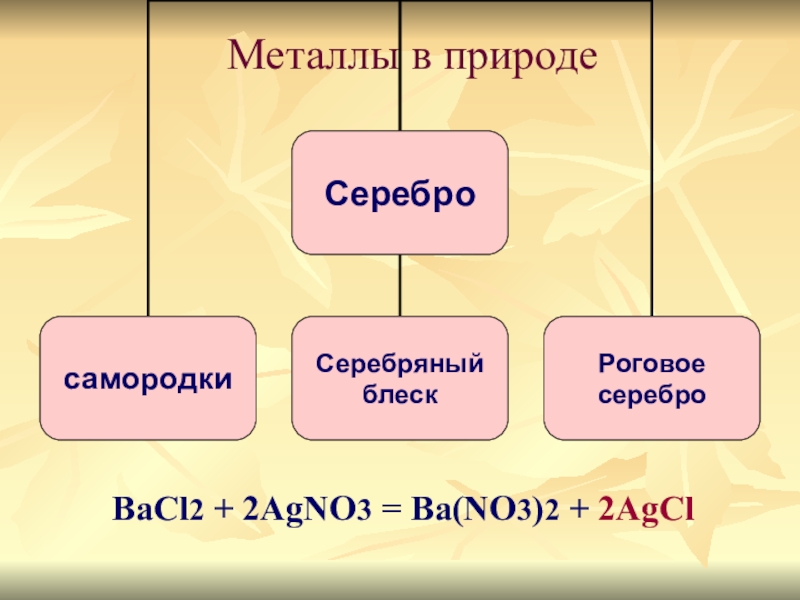
- 7. Металлы в природеBaCl2 + 2AgNO3 = Ba(NO3)2 + 2AgCl
- 8. Пробы золота В России: 375, 500,583,750,985В Англии и США проба выражена в каратах24 карата=1000Золото 18 каратов=750
- 9. Чеканка монетИз золота 900 пробыИз серебра 900 и 500 пробы
- 10. Мистический металл Золото (Au)
- 11. Золото Человек давно оценил красивый цвет
- 12. Физические характеристики золотаЭлемент 1 группыАтомный номер 79Атомная
- 13. С чем взаимодействует золото?Не растворяется, за исключением:Au
- 14. Характеристика серебраНомер группы 1 побочнаяПорядковый номер 47Номер
- 15. Значение серебра
- 16. Производство современных зеркал и экологически чистой посуды
- 17. Экологически чистая посудаСовременная посуда «Цептор»Обеззараживание воды
- 18. Ювелирная промышленность и огранка икон
- 19. Ювелирное искусство
- 20. Другое применение серебраПроводники (приборы)Посеребрение изделийАтомная промышленностьЭмульсия для кино-фотоматериалов
- 21. Серебро - инертный металл, уступает лишь золоту
- 22. Средства выразительности, основанные на переносе значения (металлы
- 23. И с Москвой золотоглавой…Светился купол золотой…Как отблеск славного былого Выходит купол золотой…
- 24. Спасибо за внимание!
- 25. Список используемой литературы1.Войлошников В.Д., Войлошникова Н.А., «Книга
Слайд 4Взаимодействие металлов с кислородом
4Na + O2 = 2Na2O
2 Cu + O2 = 2CuO
4Fe + 3O2 = 2Fe2O3
Ag + O2 = нет реакции
Au + O2 = нет реакции
6Ag + O3 = 3Ag2O
Химические свойства металлов.
Слайд 5Взаимодействие металлов с водой
Натрий + вода = ?
2Na + 2 H2O
Цинк + вода = ?
t
Zn + H2O = ZnO + H2
Золото (серебро) + вода = ?
Au (Ag) + H2O = нет реакции
Теперь не столь активный цинк возьмем
С водой. Но при условиях обычных
Мы признаков реакций не найдем,
Стараясь даже на «отлично!»
Но если сильно мы нагреем смесь,
То пузырьками на себя укажет
Газ водород, и появляясь здесь,
Он о реакции тем самым скажет:
Кусочек натрия пинцетом взять.
Отметьте, что условия обычны.
Опустим в воду – тут же результат:
Пошла реакция она экзотермична.
В миг из воды наш щелочной металл
Газ водород активно вытесняет
А тот, ликуя, что свободным стал,
Шипит и натрий по воде гоняет.
Кружит металл, как шаловливый пес,
Как будто за хвостом своим гоняясь,
Потерю электронов перенес,
С гидроксогруппой в щелочь превращаясь.
Слайд 8Пробы золота
В России:
375, 500,583,750,
985
В Англии и США
проба выражена
24 карата=1000
Золото 18 каратов=750
Слайд 11Золото
Человек давно оценил красивый цвет и блеск золота, его
Слайд 12Физические характеристики золота
Элемент 1 группы
Атомный номер 79
Атомная масса 196
Блестящий жёлтый металл
Удельный
Температура плавления = 1095 градусов
Очень мягкий металл, ковкий, тягучий,
Проводник тепла и электрического тока
Слайд 13С чем взаимодействует золото?
Не растворяется, за исключением:
Au + HNO3 + 3HCl
(«Царская водка»)
Слайд 14Характеристика серебра
Номер группы 1 побочная
Порядковый номер 47
Номер периода V большой период
Атомный
Число протонов Р+ = 47
Число электронов Е- = 47
Число нейтронов n = 60
Формула высшего оксида Me2О
Характер оксида: Основной
Светло-серый металл
Плотность 10,49 г/куб. см
Теплопроводный - первое место
Слайд 19Ювелирное искусство
Серебро, использующееся в ювелирном деле, представляет собой не чистый металл, а сплав с медью. Примесь меди часто придаёт серебряным изделиям желтоватый оттенок. Чтобы избежать этого, ювелиры отбеливают такие сплавы: изделие прокаливают на воздухе при температуре около 600 С.
Серебро — мягкий металл, поэтому зачастую оно используется в соединении с другими металлами. Серебряные монеты, например, содержат 90% серебра и 10% меди. Состав, предназначенный для украшении, ювелирных изделий и столовых приборов, содержит 92,5% серебра и 7,5% меди.
Слайд 20Другое применение серебра
Проводники (приборы)
Посеребрение изделий
Атомная промышленность
Эмульсия для кино-фотоматериалов
Слайд 21Серебро - инертный металл, уступает лишь золоту
2Ag + 4HCl =
2Ag + 2H2SO4 = Ag2SO4 + SO2 + 2H2O
3Ag + 4HNO3 + 3AgNO3 + NO + 2H2O
Слайд 22Средства выразительности, основанные на переносе значения (металлы и камни):
Золото
Серебро
Сталь
Железо
Чугун
Медь
Олово
цветы из золота
Благородные металлы у художников и поэтов.
Слайд 23И с Москвой золотоглавой…
Светился купол золотой…
Как отблеск славного былого
Выходит купол
Слайд 25Список используемой литературы
1.Войлошников В.Д., Войлошникова Н.А., «Книга о полезных ископаемых», Москва
2.Потемкин С.В. «Благородный металл», Москва «Недра» 1988г.
3.Максимов М.М. «Очерк о серебре», Москва «Недра»1991г.
4.Некрасов Б.В. «Общая химия», Москва «Химия» 1990г.
5.Карапетянц М.х. «Общая и неорганическая химия», Москва «Химия» 1993г.