- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Амины. Производство и применение . Информацию запускаю через QR
Содержание
- 1. Амины. Производство и применение . Информацию запускаю через QR
- 2. Ами́ны — органические соединения, производные аммиака — органические соединения,
- 3. НОМЕНКЛАТУРА К названию органических остатков, связанных с
- 4. ХИМИЧЕСКИЕ СВОЙСТВА Амины, являясь производными аммиака, имеют
- 5. ХИМИЧЕСКИЕ СВОЙСТВАПри нагревании с карбоновыми кислотамиПри нагревании
- 6. Первичные и вторичные амины взаимодействуют с азотистой
- 7. ПОЛУЧЕНИЕ Восстановление азотсодержащих соединений: нитросоединений(реакция Зинина).Эту реакцию
- 8. ТРИЕТИЛАМИНТриэтиламин — третичный амин. Химическая формула (С2H5)3N, часто
- 9. ПОЛУЧЕНИЕ В промышленности получают совместно с этиламиномВ
- 10. ХИМИЧЕСКИЕ СВОЙСТВА Как сильное органическое основаниеКак сильное
- 11. Анили́н (фениламин) — органическое соединение с формулой
- 12. СВОЙСТВА Для анилина характерны реакции как по
- 13. ПРОИЗВОДСТВО И ПРИМЕНЕНИЕ Изначально анилин получали восстановлением
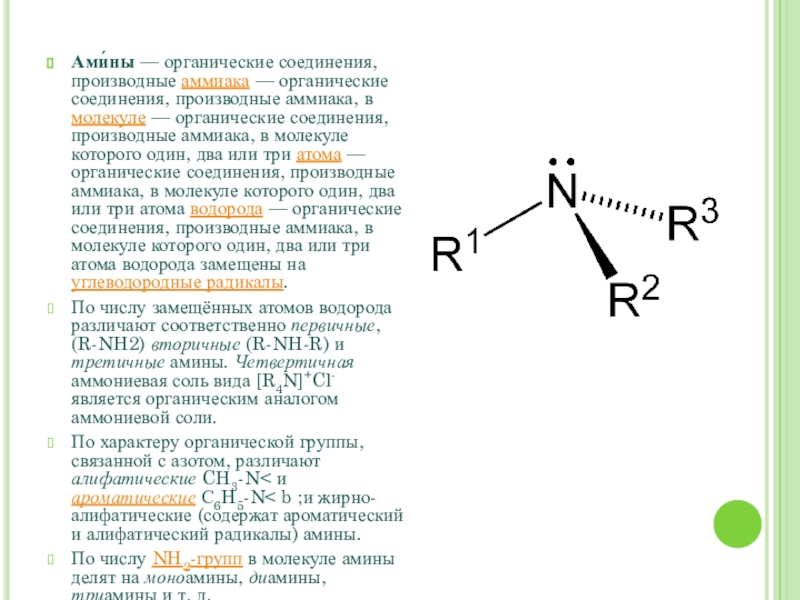
Ами́ны — органические соединения, производные аммиака — органические соединения, производные аммиака, в молекуле — органические соединения, производные аммиака, в молекуле которого один, два или три атома — органические соединения, производные аммиака, в молекуле которого один, два или три атома водорода —
Слайд 2Ами́ны — органические соединения, производные аммиака — органические соединения, производные аммиака, в молекуле —
органические соединения, производные аммиака, в молекуле которого один, два или три атома — органические соединения, производные аммиака, в молекуле которого один, два или три атома водорода — органические соединения, производные аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
По числу замещённых атомов водорода различают соответственно первичные, (R-NH2) вторичные (R-NH-R) и третичные амины. Четвертичная аммониевая соль вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По характеру органической группы, связанной с азотом, различают алифатические CH3-N< и ароматические С6H5-N< b ;и жирно-алифатические (содержат ароматический и алифатический радикалы) амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
По числу замещённых атомов водорода различают соответственно первичные, (R-NH2) вторичные (R-NH-R) и третичные амины. Четвертичная аммониевая соль вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По характеру органической группы, связанной с азотом, различают алифатические CH3-N< и ароматические С6H5-N< b ;и жирно-алифатические (содержат ароматический и алифатический радикалы) амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
Слайд 3НОМЕНКЛАТУРА
К названию органических остатков, связанных с азотом, добавляют слово «амин», при
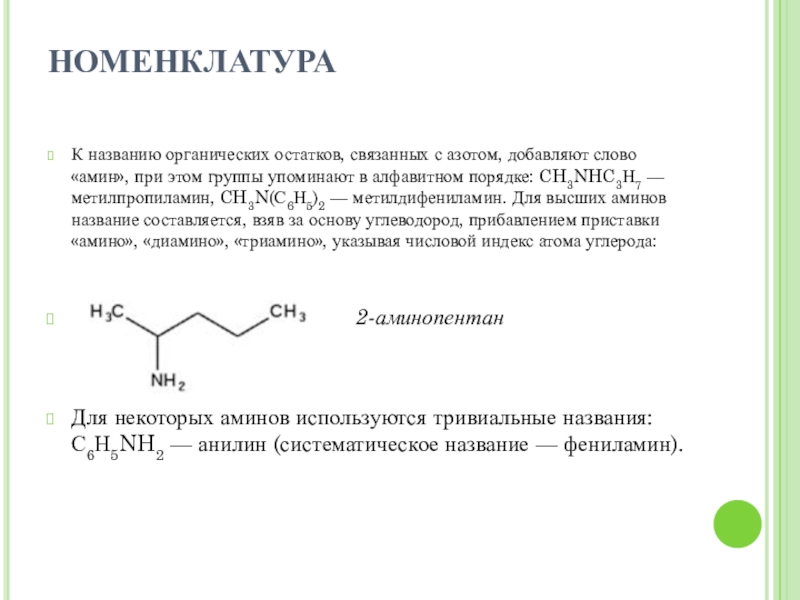
этом группы упоминают в алфавитном порядке: CH3NHC3Н7 — метилпропиламин, CH3N(С6Н5)2 — метилдифениламин. Для высших аминов название составляется, взяв за основу углеводород, прибавлением приставки «амино», «диамино», «триамино», указывая числовой индекс атома углерода:
2-аминопентан
Для некоторых аминов используются тривиальные названия: С6Н5NH2 — анилин (систематическое название — фениламин).
2-аминопентан
Для некоторых аминов используются тривиальные названия: С6Н5NH2 — анилин (систематическое название — фениламин).
Слайд 4ХИМИЧЕСКИЕ СВОЙСТВА
Амины, являясь производными аммиака, имеют сходное с ним строение и
проявляют подобные ему свойства. Для них также характерно образование донорно-акцепторной связи. Азот предоставляет неподеленную электронную пару, исполняя роль донора. В качестве акцептора электоронов может выступать, например, протон Н+, образуя ион R3NH+. Возникшая ковалентная связь N-H полностью эквивалентна остальным связям N-H в амине.
Алкиламины являются сильными основаниями, ариламины менее основны.
Водные растворы алифатических аминов проявляют щелочную реакцию, так как при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:
C2H5NH2 + H2O → [C2H5NH3]+ + OH- Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:
RNH2 + HCl → [RNH3]Cl-
Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной связи N-R, которая также эквивалентна уже имеющимся.
Алкиламины являются сильными основаниями, ариламины менее основны.
Водные растворы алифатических аминов проявляют щелочную реакцию, так как при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:
C2H5NH2 + H2O → [C2H5NH3]+ + OH- Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:
RNH2 + HCl → [RNH3]Cl-
Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной связи N-R, которая также эквивалентна уже имеющимся.
Слайд 5ХИМИЧЕСКИЕ СВОЙСТВА
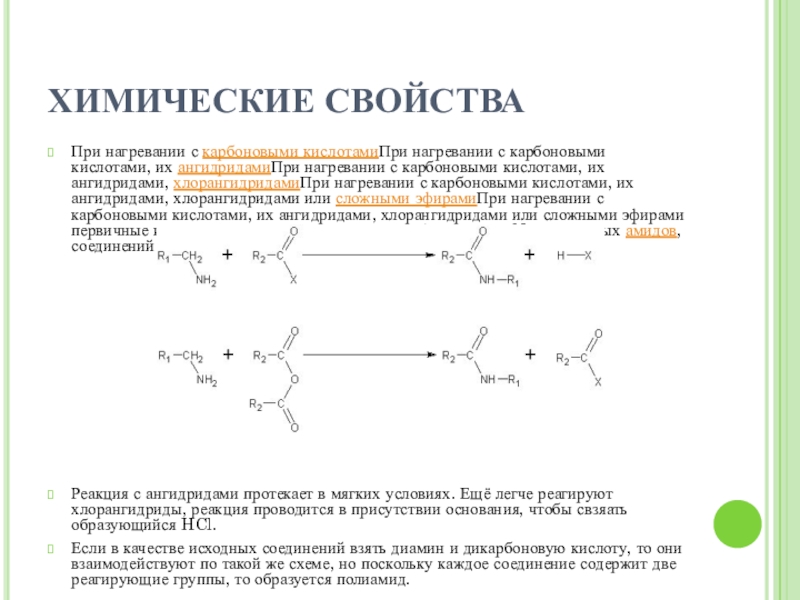
При нагревании с карбоновыми кислотамиПри нагревании с карбоновыми кислотами, их
ангидридамиПри нагревании с карбоновыми кислотами, их ангидридами, хлорангидридамиПри нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирамиПри нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирами первичные и вторичные амины ацилируются с образованием N-замещенных амидов, соединений с фрагментом -С(О)N<:
Реакция с ангидридами протекает в мягких условиях. Ещё легче реагируют хлорангидриды, реакция проводится в присутствии основания, чтобы свзяать образующийся HCl.
Если в качестве исходных соединений взять диамин и дикарбоновую кислоту, то они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полиамид.
Реакция с ангидридами протекает в мягких условиях. Ещё легче реагируют хлорангидриды, реакция проводится в присутствии основания, чтобы свзяать образующийся HCl.
Если в качестве исходных соединений взять диамин и дикарбоновую кислоту, то они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полиамид.
Слайд 6Первичные и вторичные амины взаимодействуют с азотистой кислотой различным образом. Из
первичных аминов образуются первичные спирты:
C2H5NH2 + HNO2 → C2H5OH + N2 +H2O Вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины — соединения, содержащие фрагмент >N-N=O:
(C2H5)2NH + HNO2 → (C2H5)2N-N=O + H2O Третичные амины при обычной температуре с азотистой кислотой не реагируют,
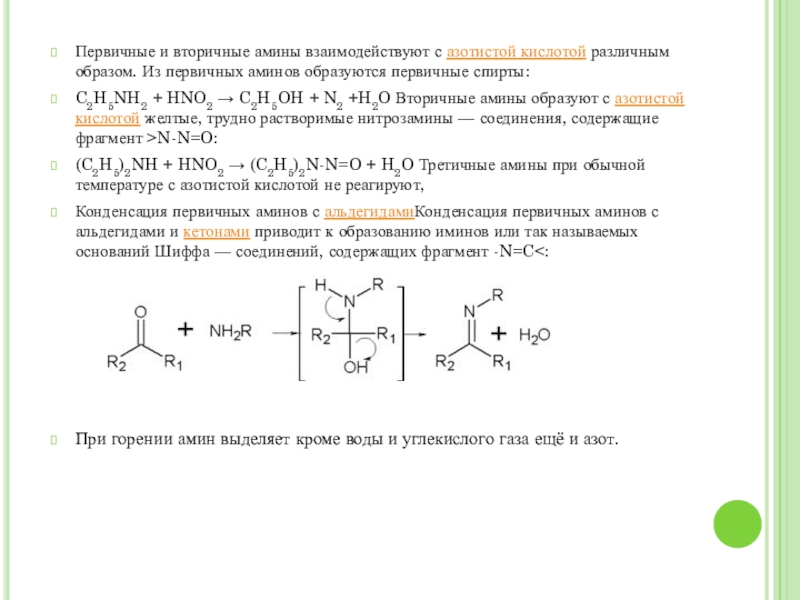
Конденсация первичных аминов с альдегидамиКонденсация первичных аминов с альдегидами и кетонами приводит к образованию иминов или так называемых оснований Шиффа — соединений, содержащих фрагмент -N=C<:
При горении амин выделяет кроме воды и углекислого газа ещё и азот.
C2H5NH2 + HNO2 → C2H5OH + N2 +H2O Вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины — соединения, содержащие фрагмент >N-N=O:
(C2H5)2NH + HNO2 → (C2H5)2N-N=O + H2O Третичные амины при обычной температуре с азотистой кислотой не реагируют,
Конденсация первичных аминов с альдегидамиКонденсация первичных аминов с альдегидами и кетонами приводит к образованию иминов или так называемых оснований Шиффа — соединений, содержащих фрагмент -N=C<:
При горении амин выделяет кроме воды и углекислого газа ещё и азот.
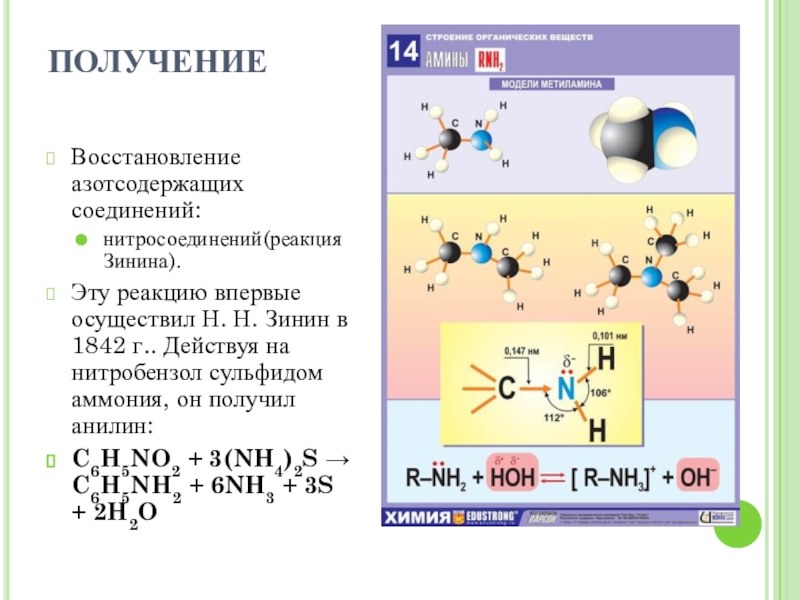
Слайд 7ПОЛУЧЕНИЕ
Восстановление азотсодержащих соединений:
нитросоединений(реакция Зинина).
Эту реакцию впервые осуществил Н. Н. Зинин в 1842 г..
Действуя на нитробензол сульфидом аммония, он получил анилин:
C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
Слайд 8ТРИЕТИЛАМИН
Триэтиламин — третичный амин. Химическая формула (С2H5)3N, часто используется обозначение Et3N. Нашёл
широкое применение, как простейший симметричный третичный амин, находящийся в жидком состоянии.
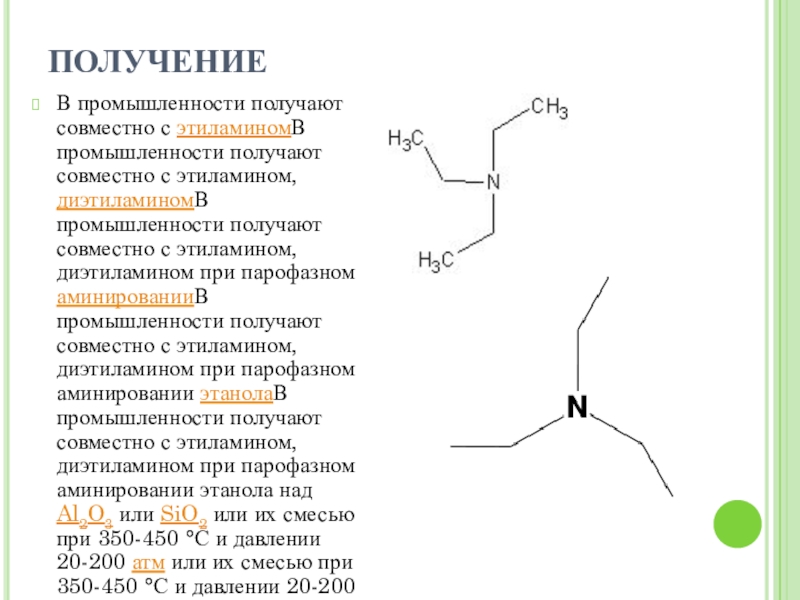
Слайд 9ПОЛУЧЕНИЕ
В промышленности получают совместно с этиламиномВ промышленности получают совместно с этиламином,
диэтиламиномВ промышленности получают совместно с этиламином, диэтиламином при парофазном аминированииВ промышленности получают совместно с этиламином, диэтиламином при парофазном аминировании этанолаВ промышленности получают совместно с этиламином, диэтиламином при парофазном аминировании этанола над Al2O3 или SiO2 или их смесью при 350-450 °С и давлении 20-200 атм или их смесью при 350-450 °С и давлении 20-200 атм либо над Ni или их смесью при 350-450 °С и давлении 20-200 атм либо над Ni, Co или их смесью при 350-450 °С и давлении 20-200 атм либо над Ni, Co, Cu или их смесью при 350-450 °С и давлении 20-200 атм либо над Ni, Co, Cu, Re или их смесью при 350-450 °С и давлении 20-200 атм либо над Ni, Co, Cu, Re и H2 при 150-230 °С и давлении 17-35 атм. Состав получаемой смеси зависит от исходных соотношений[1].
CH3CH2OHOH + NH3 = CH3CH2NH2 + H2O CH3CH2OH + CH3CH2NH2 = (CH3CH2)2NH + H2O CH3CH2OH + (CH3CH2)2NH = (CH3CH2)3N + H2O Полученная смесь разделяется ректификацией.
CH3CH2OHOH + NH3 = CH3CH2NH2 + H2O CH3CH2OH + CH3CH2NH2 = (CH3CH2)2NH + H2O CH3CH2OH + (CH3CH2)2NH = (CH3CH2)3N + H2O Полученная смесь разделяется ректификацией.
Слайд 10ХИМИЧЕСКИЕ СВОЙСТВА
Как сильное органическое основаниеКак сильное органическое основание (pKaКак сильное органическое
основание (pKa=10.87) образует кристаллические триэтиламмонийные соли с органическими и минеральными кислотами.
HCl + Et3N → Et3NH+Cl- В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов из ацилхлоридов В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов из ацилхлоридов для связывания образующегося хлороводорода.
R2NH + R'C(O)Cl + Et3N → R'C(O)NR2 + Et3NH+Cl- Также используется в реакции дегидрогалогенирования.
Триэтиламин легко алкилируется, образуя четвертичные аммониевые соли
RI + Et3N → Et3NR+I- поэтому для создания основной среды в присутствии алкилаторов поэтому для создания основной среды в присутствии алкилаторов используют диизопропилэтиламин.
HCl + Et3N → Et3NH+Cl- В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов из ацилхлоридов В качестве основания триэтиламин широко используется в органическом синтезе, в частности при синтезе сложных эфиров и амидов из ацилхлоридов для связывания образующегося хлороводорода.
R2NH + R'C(O)Cl + Et3N → R'C(O)NR2 + Et3NH+Cl- Также используется в реакции дегидрогалогенирования.
Триэтиламин легко алкилируется, образуя четвертичные аммониевые соли
RI + Et3N → Et3NR+I- поэтому для создания основной среды в присутствии алкилаторов поэтому для создания основной среды в присутствии алкилаторов используют диизопропилэтиламин.
Слайд 11
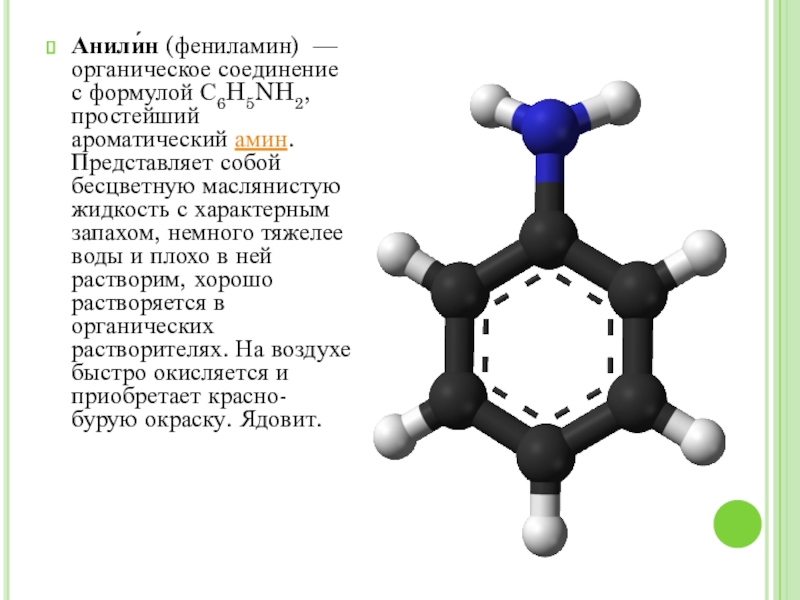
Анили́н (фениламин) — органическое соединение с формулой С6H5NH2, простейший ароматический амин.
Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного тяжелее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
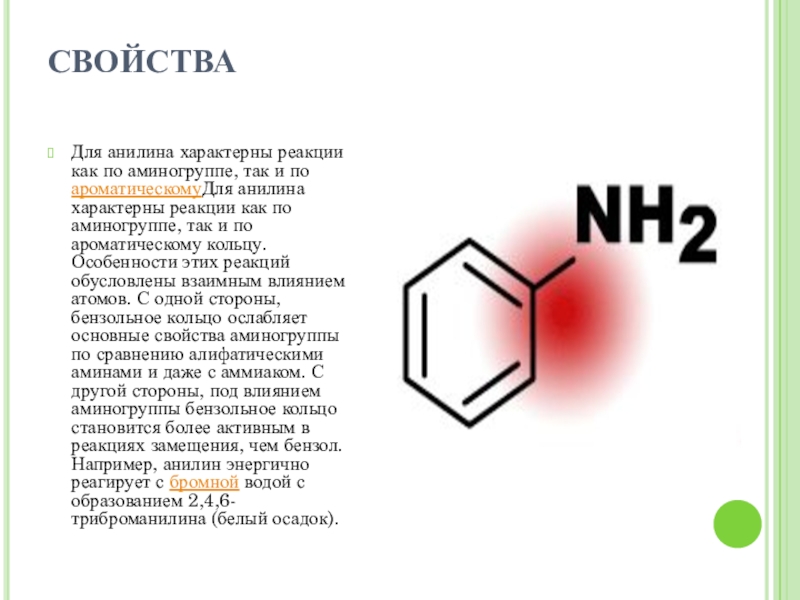
Слайд 12СВОЙСТВА
Для анилина характерны реакции как по аминогруппе, так и по ароматическомуДля
анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок).
Слайд 13ПРОИЗВОДСТВО И ПРИМЕНЕНИЕ
Изначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход
анилина не превышал 15 %. В 1842 годуИзначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. В 1842 году профессором Казанского университета Н. Н. Зининым был разработан более рациональный способ получения анилина восстановлением нитробензола (реакция ЗининаИзначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. В 1842 году профессором Казанского университета Н. Н. Зининым был разработан более рациональный способ получения анилина восстановлением нитробензола (реакция Зинина). При взаимодействии концентрированной соляной кислоты с железом выделялся атомарный водородИзначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. В 1842 году профессором Казанского университета Н. Н. Зининым был разработан более рациональный способ получения анилина восстановлением нитробензола (реакция Зинина). При взаимодействии концентрированной соляной кислоты с железом выделялся атомарный водород, более химически активный по сравнению с молекулярным. В реакционную массу вливали нитробензол, восстанавливавшийся до анилина.
Промышленное производство фиолетового красителя мовеинаПромышленное производство фиолетового красителя мовеина на основе анилина началось в 1856 году.
В настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатовВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретановВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуковВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков (9 %), гербицидовВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков (9 %), гербицидов (2 %) и красителей (2 %). [1]
В России он в основном применяется в качестве полупродукта в производстве красителейВ России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществВ России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины потребителей в среднесрочной перспективе.
Промышленное производство фиолетового красителя мовеинаПромышленное производство фиолетового красителя мовеина на основе анилина началось в 1856 году.
В настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатовВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретановВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуковВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков (9 %), гербицидовВ настоящий момент в мире основная часть (85 %) производимого анилина используется для производства метилдиизоцианатов, (MDI) используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков (9 %), гербицидов (2 %) и красителей (2 %). [1]
В России он в основном применяется в качестве полупродукта в производстве красителейВ России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществВ России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины потребителей в среднесрочной перспективе.