- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Аминокислоты 2013 год. Для урока.
Содержание
- 1. Аминокислоты 2013 год. Для урока.
- 2. Аминокислоты- это…органические соединения, в молекуле которых одновременно
- 3. Структура и физические свойства:
- 4. Химические свойства: Реакции по карбоксильным
- 5. В природе существует множество аминокислот, но их можно разделить на 2 группы:Природные(есть в жив. организмах)Синтетические
- 6. Применение аминокислот: Смеси L-аминокислот.,
- 7. Амины для спортсменовВ бодибилдинге аминокислоты называют еще
- 8. Все свойства, о которых было
- 9. С точки зрения биологии……аминокислоты - это строительный
- 10. Уровни организации:Кроме последовательности аминокислот полипептида (первичной структуры),
- 11. Уровни организации наглядно:
- 12. Вывод: Вообщем, аминокислоты- это незаменимые вещества
Аминокислоты- это…органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.Структура α-аминокислоты с аминогруппой слева и карбоксильной группой
Слайд 2Аминокислоты- это…
органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные
группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Структура α-аминокислоты с
аминогруппой слева и карбоксильной
группой справа
Слайд 3Структура и физические свойства:
По физическому и ряду
химических свойств аминокислоты резко отличаются от соответствующих кислот и оснований. Они лучше растворяются в воде, чем в органических р-рителях; хорошо кристаллизуются; имеют высокую плотность и исключительно высокие температуры плавления (часто разложения). Эти св-ва указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твердом состоянии и в растворе (в широком интервале рН) находятся в цвиттер-ионной форме( цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO-. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот) Например, для глицина кислотно-основное равновесие:
Слайд 4Химические свойства:
Реакции по карбоксильным группам аминокислот, аминогруппа которых
защищена ацилированием или солеобразованием, протекают аналогично превращениям карбоновых кислот. Аминокислоты легко образуют соли, сложные эфиры, амиды, гидразиды, азиды, тиоэфиры, галогенангидриды, смешанные ангидриды и т.д. Эфиры аминокислот под действием натрия или магнийорг. соед. превращаются в аминоспирты. При сухой перегонке в присутствии Ва(ОН)2 аминокислоты декарбоксилируются.
Р-ции аминогрупп аминокислот аналогичны превращениям аминов.
Р-ции аминогрупп аминокислот аналогичны превращениям аминов.
Слайд 5В природе существует множество аминокислот, но их можно разделить на 2
группы:
Природные(есть в жив. организмах)
Синтетические
Природные(есть в жив. организмах)
Синтетические
Слайд 6Применение аминокислот:
Смеси L-аминокислот., а также индивидуальные аминокислоты
применяют в медицине для парэнтерального питания больных с заболеваниями пищеварительной и др. органов, при нарушениях обмена веществв и др.; лизин, метионин, треонин, триптофан - в животноводстве для обогащения кормов; глутамат натрия и лизин - в пищевой промышленности. . и их лактамы служат для промышленного производства полиамидов. Аминомасляная кислота - медиатор в центральной нервной системе, применяется как лекарствоенн ср-во при сосудистых заболеваниях головного мозга. Ароматич. аминокислоты используют в синтезе красителей и лек. средств. На основе аминокарбоновых и аминофосфоновых к-т синтезируют селективные комплексоны, комплексообразующие иониты, лигандообменные сорбенты, ПАВ.
Слайд 7Амины для спортсменов
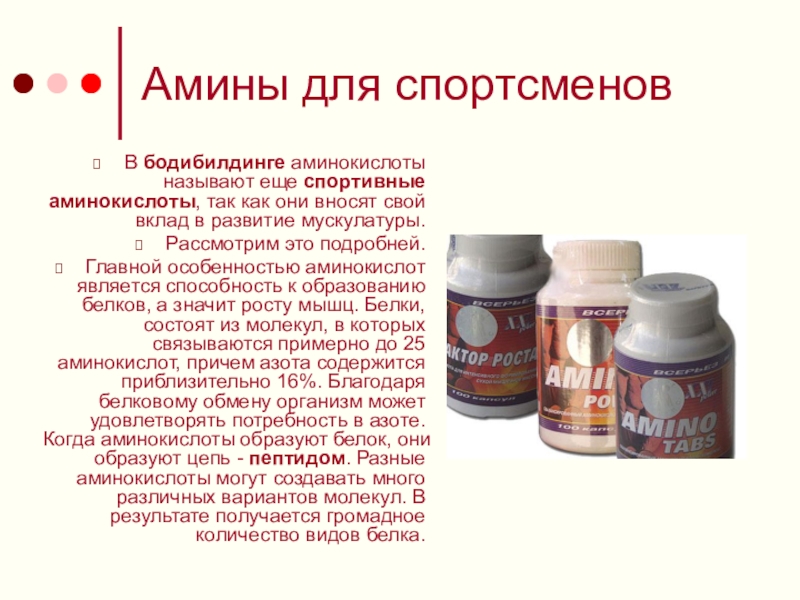
В бодибилдинге аминокислоты называют еще спортивные аминокислоты, так как
они вносят свой вклад в развитие мускулатуры.
Рассмотрим это подробней.
Главной особенностью аминокислот является способность к образованию белков, а значит росту мышц. Белки, состоят из молекул, в которых связываются примерно до 25 аминокислот, причем азота содержится приблизительно 16%. Благодаря белковому обмену организм может удовлетворять потребность в азоте. Когда аминокислоты образуют белок, они образуют цепь - пептидом. Разные аминокислоты могут создавать много различных вариантов молекул. В результате получается громадное количество видов белка.
Рассмотрим это подробней.
Главной особенностью аминокислот является способность к образованию белков, а значит росту мышц. Белки, состоят из молекул, в которых связываются примерно до 25 аминокислот, причем азота содержится приблизительно 16%. Благодаря белковому обмену организм может удовлетворять потребность в азоте. Когда аминокислоты образуют белок, они образуют цепь - пептидом. Разные аминокислоты могут создавать много различных вариантов молекул. В результате получается громадное количество видов белка.
Слайд 8 Все свойства, о которых было написано в предыдущих слайдах,
описывают аминокислоты с химической точки зрения. А каково же строение аминокислот с биологической точки зрения?...
Слайд 9С точки зрения биологии…
…аминокислоты - это строительный материал молекул белка. Все
клетки человека содержат аминокислоты.
Бесконечное разнообразие белков создается за счет различного сочетания всего лишь 20 аминокислот. Общим признаком аминокислот, входящих в состав белка (исключение составляет пролин), является наличие свободной карбоксильной группы и свободной незамещенной аминогруппы у альфа-углеродного атома.
Бесконечное разнообразие белков создается за счет различного сочетания всего лишь 20 аминокислот. Общим признаком аминокислот, входящих в состав белка (исключение составляет пролин), является наличие свободной карбоксильной группы и свободной незамещенной аминогруппы у альфа-углеродного атома.
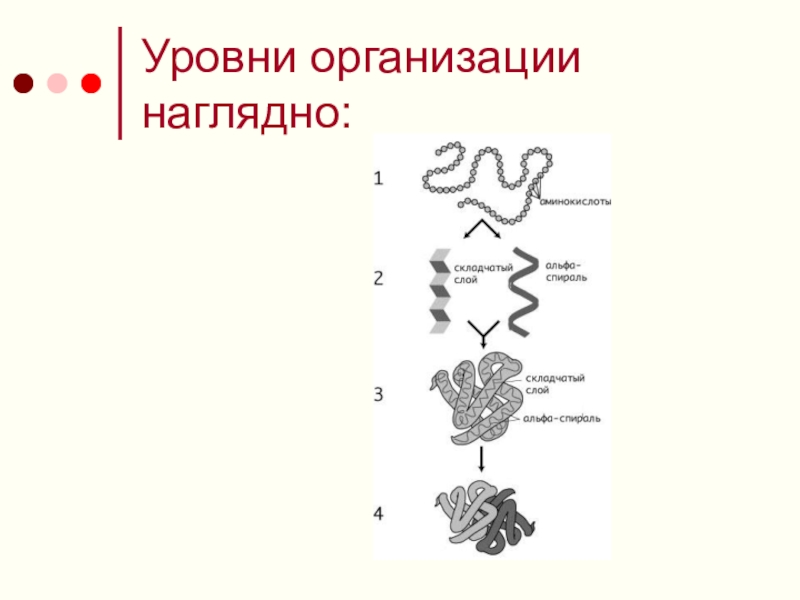
Слайд 10Уровни организации:
Кроме последовательности аминокислот полипептида (первичной структуры), крайне важна трёхмерная структура
белка, которая формируется в процессе фолдинга (от англ. folding, «сворачивание»). Трёхмерная структура формируется в результате взаимодействия структур более низких уровней. Выделяют четыре уровня структуры белка:
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, важных для функции белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями и гидрофобными взаимодействиями.
Третичная или трёхмерная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий.
Четверичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, важных для функции белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями и гидрофобными взаимодействиями.
Третичная или трёхмерная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий.
Четверичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру
Слайд 12Вывод:
Вообщем, аминокислоты- это незаменимые вещества как в организме человека,
где они выполняют различные важные функции и без которых нормальное функционирование организма невозможно, так и в природе.