- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему 29. урок по теме Аммиак
Содержание
- 1. 29. урок по теме Аммиак
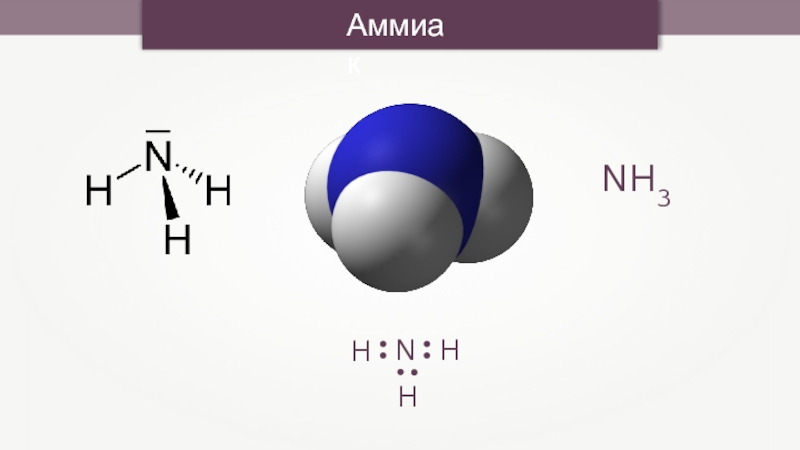
- 2. АммиакNHHH
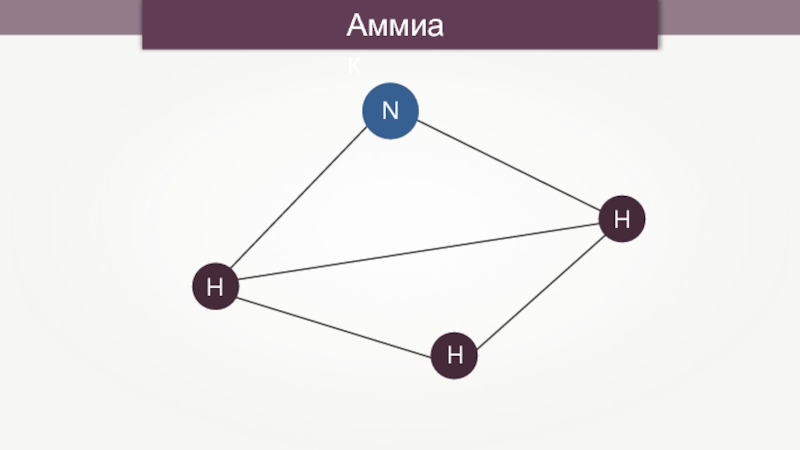
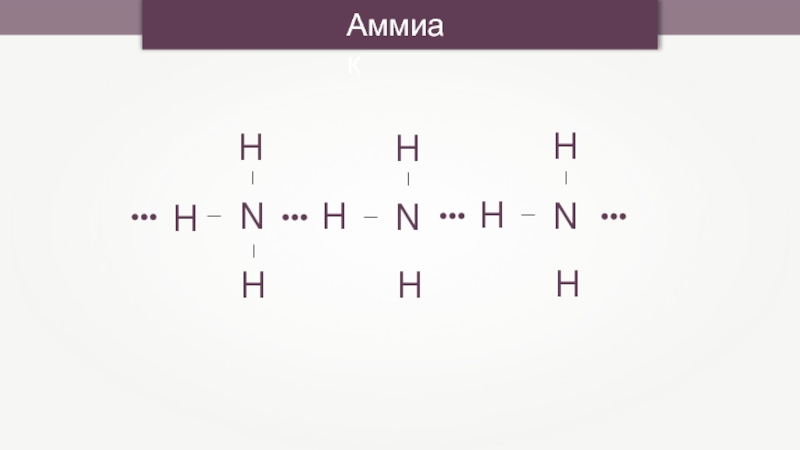
- 3. АммиакNHHH———HNHH——HNHH——
- 4. Аммиак
- 5. Аммиак переходит из газообразного в жидкое состояние
- 6. АммиакАммиачная водаНашатырный спирт
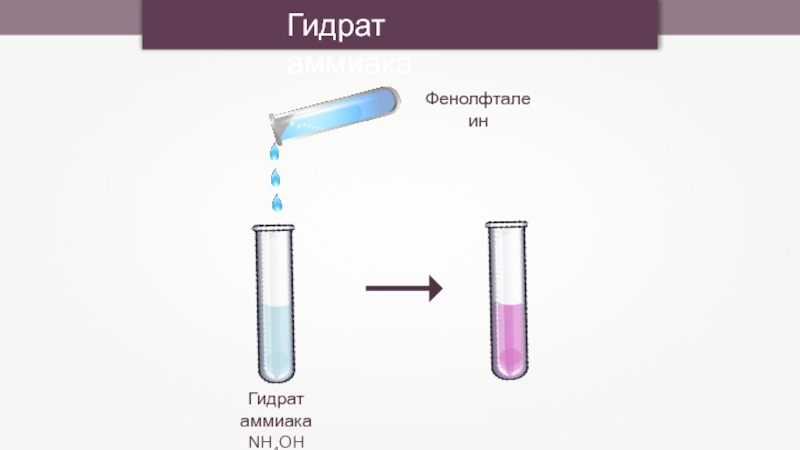
- 7. Гидрат аммиака
- 8. Гидрат аммиака Гидрат аммиакаNH4OHФенолфталеин
- 9. Аммиак способен взаимодействовать с кислотами. В результате
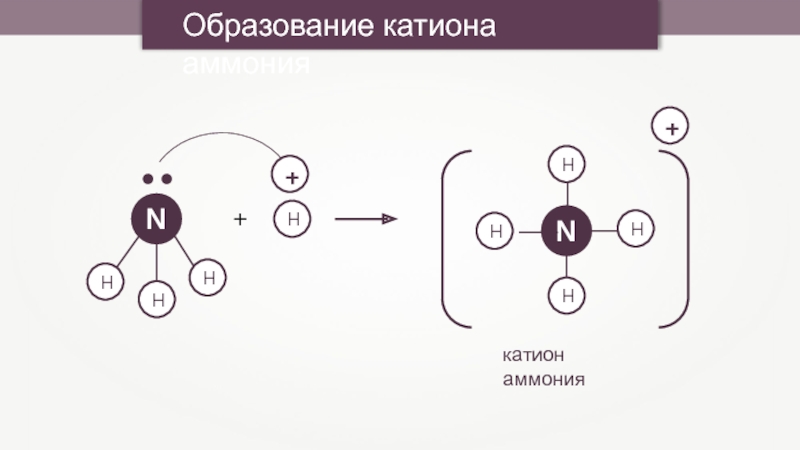
- 10. Образование катиона аммонияHHH+HH++катион аммония
- 11. Степень окисления азота в молекуле аммиака минимальная
- 12. Без участия катализатора аммиак окисляется кислородом до
- 13. Получение аммиака в промышленностиN2 + 3H2 = 2NH3
- 14. Распознать аммиак можно:По характерному запахуИспользуя влажную лакмусовую
- 15. Применение аммиакаИспользование в холодильных установкахПроизводство азотной кислотыПроизводство
АммиакNHHH
Слайд 5
Аммиак переходит из газообразного в жидкое состояние уже при –33,4 оС.
Процесс испарения жидкого аммиака сопровождается поглощением тепла из окружающей среды, такая особенность позволяет использовать аммиак в холодильных установках.
Слайд 9
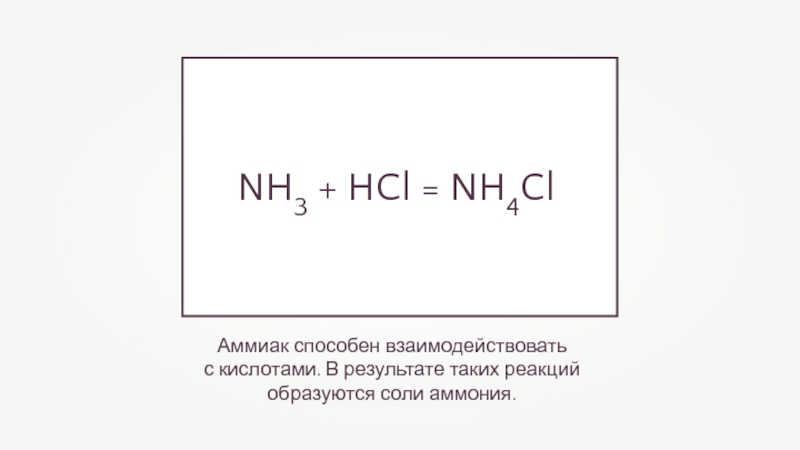
Аммиак способен взаимодействовать
с кислотами. В результате таких реакций образуются соли
аммония.
NH3 + HCl = NH4Cl
Слайд 11
Степень окисления азота в молекуле аммиака минимальная отрицательная и равна –3,
следовательно, аммиак в окислительно-восстановительных реакциях может выступать исключительно в роли восстановителя.
Слайд 12
Без участия катализатора аммиак окисляется кислородом до свободного азота, в присутствии
катализатора — до оксида азота (II).
4NH3 + 3O2 = 2N2 + 6H2O
4NH3 + 5O2 = 4NO + 6H2O
Слайд 14
Распознать аммиак можно:
По характерному запаху
Используя влажную лакмусовую бумажку, которая в присутствии
аммиака приобретёт синюю окраску
По белому дыму, который появляется при внесении в аммиак стеклянной палочки, смоченной соляной кислотой
Слайд 15
Применение аммиака
Использование в холодильных установках
Производство азотной кислоты
Производство минеральных удобрений
Использование для паяния
Для
получения взрывчатых веществ
Использование в медицине и быту