- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему 15. Бериллий, магний и щёлочноземельные металлы
Содержание
- 1. 15. Бериллий, магний и щёлочноземельные металлы
- 2. БериллийChemicalinterestМагнийPtyxDePiep
- 3. Слайд 3
- 4. БарийChemicalinterestМагнийPtyx
- 5. СтронцийКальцийAlchemist-hpJurii
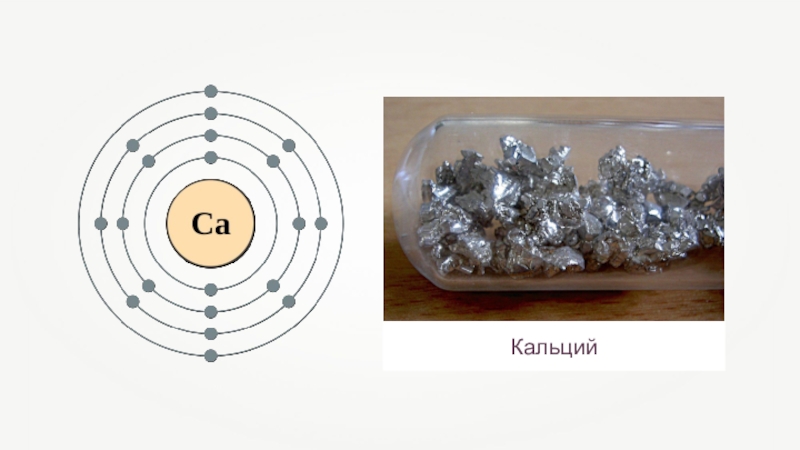
- 6. Кальций
- 7. Слайд 7
- 8. Слайд 8
- 9. Ca + CI2 = CaCI2хлоридХимические свойства металлов
- 10. Сa + S = CaSсульфидХимические свойства металлов
- 11. 3Сa + N2 = Ca3N2нитридХимические свойства металлов
- 12. Сa + 2Н2О = Ca(ОН)2+ Н2Химические свойства
- 13. 2Сa + О2 = 2CaОХимические свойства металлов
- 14. Сa + 2С = CaС2Химические свойства металлов
- 15. Вследствие своей высокой химической активности в природе
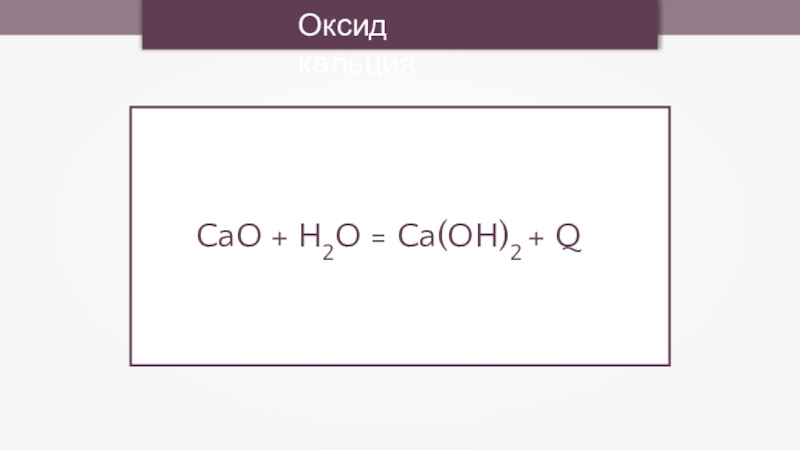
- 16. Оксид кальция
- 17. Оксид кальцияCaO + H2O = Ca(OH)2 + Q
- 18. Гашёная известь
- 19. Щелочные свойства гашёной известиCa(OH)2 + CO2 → CaCO3↓ + H2O
- 20. При пропускании через известковую воду оксида углерода
- 21. Карбонат кальцияCaCO3
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Сульфат кальцияCaSO4 ⋅ 2H2О
- 26. Жжёный гипс
- 27. Если алебастр смешать с водой, то он
- 28. Сульфат кальция широко используют в строительстве для
Слайд 1
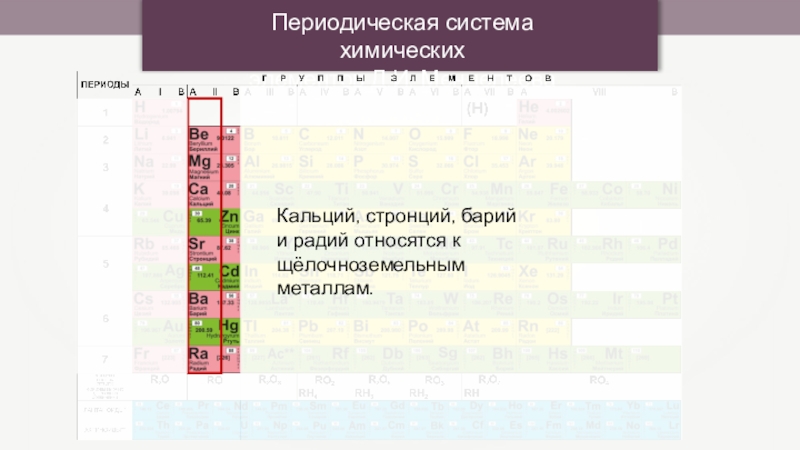
Периодическая система химических
элементов Д.И. Менделеева
Кальций, стронций, барий и радий относятся
Слайд 9
Ca + CI2 = CaCI2
хлорид
Химические свойства металлов
главной подгруппы II группы
При взаимодействии кальция с хлором образуется хлорид кальция.
Слайд 10
Сa + S = CaS
сульфид
Химические свойства металлов
главной подгруппы II группы
При взаимодействии кальция с серой образуется сульфид кальция.
Слайд 11
3Сa + N2 = Ca3N2
нитрид
Химические свойства металлов
главной подгруппы II группы
При взаимодействии кальция с азотом образуется нитрид кальция.
Слайд 12
Сa + 2Н2О = Ca(ОН)2+ Н2
Химические свойства металлов
главной подгруппы II
Кальций (Ca), являясь активным металлом, вытесняет водород из воды.
Слайд 13
2Сa + О2 = 2CaО
Химические свойства металлов
главной подгруппы II группы
При нагревании на воздухе кальций сгорает, образуя оксид кальция.
2М + О2 = 2МО
0
0
+2
–2
t
4e
–
Слайд 14
Сa + 2С = CaС2
Химические свойства металлов
главной подгруппы II группы
При взаимодействии кальций с углеродом образуется карбид кальция.
карбид кальция
Слайд 15
Вследствие своей высокой химической активности в природе щёлочноземельные металлы находятся только
Оксиды данных металлов твёрдые белые тугоплавкие вещества, устойчивые к воздействию высоких температур. Проявляют основные свойства.
Слайд 20
При пропускании через известковую воду оксида углерода (IV) раствор мутнеет.
CaСO3 +
→
→
Слайд 27
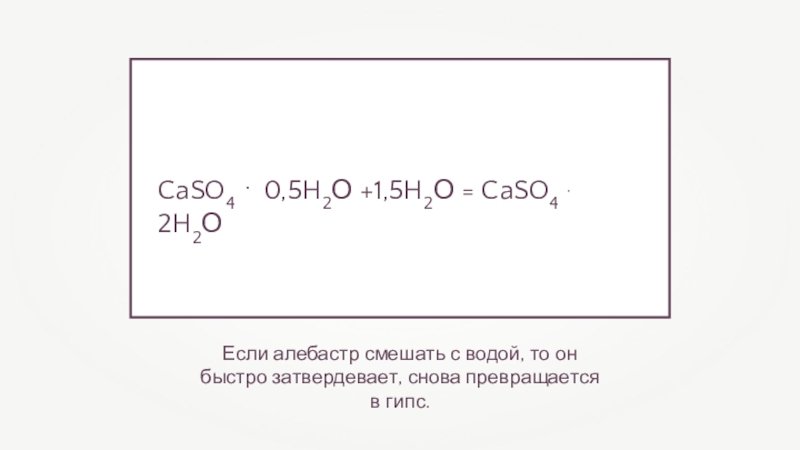
Если алебастр смешать с водой, то он быстро затвердевает, снова превращается
CaSO4 ⋅ 0,5H2О +1,5H2О = CaSO4 ⋅ 2H2О