- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по физике Основы термодинамики
Содержание
- 1. Презентация по физике Основы термодинамики
- 2. Внутренняя энергияСумма кинетических энергий хаотического движения всех
- 3. Внутренняя энергия одноатомного идеального газаДля идеального газа:
- 4. Способы изменения внутренней энергии Совершение работыАнад телом ( U увелич.)самим телом (U уменьш.)ТеплопередачаQВиды теплопередачи:теплопроводностьконвекцияизлучение
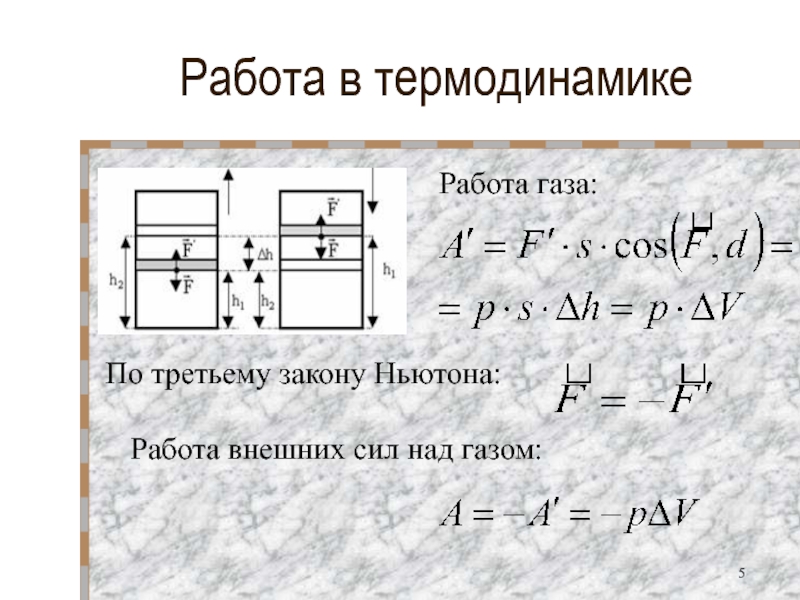
- 5. Работа в термодинамикеПо третьему закону Ньютона: Работа внешних сил над газом:Работа газа:
- 6. Геометрический смысл работыРабота численно равна площади под
- 7. Количество теплотыQ = cm(t02-t01) – нагревание (охлаждение)Q=±λm
- 8. Первый закон термодинамикиОбмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы
- 9. Первый закон термодинамикиИзменение внутренней энергии системы при
- 10. 1 закон термодинамики для изопроцессов Изотермический процесс Т-пост, Изобарный процесс р-постИзохорный процесс V- пост
- 11. Адиабатный процессМодель. Адиабатический процессСемейства изотерм (красные кривые)
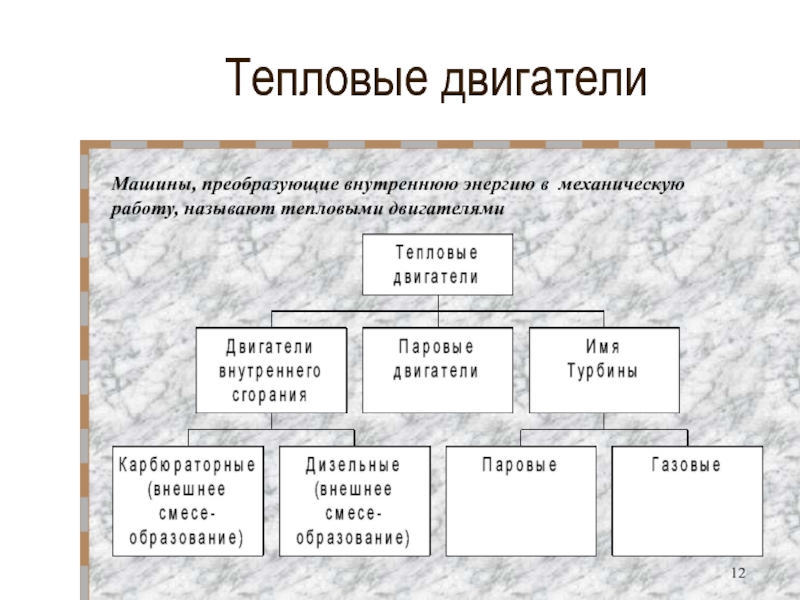
- 12. Тепловые двигателиМашины, преобразующие внутреннюю энергию в механическую работу, называют тепловыми двигателями
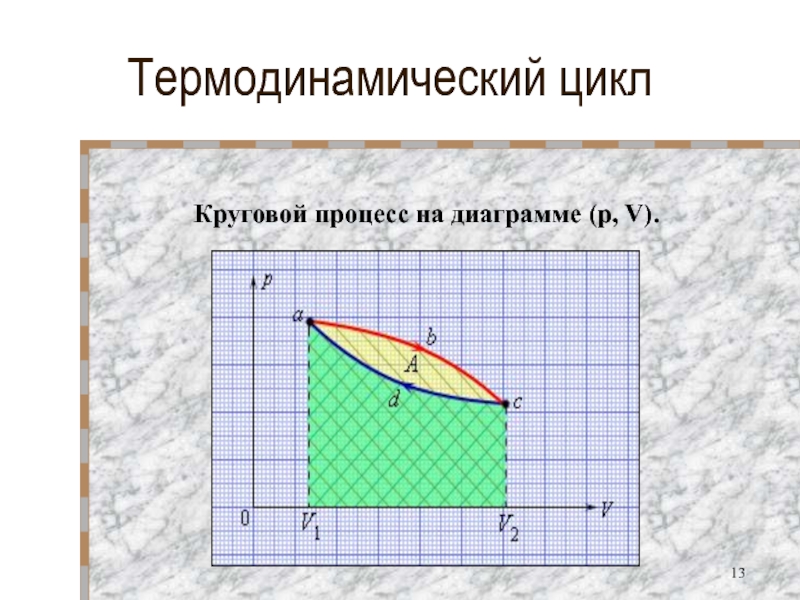
- 13. Термодинамический циклКруговой процесс на диаграмме (p, V).
- 14. Тепловой двигательКПД теплового двигателяКпд реальных двигателей:турбореактивный -
- 15. Идеальная тепловая машинаИдеальная тепловая машина - машина
- 16. Второй закон термодинамикиВторой з-н термодинамики указывает направление
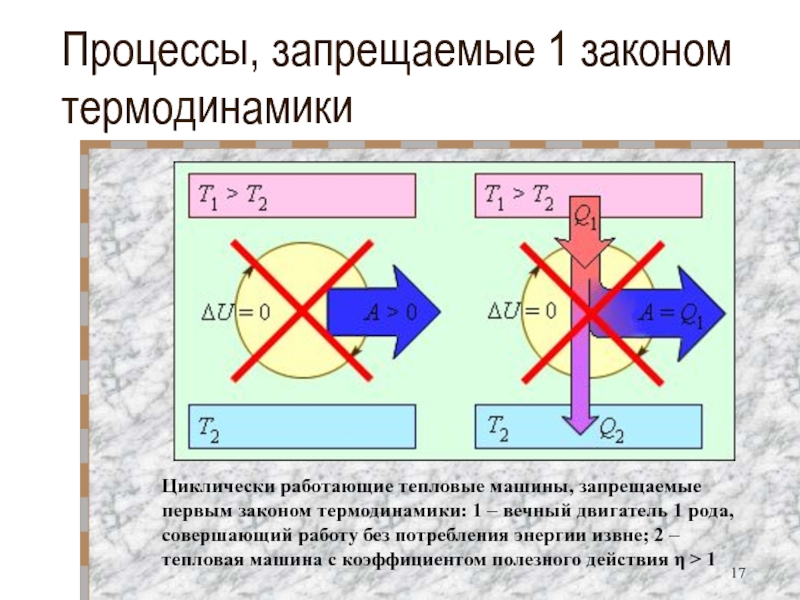
- 17. Процессы, запрещаемые 1 законом термодинамикиЦиклически работающие тепловые
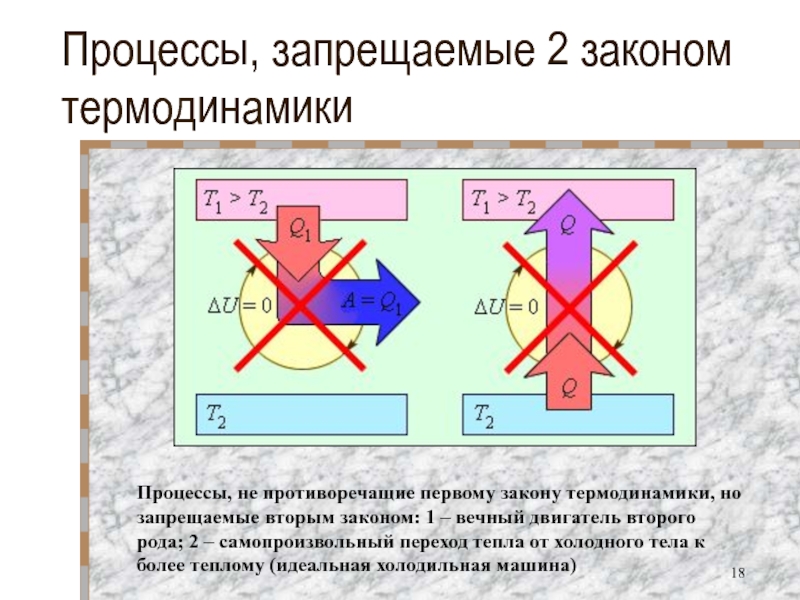
- 18. Процессы, запрещаемые 2 законом термодинамикиПроцессы, не противоречащие
Слайд 2Внутренняя энергия
Сумма кинетических энергий хаотического движения всех частиц тела относительно центра
Кинетическая энергия частиц определяется скоростью, а значит - температурой тела.
Потенциальная - расстоянием между частицами, а значит - объемом.
Следовательно: U=U(T,V) - внутренняя энергия зависит от объема и температуры.
Слайд 3Внутренняя энергия одноатомного идеального газа
Для идеального газа: U=U(T), т.к. взаимодействием на
или
Внутренняя энергия одноатомного идеального газа:
Слайд 4Способы изменения внутренней энергии
Совершение работы
А
над телом
( U увелич.)
самим телом
(U уменьш.)
Теплопередача
Q
Виды теплопередачи:
теплопроводность
конвекция
излучение
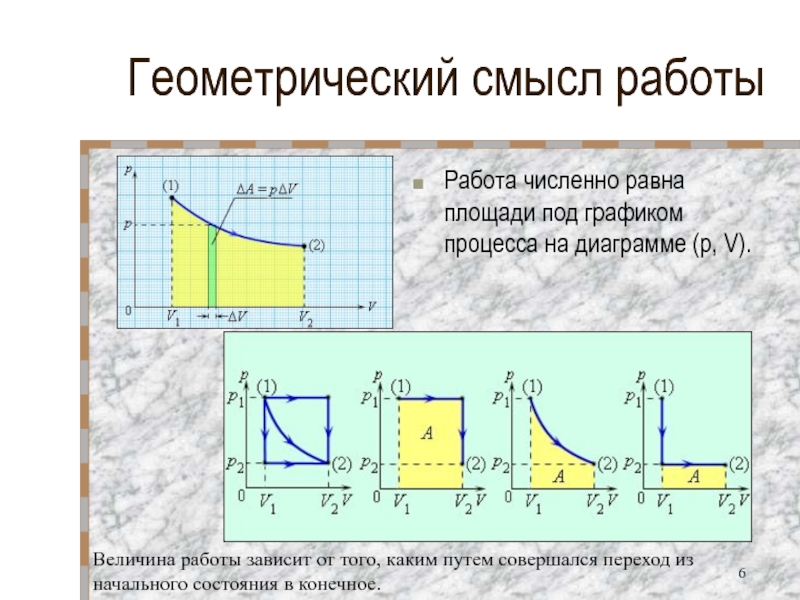
Слайд 6Геометрический смысл работы
Работа численно равна площади под графиком процесса на диаграмме
Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное.
Слайд 7Количество теплоты
Q = cm(t02-t01) – нагревание (охлаждение)
Q=±λm - плавление (отвердевание)
Q =
Q = qm – сгорание топлива
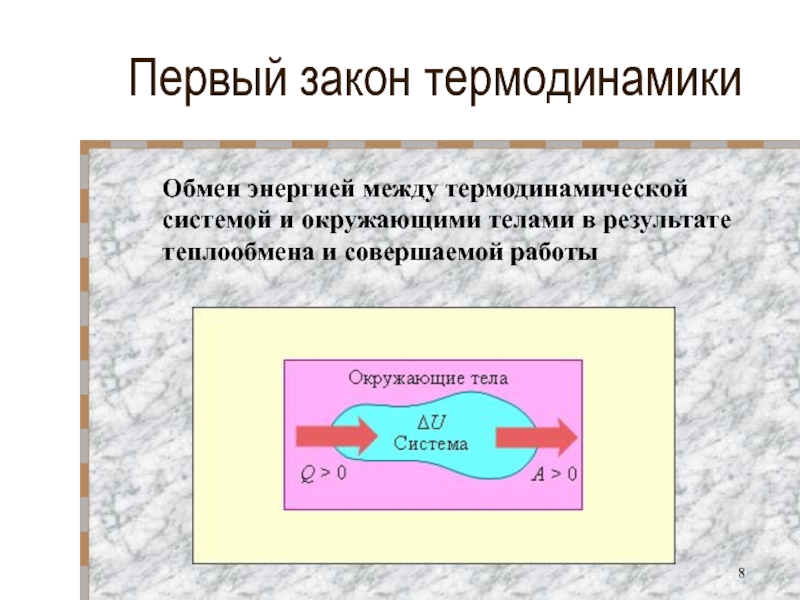
Слайд 8Первый закон термодинамики
Обмен энергией между термодинамической системой и окружающими телами в
Слайд 9Первый закон термодинамики
Изменение внутренней энергии системы при переходе ее из одного
Если А - работа внешних сил, а А' - работа газа, то А = - А' (в соответствии с 3-м законом Ньютона). Тогда:
другая форма записи первого закона термодинамики
Слайд 101 закон термодинамики для изопроцессов
Изотермический процесс Т-пост,
Изобарный процесс р-пост
Изохорный
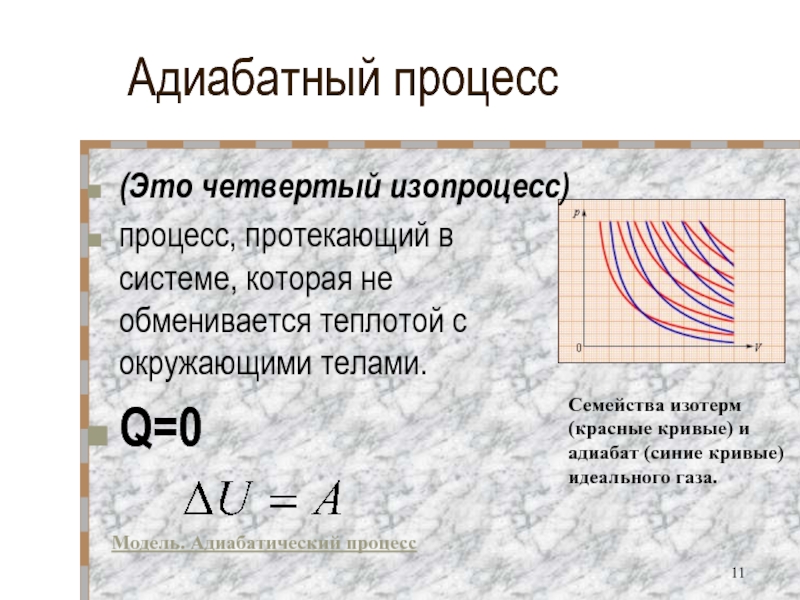
Слайд 11Адиабатный процесс
Модель. Адиабатический процесс
Семейства изотерм (красные кривые) и адиабат (синие кривые)
(Это четвертый изопроцесс)
процесс, протекающий в системе, которая не обменивается теплотой с окружающими телами.
Q=0
Слайд 12Тепловые двигатели
Машины, преобразующие внутреннюю энергию в механическую работу, называют тепловыми двигателями
Слайд 14Тепловой двигатель
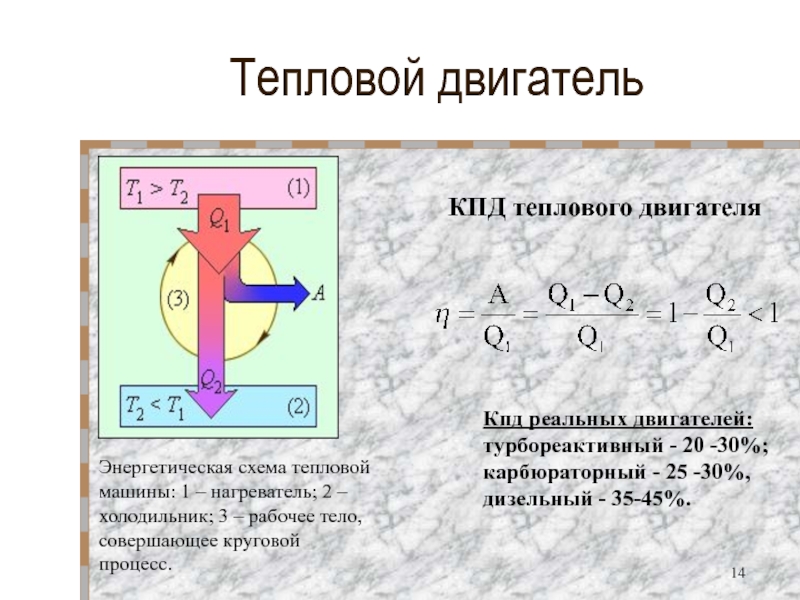
КПД теплового двигателя
Кпд реальных двигателей:
турбореактивный - 20 -30%; карбюраторный -
дизельный - 35-45%.
Энергетическая схема тепловой машины: 1 – нагреватель; 2 – холодильник; 3 – рабочее тело, совершающее круговой процесс.
Слайд 15Идеальная тепловая машина
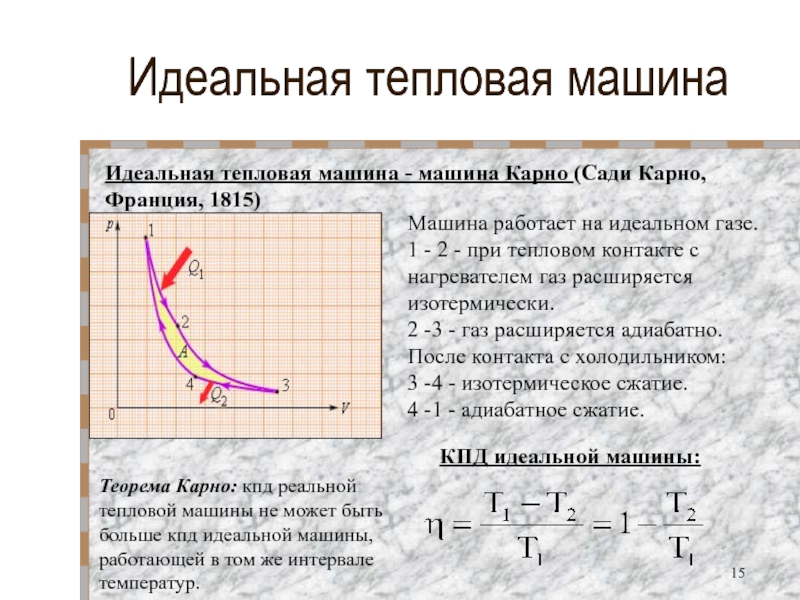
Идеальная тепловая машина - машина Карно (Сади Карно, Франция,
Машина работает на идеальном газе.
1 - 2 - при тепловом контакте с нагревателем газ расширяется изотермически.
2 -3 - газ расширяется адиабатно.
После контакта с холодильником:
3 -4 - изотермическое сжатие.
4 -1 - адиабатное сжатие.
КПД идеальной машины:
Теорема Карно: кпд реальной тепловой машины не может быть больше кпд идеальной машины, работающей в том же интервале температур.
Слайд 16Второй закон термодинамики
Второй з-н термодинамики указывает направление возможных энергетических превращений и
Формулировка Р. Клаузиуса: невозможно перевести тепло от более холодной системы к более горячей при отсутствии одновременных изменений в обеих системах или окружающих телах.
Формулировка У. Кельвина: невозможно осуществить такой периодический процесс, единственным результатом которого было бы получение работы за счет теплоты, взятой от одного источника.
Невозможен тепловой вечный двигатель второго рода, т.е. двигатель, совершающий механическую работу за счет охлаждения какого-либо одного тела.