- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
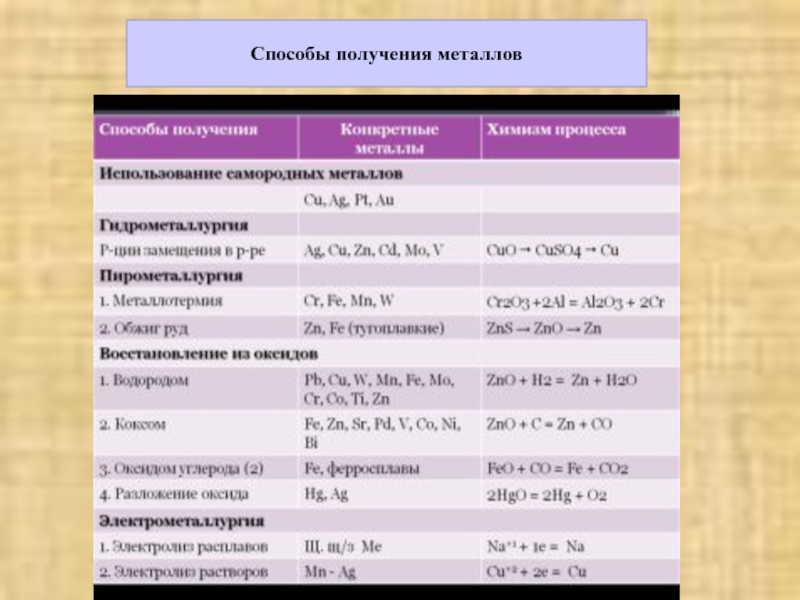
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад интегрированного урока Этот удивительный мир металлов
Содержание
- 1. Презентация интегрированного урока Этот удивительный мир металлов
- 2. ЦелиОбразовательныеВоспитательныеРазвивающиеРазвивать представления о причинно – следственных связях
- 3. Задачи:закрепить знания о свойствах металлов, способах
- 4. Слайд 4
- 5. Слайд 5
- 6. Ход занятияОрганизационный моментСтадия вызоваПостановка целиРаскрыть причину особых
- 7. . 1. Алхимики считали, что на
- 8. Стадия осмысления.Составляем с учащимися кластер в тетради
- 9. Слайд 9
- 10. Взаимодействие сурьма с хлоромВзаимодействие натрия с водойПолучение гидроксида железаОпыты с литиемЦветные химические реакцииМеталлы как химические элементы
- 11. Металлы в ПС в основном располагаются в левом нижнем углу.МЕТАЛЛЫМеталлы как химические элементы
- 12. Слайд 12
- 13. Металлы, как простые вещества.Формула простого вещества.
- 14. Металлическая связьМеталлическая связь
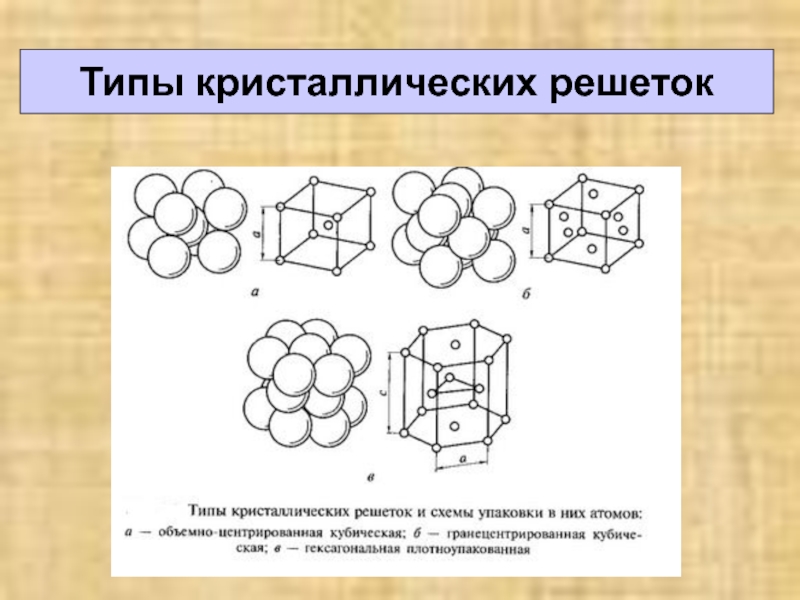
- 15. Типы кристаллических решеток
- 16. Физические свойства
- 17. Физические свойства металловМеталлыПластичность Au, Ag, Cu, Sn,
- 18. Слайд 18
- 19. Лабораторная работа 1. Две стеклянные пластинки накладывают
- 20. Лабораторная работа 2. Определение теплопроводности различных металловУчащиеся проводят эксперимент: нагревают гвоздь и алюминиевую фольгу.Практическая часть
- 21. Задание. Заполните пропуски нужными словами:1. Радиус атомов
- 22. Закончите уравнения возможных реакций:Na + H2O
- 23. Способы получения металлов
- 24. Применение. О применении металлов – небольшая мультимедийная
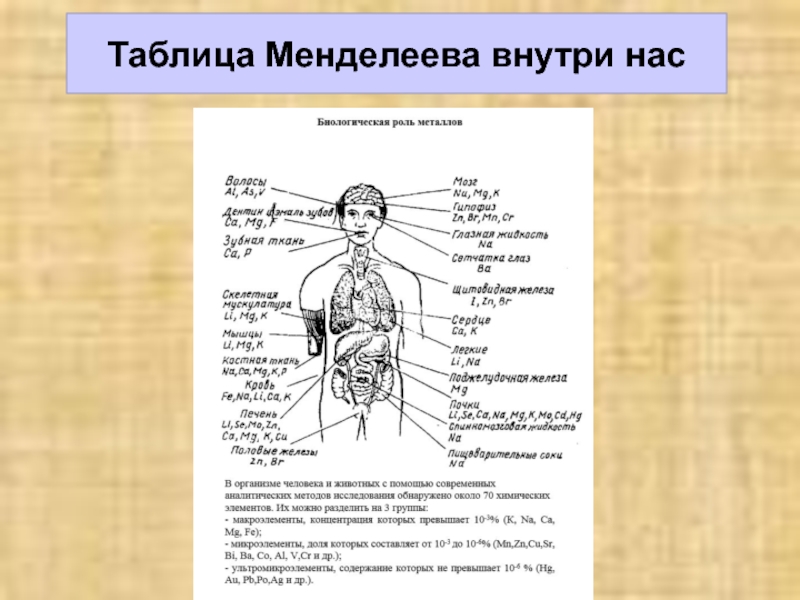
- 25. Таблица Менделеева внутри нас
- 26. Таблица Менделеева внутри нас
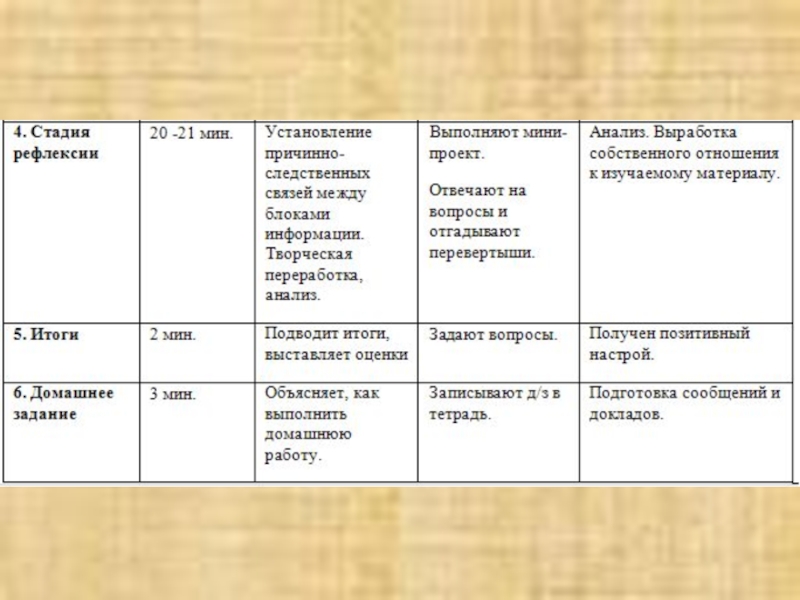
- 27. Стадия рефлексии.
- 28. Цель: Определение содержания металлов в продуктах питания?Объект
- 29. Нами были исследованы образцы следующих пищевых продуктов:
- 30. Перевертыши:1. Разговор – ртуть, крик – платина.
- 31. Подводим итог урока. Оцениваем работу учащихся, предлагаем домашнее задание.
- 32. Домашнее заданиеЗаполнить таблицу:Найдите дополнительную интересную и полезную
- 33. Источники:1. Венецкий С. И. Рассказы о металлах.
Слайд 1
Интегрированный урок по физике и химии
«Этот удивительный мир металлов»
«Металл – всех
(Джон Апдайк)
Авторы: Малык Т.К. – преподаватель
БОУ ЧР СПО ЧЭМК Хлебникова Л.А. - преподаватель БОУ ЧР СПО ЧЭМК
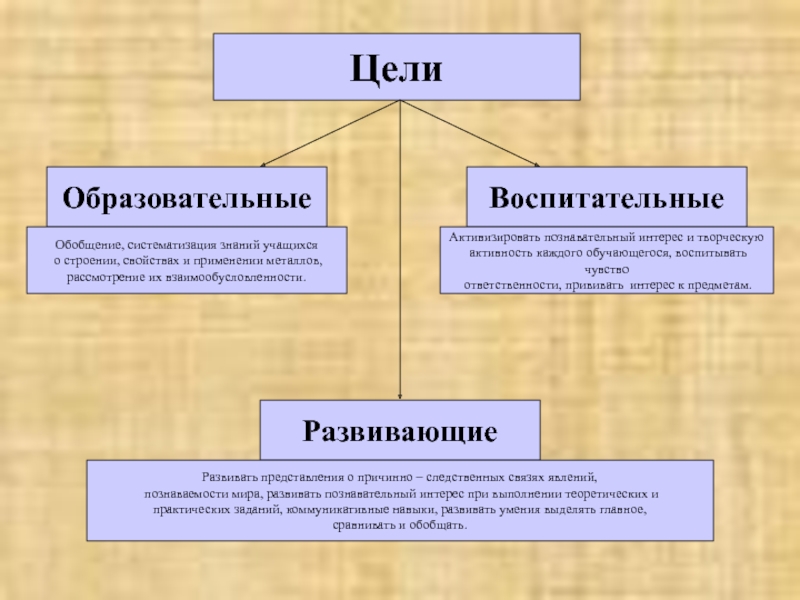
Слайд 2Цели
Образовательные
Воспитательные
Развивающие
Развивать представления о причинно – следственных связях явлений,
познаваемости мира, развивать
практических заданий, коммуникативные навыки, развивать умения выделять главное,
сравнивать и обобщать.
Обобщение, систематизация знаний учащихся
о строении, свойствах и применении металлов,
рассмотрение их взаимообусловленности.
Активизировать познавательный интерес и творческую
активность каждого обучающегося, воспитывать чувство
ответственности, прививать интерес к предметам.
Слайд 3 Задачи:
закрепить знания о свойствах металлов, способах получения, их нахождении в
развивать умения пользоваться опорными знаниями, закреплять умения и навыки выполнения физического и химического экспериментов;
развивать навыки научно-исследовательской работы учащихся, их творческой и деловой активности.
ЗАДАЧИ
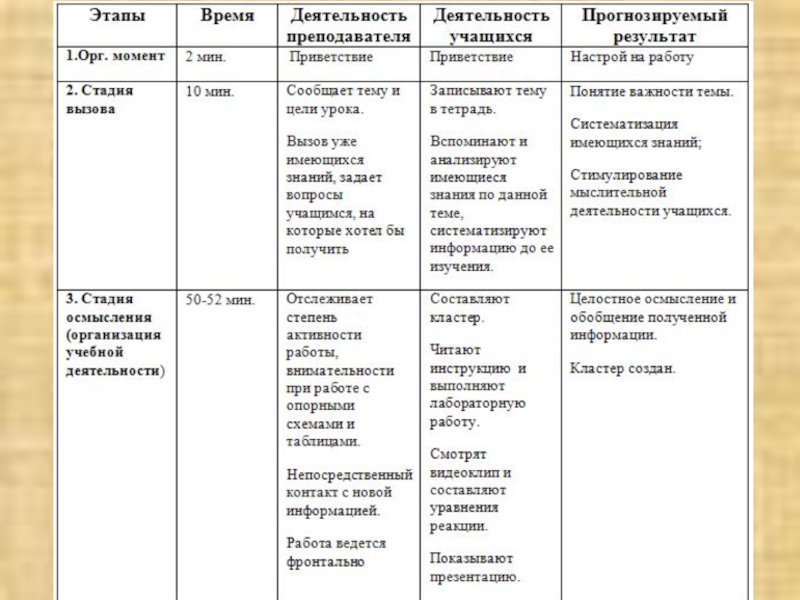
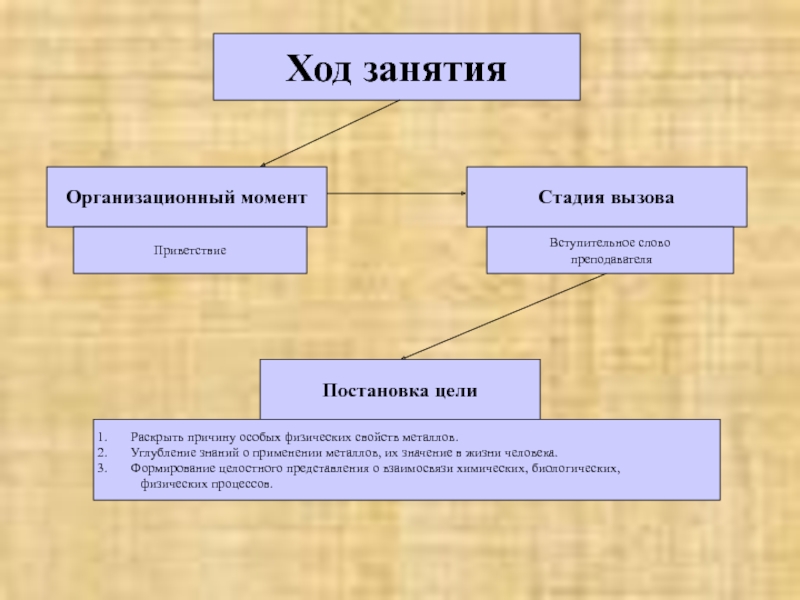
Слайд 6Ход занятия
Организационный момент
Стадия вызова
Постановка цели
Раскрыть причину особых физических свойств металлов.
Углубление знаний
Формирование целостного представления о взаимосвязи химических, биологических,
физических процессов.
Вступительное слово
преподавателя
Приветствие
Слайд 7.
1. Алхимики считали, что на небе 7 светил и каждое
2. Какой металл загорается в холодной воде?
3. Почему свежий разрез яблока на воздухе буреет?
4. Какой металл плавится от тепла человеческой руки?
5. Если бы существовал приз «за активность», то атомам какого из металлов вы бы его присудили?
6. Какой из металлов в глубокой древности называли «небесной медью» и почему?
7. Какое молоко не пьют?
8. От соединений каких металлов зависит красный цвет крови и зеленая окраска растений?
Стадия вызова. Блиц-опрос
Слайд 8Стадия осмысления.
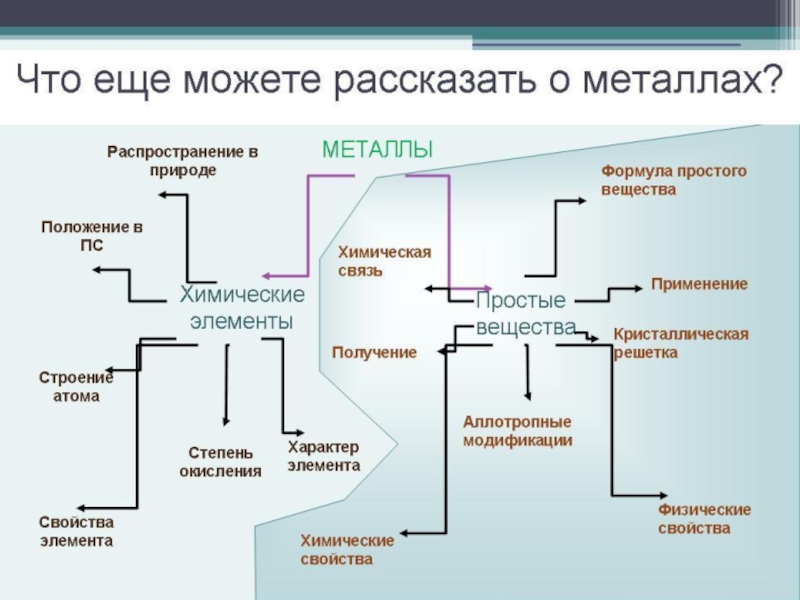
Составляем с учащимися кластер в тетради и на доске –
Работа с опорными конспектами и схемами
(Составление схемы «Общие свойства металлов»
Положение в периодической системе
Строение атома.
Слайд 10
Взаимодействие сурьма с хлором
Взаимодействие натрия с водой
Получение гидроксида железа
Опыты с литием
Цветные
Металлы как химические элементы
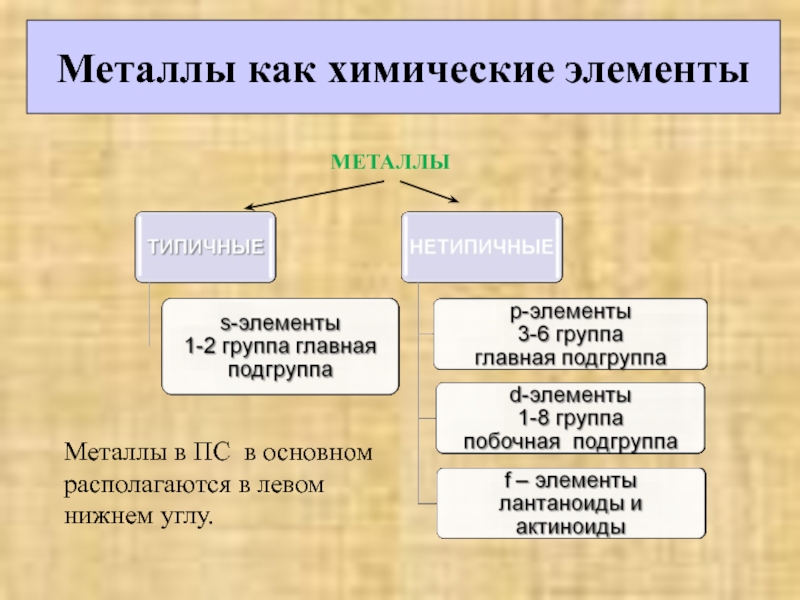
Слайд 11Металлы в ПС в основном располагаются в левом нижнем углу.
МЕТАЛЛЫ
Металлы как
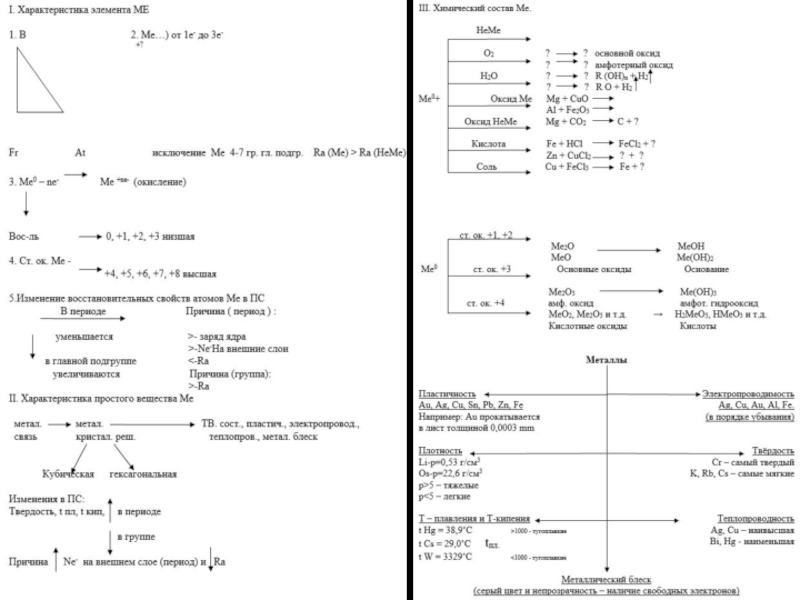
Слайд 17Физические свойства металлов
Металлы
Пластичность Au, Ag, Cu, Sn, Pb, Zn, Fe.
Например: Au
Электропроводимость Ag, Cu, Au, Al, Fe (в порядке убывания)
Плотность Li-p=0,53 г/см3 Os-p=22,6 г/см3 p>5 – тяжелые
p<5 – легкие
ТвёрдостьCr – самый твердый K, Rb, Cs – самые мягкие
T – плавления и T-кипения Hg = 38,9˚C t >1000 – тугоплавкие
t Cs = 29,0˚C tпл. t W = 3329˚C t <1000 – легкоплавкие
Теплопроводность Ag, Cu – наивысшая Bi, Hg – наименьшая
Металлический блеск(серый цвет и непрозрачность – наличие свободных электронов)
Физические свойства металлов
Слайд 18
которое на огне плавить и
холодное
ковать можно»
М.В.Ломоносов о металлах
Слайд 19
Лабораторная работа 1. Две стеклянные пластинки накладывают друг на друга. Их
Практическая часть
Слайд 20
Лабораторная работа 2. Определение теплопроводности различных металлов
Учащиеся проводят эксперимент: нагревают гвоздь
Практическая часть
Слайд 21Задание.
Заполните пропуски нужными словами:
1. Радиус атомов металлов ……………
2. При комнатной температуре металлы находятся в ……………. . агрегатном состоянии, за исключением ……………. .
3. Они хорошо проводят …………… . и ……………….. .
4. Самый тяжелый металл ……………, самый легкий ………………., самый тугоплавкий …………………, самый легкоплавкий …………… .
Слайд 22Закончите уравнения возможных реакций:
Na + H2O =
Ag + H2O = Zn + HCl =
Zn + CuSO4 = Na + Cl2 =
Cu + AgNO3 = Al + ZnCl2 =
Слайд 24Применение.
О применении металлов – небольшая мультимедийная презентация, подготовленная учащимися.
- История
- Металл в быту человека вчера и сегодня.
- Биологическая роль металлов.
- Металлы в художественном творчестве.
- Роль металлов в производстве.
- Применении металлов, их значении в жизни растений, животных и человека.
Применение.
Слайд 28Цель: Определение содержания металлов в продуктах питания?
Объект исследования: печень говяжья (сырая),
Предмет исследования Последствия воздействия роданида калия (окрашивание) на объект исследования.
Гипотеза Роданид калия приводит к появлению ярко-красной окраски при наличии ионов Fe2+ и Fe3+.
Задача: провести химический эксперимент, в ходе которого выявить наличие ионов железа в печени говяжьей, в гречневой и рисовой муке.
Слайд 29Нами были исследованы образцы следующих пищевых продуктов: печень говяжья (сырая), мука
Вывод: железо содержится в продуктах питания (печень, гречневая мука). Отсутствие положительной реакции при обнаружении железа в муке рисовой можно объяснить маленьким % содержанием железа в данном образце.
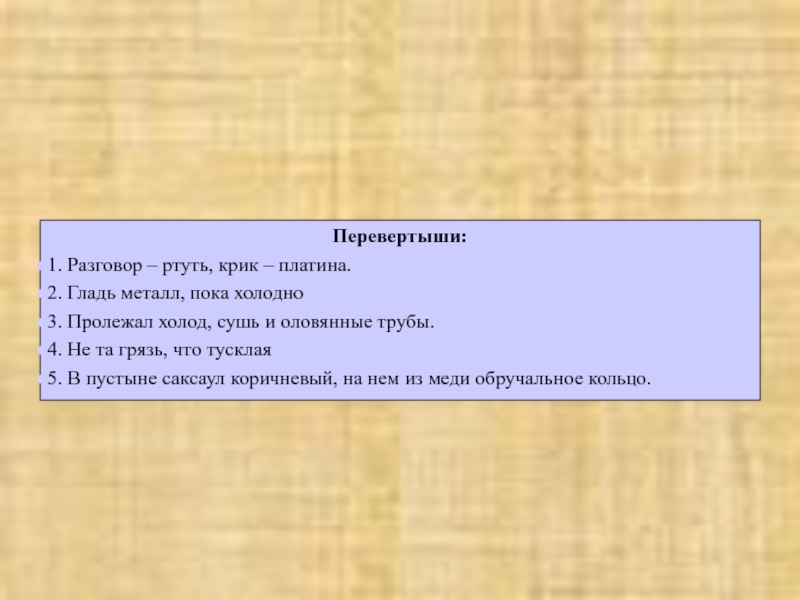
Слайд 30Перевертыши:
1. Разговор – ртуть, крик – платина.
2. Гладь металл, пока
3. Пролежал холод, сушь и оловянные трубы.
4. Не та грязь, что тусклая
5. В пустыне саксаул коричневый, на нем из меди обручальное кольцо.
Слайд 32Домашнее задание
Заполнить таблицу:
Найдите дополнительную интересную и полезную информацию по теме (пословицы,
Слайд 33Источники:
1. Венецкий С. И. Рассказы о металлах. – М.: Металлургия, 1982
2.
3. Рудзитис Г.Е., Фельдман Ф.Г. Химия. 9 класс.- М.: Просвещение,2009
4. Фадеев Г.Н., Сычев А.П. Мир металлов и сплавов. Книга для внеклассного чтения. – М.: Просвещение, 1997
5. Шерстобоева О.Б. «Мир металлов глазами химика, физика и биолога» Химия в школе №2 2004
6. Энциклопедический словарь юного химика. – М.: Педагогика, 1992
7. Энциклопедический словарь юного химика. – М.: Педагогика, 1992
8. http://all-met.narod.ru/
9. http://elementy.ru/