- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад для 10 класса Основы молекулярно-кинетической теории
Содержание
- 1. Презентация для 10 класса Основы молекулярно-кинетической теории
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
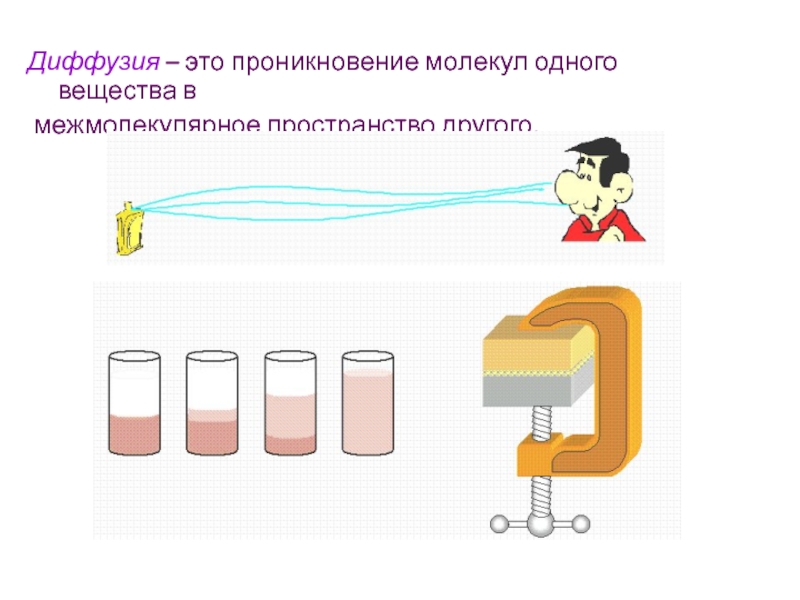
- 5. Диффузия – это проникновение молекул одного вещества в межмолекулярное пространство другого.
- 6. Причина: удары молекул жидкости о частицу
- 7. Слайд 7
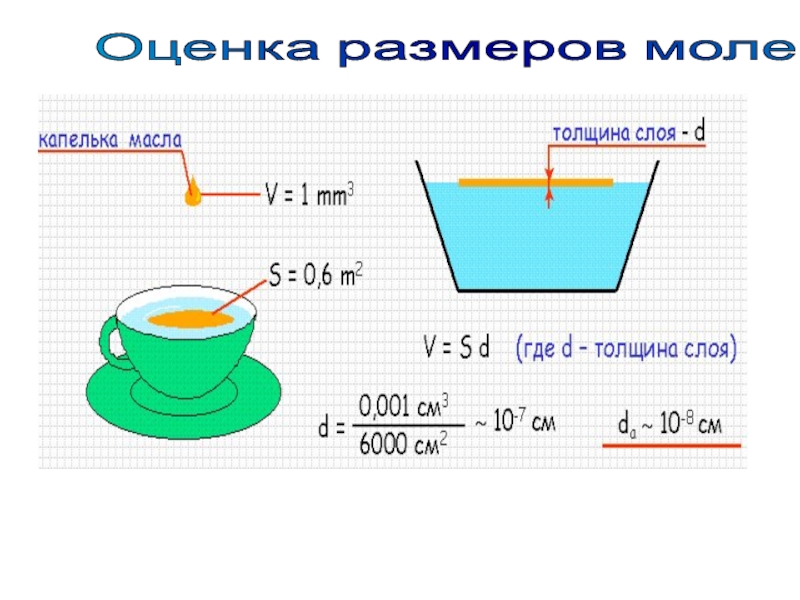
- 8. Оценка размеров молекул
- 9. Число молекул Подсчитаем приблизительное число молекул в
- 10. Масса молекулы Вычислим массу одной молекулы воды.В 1 г воды содержится 3,7·1022 молекул.
- 11. Относительная молекулярная масса Относительной молекулярной (или атомной)
- 12. Постоянная Авогадро Один моль – это количество
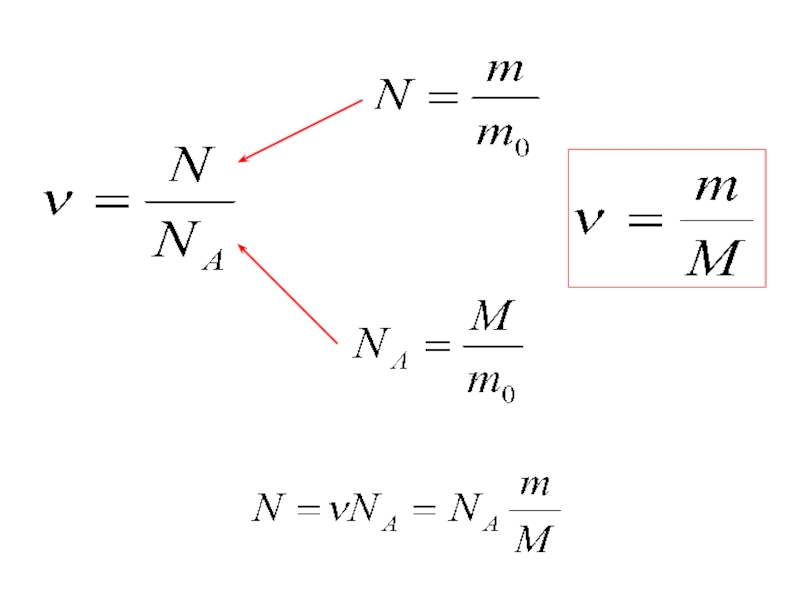
- 13. Количество вещества ν равно отношению числа молекул
- 14. Молярная масса Молярной массой М вещества называют
- 15. Слайд 15
- 16. Слайд 16
Слайд 1Молекулярная физика.
Основные положения молекулярно-
кинетической теории (МКТ)
Размеры молекул.
Масса молекул. Количество вещества
Диффузия.
Слайд 6Причина: удары молекул жидкости
о частицу не компенсируют друг друга
Характер движения
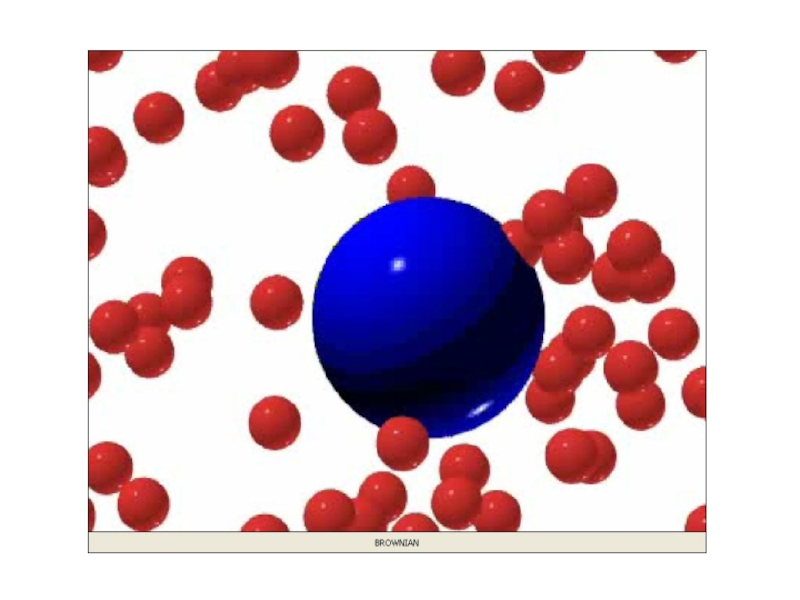
Броуновское движение- это беспорядочное непрерывное движение мельчайших, взвешенных в жидкости или газе частиц твердого тела под ударами молекул жидкости или газа
Характер движения зависит от вида жидкости,
размера и формы частиц, температуры.
Характер движения зависит от вида жидкости, размера и формы частиц, температуры.
Р. Броун 1827 г.
Слайд 9Число молекул
Подсчитаем приблизительное число молекул в капле воды массой 1
Слайд 11Относительная молекулярная масса
Относительной молекулярной (или атомной) массой вещества Мr называют
Mr (Н2О)= 2·1+16=18 а.е.м.
Вычислим Mr воды Н2О (для этого воспользуемся таблицей Менделеева)
Атомная единица массы (а.е.м.) ≈ 1,66·10-27 кг
Слайд 12Постоянная Авогадро
Один моль – это количество вещества, в котором содержится
1 моль любого вещества содержится одно и то же число атомов или молекул. Это число атомов обозначают NA и называют постоянной Авогадро в честь итальянского ученого (XIX в.).
NA = 6·1023 моль-1
Слайд 13Количество вещества ν равно отношению числа молекул N в данном теле
Количество вещества
Слайд 14Молярная масса
Молярной массой М вещества называют массу вещества, взятого в
M = m0NA
Масса т любого количества вещества равна произведению массы одной молекулы на число молекул в теле:
m = m0N