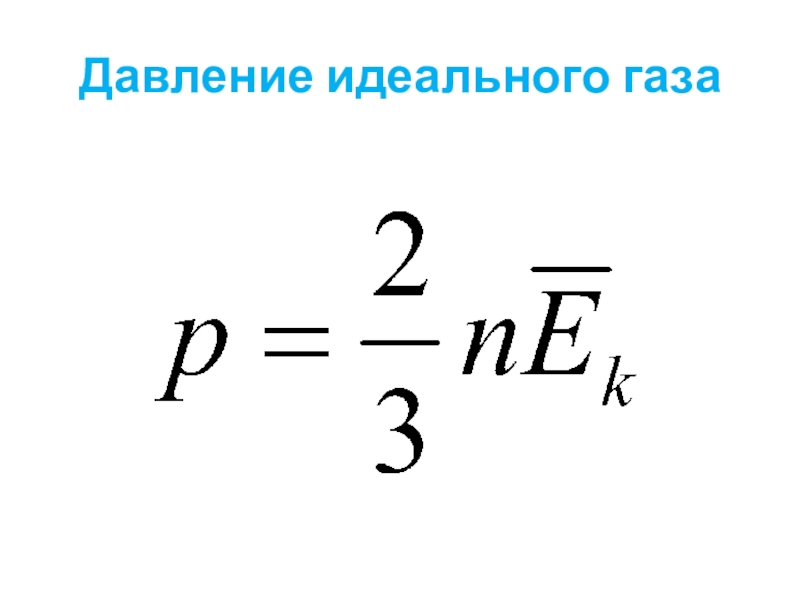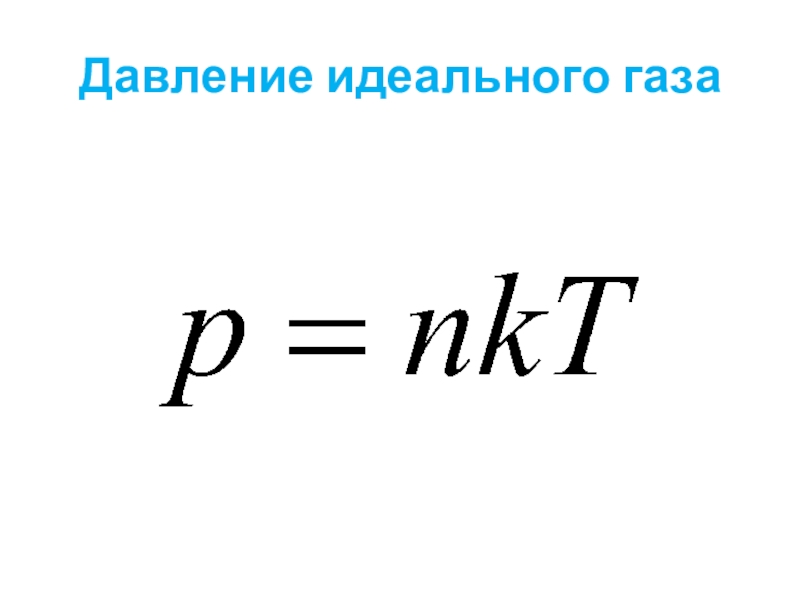- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Материалы к уроку: Идеальный газ
Содержание
- 1. Материалы к уроку: Идеальный газ
- 2. Идеальный газа) Собственный объем молекул газа пренебрежимо
- 3. Основное уравнение молекулярно-кинетической теории идеального газа
- 4. Давление идеального газа
- 5. Давление идеального газа
- 6. Средняя кинетическая энергия
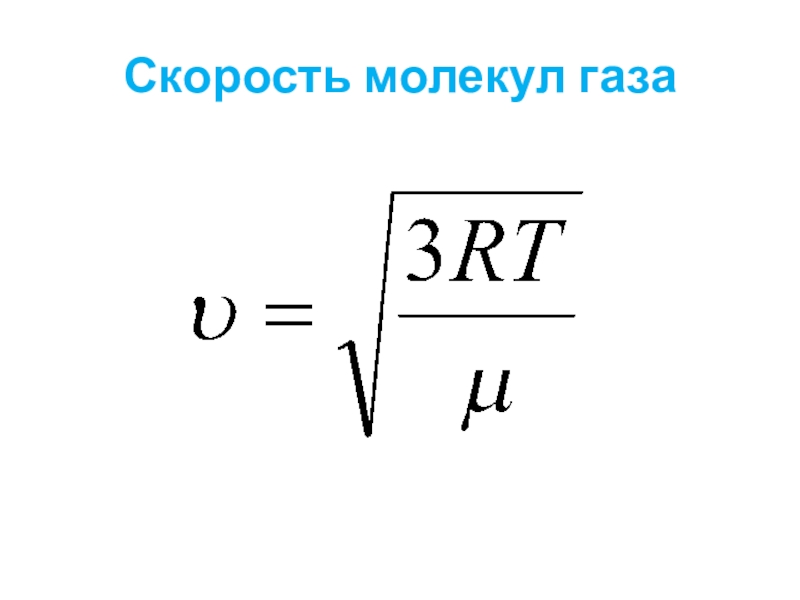
- 7. Скорость молекул газа
- 8. Распределение Максвелла молекул идеального газа по скоростям Вид
- 9. Термодинамические параметры параметры состояниятемпература, плотность, давление, объем,
- 10. Уравнение Менделеева - Клапейрона Физическое состояние массы газа
- 11. Уравнение Менделеева – КлапейронаУравнение состояния позволяет определить
- 12. Газовые законы Газовыми законами называются количественные зависимости между двумя макроскопическими параметрами при фиксированном значении третьего параметра
- 13. Изопроцессы Изопроце́ссы — термодинамические процессы, во время которых количество вещества
- 14. Изопроцессы
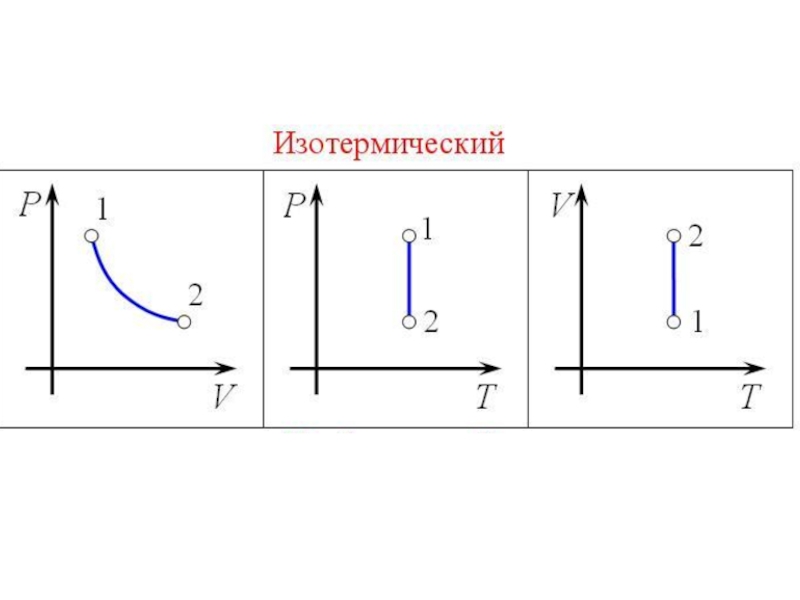
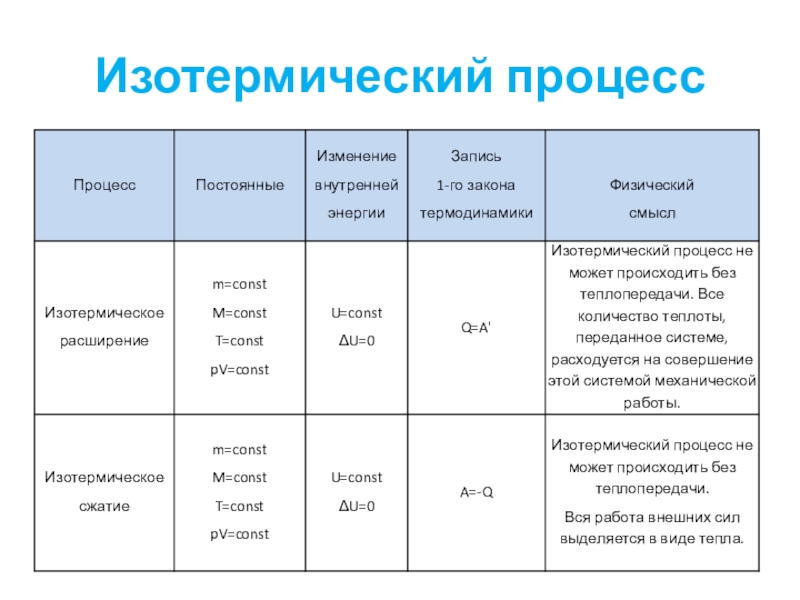
- 15. Изотермический процесс
- 16. Слайд 16
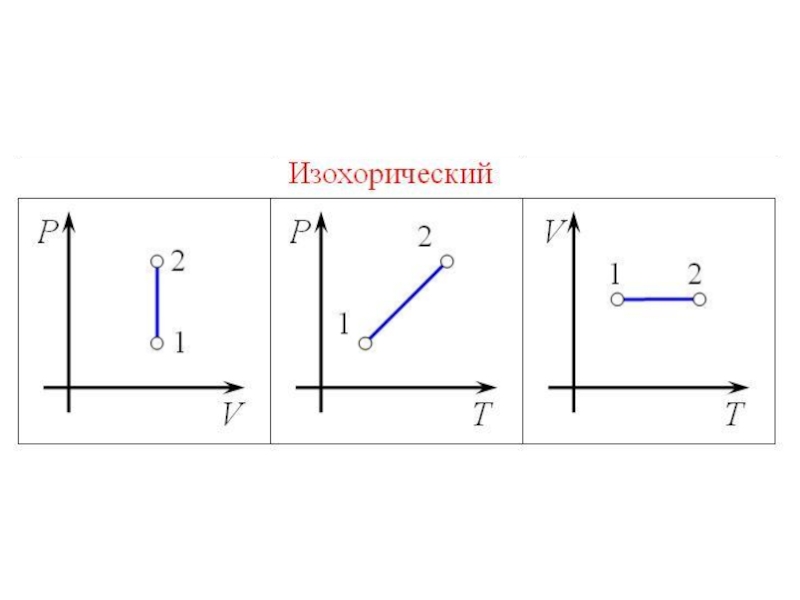
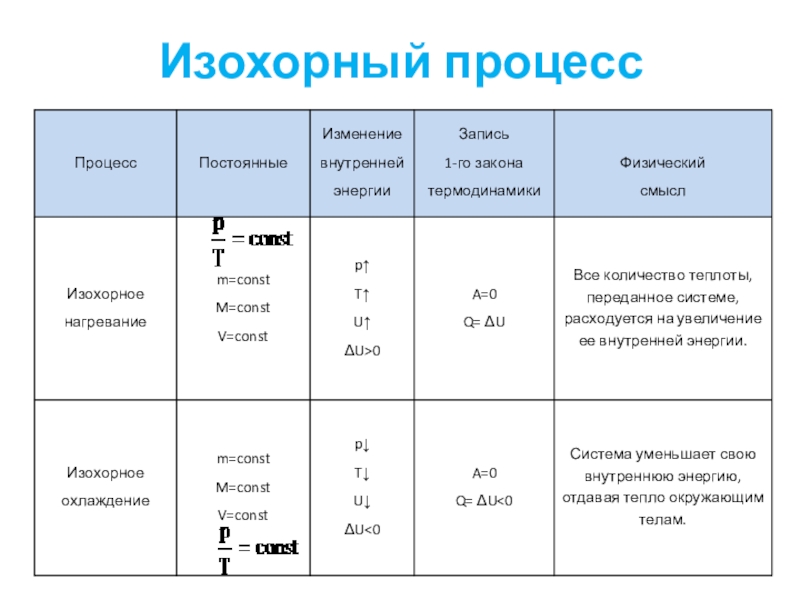
- 17. Изохорный процесс
- 18. Слайд 18
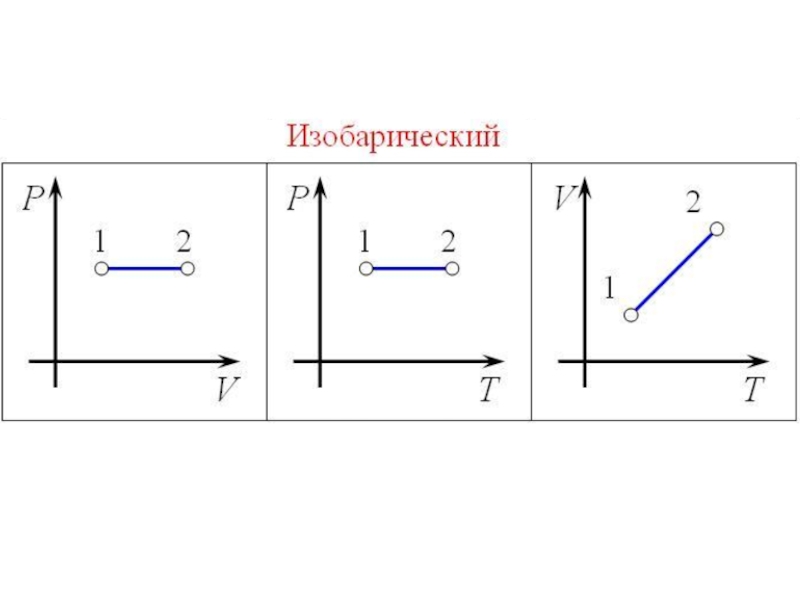
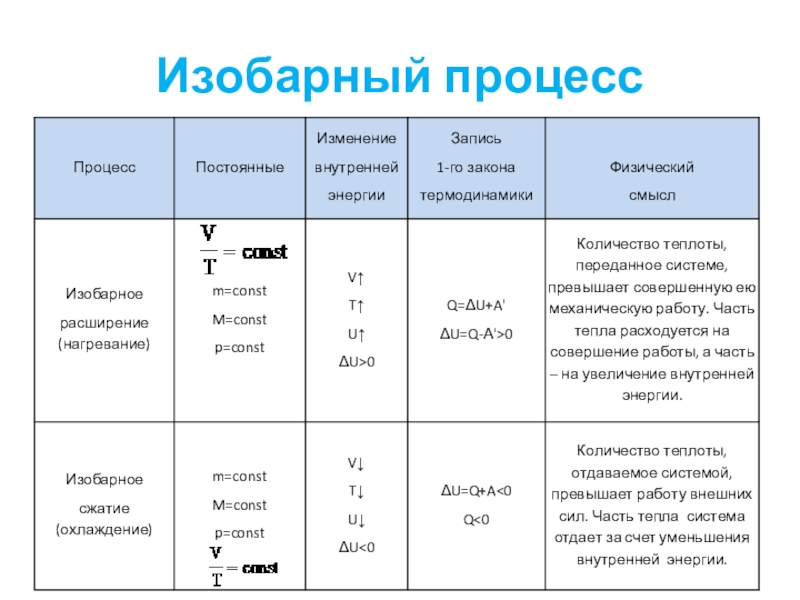
- 19. Изобарный процесс
- 20. Слайд 20
- 21. Термодинамика
- 22. Внутренняя энергия
- 23. Способы изменения внутренней энергииВнутреннюю энергию можно
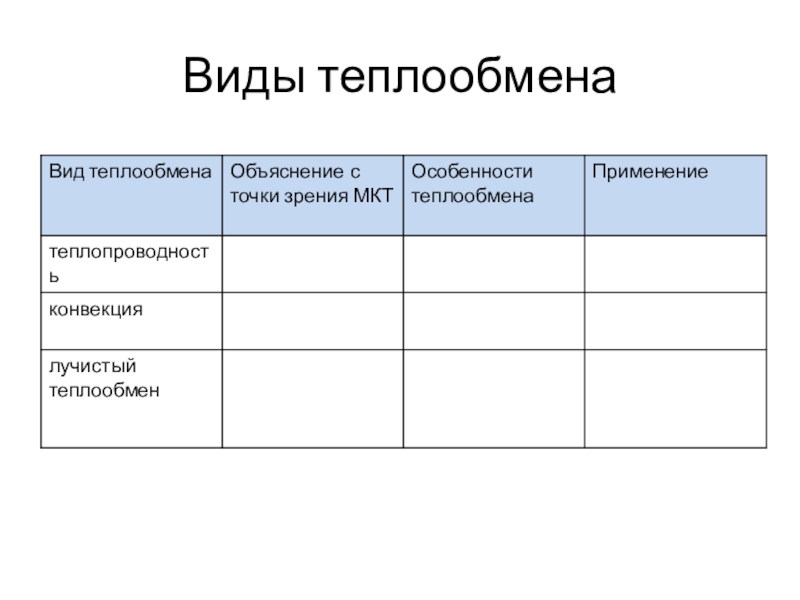
- 24. Виды теплообменаТеплопроводностьКонвекцияЛучистые теплообмен
- 25. Виды теплообмена
- 26. ТеплопроводностьТеплопроводность - это способ теплопередачи, при котором
- 27. ОсобенностиМожет происходить в твердых, жидких газообразных веществах;Лучше
- 28. КонвекцияКонвекция - это способ теплопередачи, при котором тепло передается от нагревателя восходящими струями газа
- 29. Особенности Конвекция может наблюдаться только в жидкостях и
- 30. Лучистый теплообменЛучистый теплообмен - это способ передачи тепла от нагревателя посредством испускания лучей.
- 31. ОсобенностиЧем выше температура источника тепла, тем излучение
- 32. Термодинамика В основе термодинамики лежат 3 фундаментальных закона,
- 33. Нулевое (или общее) начало термодинамики Замкнутая система независимо
- 34. Первое начало термодинамики Закон сохранения энергии в применении
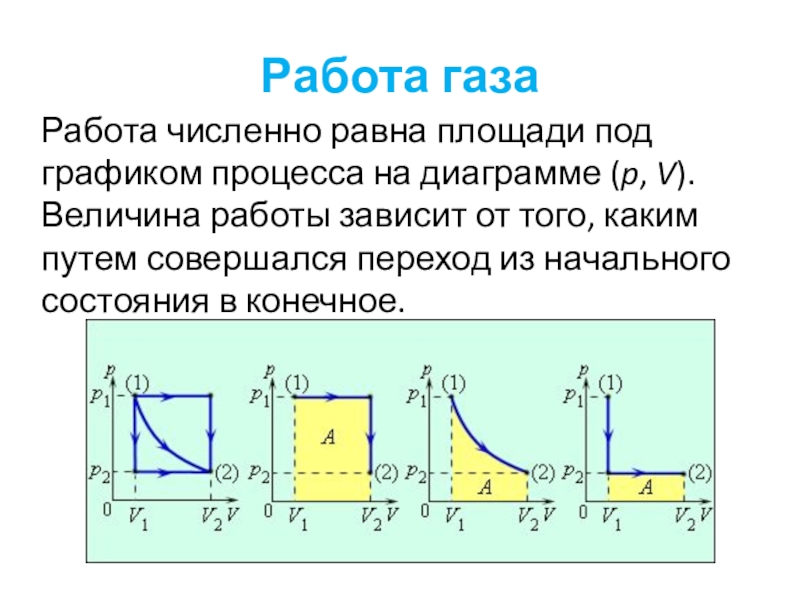
- 35. Работа газа
- 36. Работа газаРабота численно равна площади под графиком
- 37. Количество теплотыКоличество теплоты- количественная мера изменения внутренней энергии при теплообмене
- 38. Количество теплоты
- 39. Второе начало термодинамики Накладывает ограничения на направление термодинамических
- 40. Необратимость процессов в природе
- 41. Применение первого закона термодинамики к изопроцессам
- 42. Изотермический процесс
- 43. Изохорный процесс
- 44. Изобарный процесс
- 45. Спасибо за внимание.
Идеальный газа) Собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда (разреженность).б) Между молекулами отсутствуют силы взаимодействия.в) Столкновение молекул газа между собой и со стенками сосуда абсолютно упругие.
Слайд 2Идеальный газ
а) Собственный объем молекул газа пренебрежимо мал по сравнению с
объемом сосуда (разреженность).
б) Между молекулами отсутствуют силы взаимодействия.
в) Столкновение молекул газа между собой и со стенками сосуда абсолютно упругие.
б) Между молекулами отсутствуют силы взаимодействия.
в) Столкновение молекул газа между собой и со стенками сосуда абсолютно упругие.
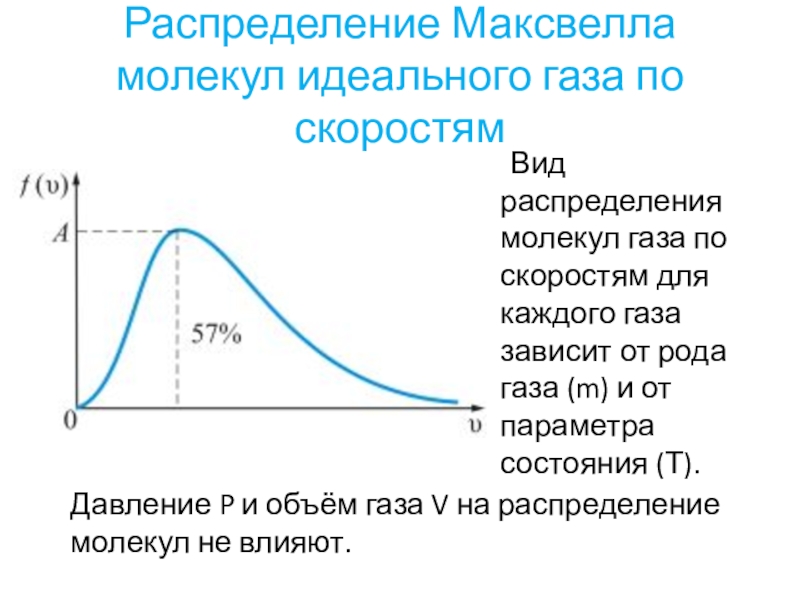
Слайд 8Распределение Максвелла молекул идеального газа по скоростям
Вид распределения молекул газа по
скоростям для каждого газа зависит от рода газа (m) и от параметра состояния (Т).
Давление P и объём газа V на распределение молекул не влияют.
Слайд 9Термодинамические параметры
параметры состояния
температура, плотность, давление, объем, удельное электрическое сопротивление и другие
физические величины:
- однозначно определяющие термодинамическое состояние системы;
- не учитывающие молекулярное строение тел;
- описывающие макроскопическое строение тел.
Слайд 10Уравнение Менделеева - Клапейрона
Физическое состояние массы газа определяется тремя термодинамическими параметрами:
давлением р, объемом V и температурой Т.
Между этими параметрами существует определенная связь, называемая уравнением состояния
Между этими параметрами существует определенная связь, называемая уравнением состояния
Слайд 11Уравнение Менделеева – Клапейрона
Уравнение состояния позволяет определить одну из величин, если
известны две другие
Зная уравнение состояния можно предсказать как будет протекать процесс при определенных внешних условиях
Зная уравнение состояния можно определить, как меняется состояние системы, если она совершает работу или получает теплоту от окружающих тел.
Зная уравнение состояния можно предсказать как будет протекать процесс при определенных внешних условиях
Зная уравнение состояния можно определить, как меняется состояние системы, если она совершает работу или получает теплоту от окружающих тел.
Слайд 12Газовые законы
Газовыми законами называются количественные зависимости между двумя макроскопическими параметрами при
фиксированном значении третьего параметра
Слайд 13Изопроцессы
Изопроце́ссы — термодинамические процессы, во время которых количество вещества и ещё одна из
физических величин — параметров состояния: давление, объём, температура — остаются неизменными
Слайд 23Способы изменения
внутренней энергии
Внутреннюю энергию можно изменить:
За счет совершения механической
работы над телом
Без совершения работы – теплообмен
Без совершения работы – теплообмен
Слайд 26Теплопроводность
Теплопроводность - это способ теплопередачи, при котором тепло передается от более
нагретой части тела, к менее нагретым, без перемещения вещества.
Слайд 27Особенности
Может происходить в твердых, жидких газообразных веществах;
Лучше всего проводят тепло твердые
тела, а из твердых – металлы;
Газы проводят тепло хуже чем жидкости;
Чем выше температура нагревателя, тем быстрее передается тепло от одной части тела к другой.
Газы проводят тепло хуже чем жидкости;
Чем выше температура нагревателя, тем быстрее передается тепло от одной части тела к другой.
Слайд 28Конвекция
Конвекция - это способ теплопередачи, при котором тепло передается от нагревателя
восходящими струями газа
Слайд 29Особенности
Конвекция может наблюдаться только в жидкостях и газах;
Конвекция происходит быстрее в
газах, чем в жидкостях при прочих равных условиях;
Чем больше площадь поверхности нагретого тела, тем больше жидкости или газа вовлекается в процесс конвекции;
Чем выше температура нагревателя, тем интенсивнее конвекция.
Чем больше площадь поверхности нагретого тела, тем больше жидкости или газа вовлекается в процесс конвекции;
Чем выше температура нагревателя, тем интенсивнее конвекция.
Слайд 30Лучистый теплообмен
Лучистый теплообмен - это способ передачи тепла от нагревателя посредством
испускания лучей.
Слайд 31Особенности
Чем выше температура источника тепла, тем излучение больше;
Чем больше площадь поверхности,
тем больше энергии излучает тело при прочих равных условиях;
При одинаковых температурах и площадях поверхности излучает больше тот нагреватель, который имеет черную поверхность;
Излучение может распространяться в твердых, жидких и газообразных средах, а также в вакууме.
При одинаковых температурах и площадях поверхности излучает больше тот нагреватель, который имеет черную поверхность;
Излучение может распространяться в твердых, жидких и газообразных средах, а также в вакууме.
Слайд 32Термодинамика
В основе термодинамики лежат 3 фундаментальных закона, называемых началами термодинамики, установленных
на основании обобщения большой совокупности опытных фактов.
Слайд 33Нулевое (или общее) начало термодинамики
Замкнутая система независимо от начального состояния в
конце концов приходит к состоянию термодинамического равновесия и самостоятельно выйти из него не может.
Слайд 34Первое начало термодинамики
Закон сохранения энергии в применении к термодинамическим системам.
Количество теплоты,
полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил
Слайд 36Работа газа
Работа численно равна площади под графиком процесса на диаграмме (p,
V). Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное.
Слайд 37Количество теплоты
Количество теплоты- количественная мера изменения внутренней энергии при теплообмене
Слайд 39Второе начало термодинамики
Накладывает ограничения на направление термодинамических процессов, запрещая самопроизвольную передачу
тепла от менее нагретых тел к более нагретым.