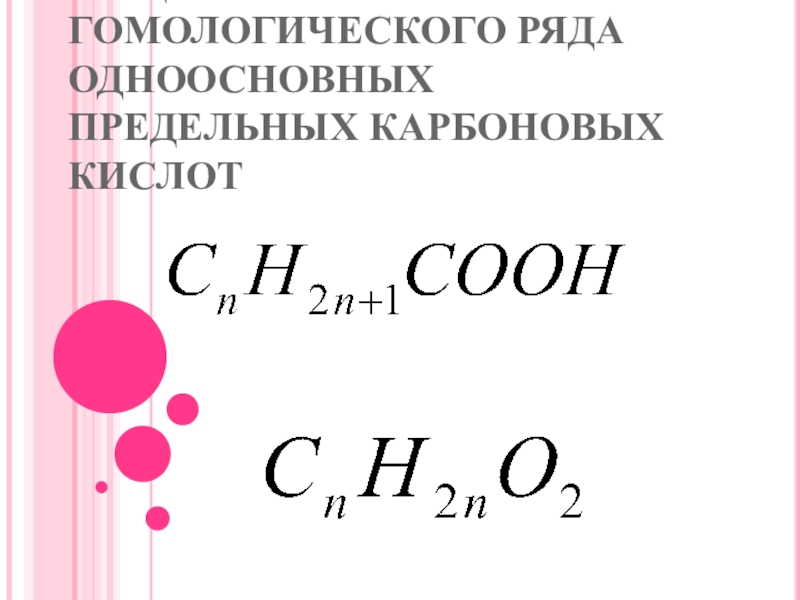- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии на тему Карбоновые кислоты
Содержание
- 1. Презентация к уроку химии на тему Карбоновые кислоты
- 2. Слайд 2
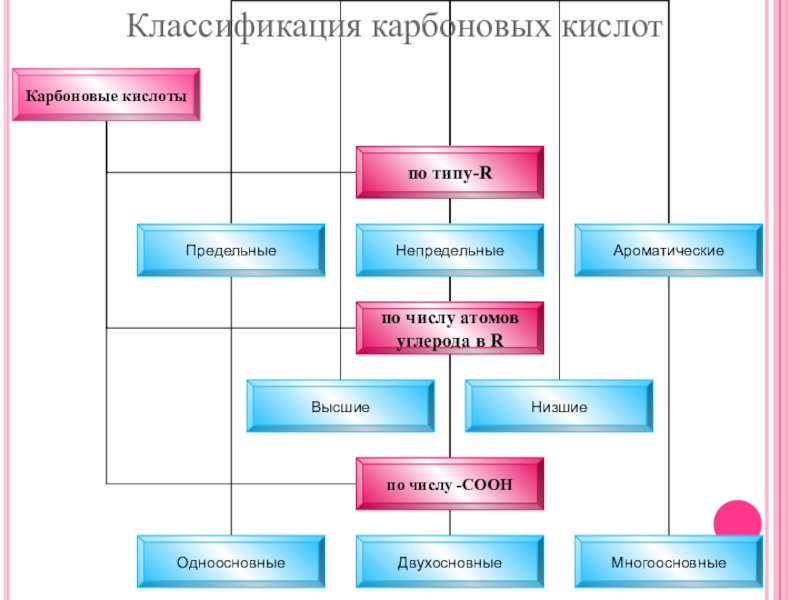
- 3. Классификация карбоновых кислот
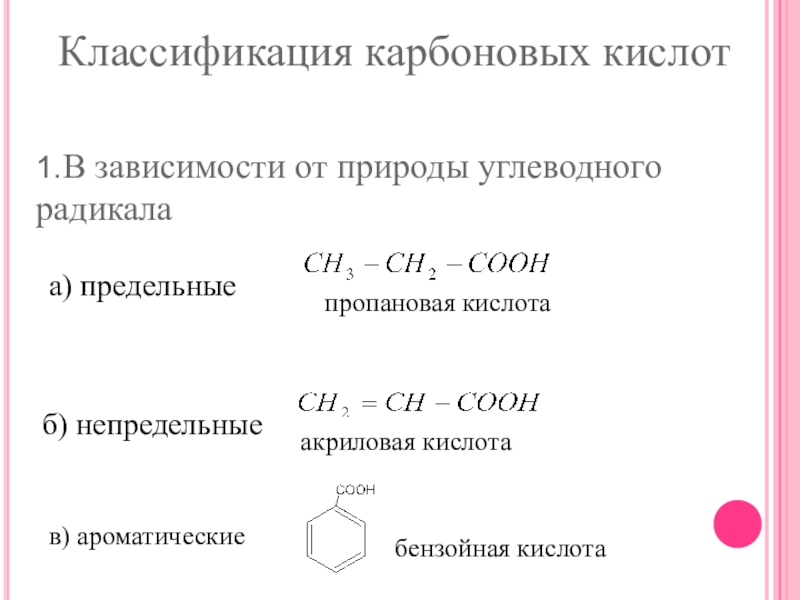
- 4. 1.В зависимости от природы углеводного радикалаа) предельныеб) непредельныепропановая кислотаакриловая кислотав) ароматическиебензойная кислотаКлассификация карбоновых кислот
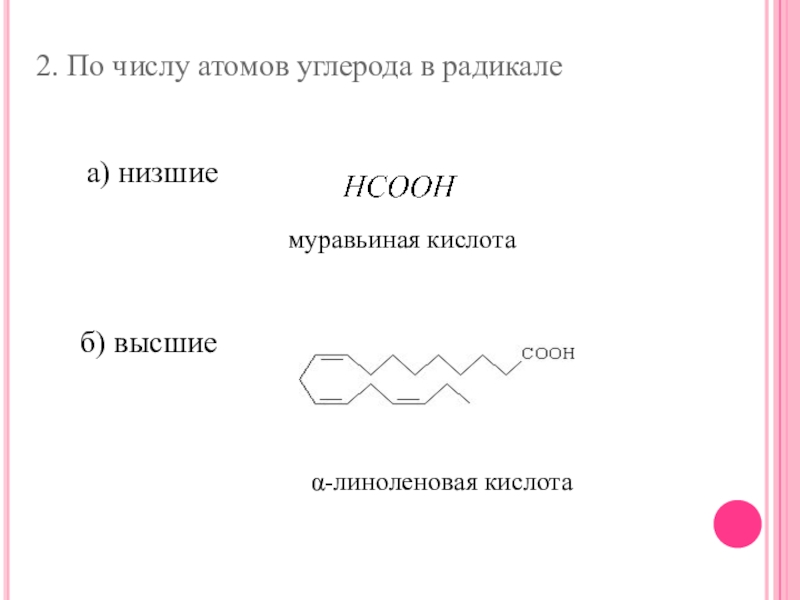
- 5. 2. По числу атомов углерода в радикалеа) низшиемуравьиная кислотаб) высшиеα-линоленовая кислота
- 6. 3. По количеству карбоксильных групп
- 7. ОБЩАЯ ФОРМУЛА ГОМОЛОГИЧЕСКОГО РЯДА ОДНООСНОВНЫХ ПРЕДЕЛЬНЫХ КАРБОНОВЫХ КИСЛОТ
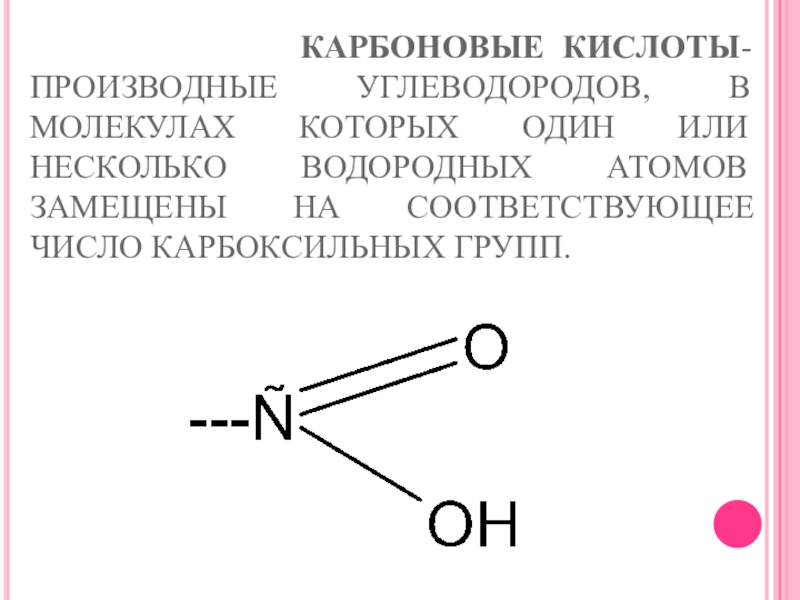
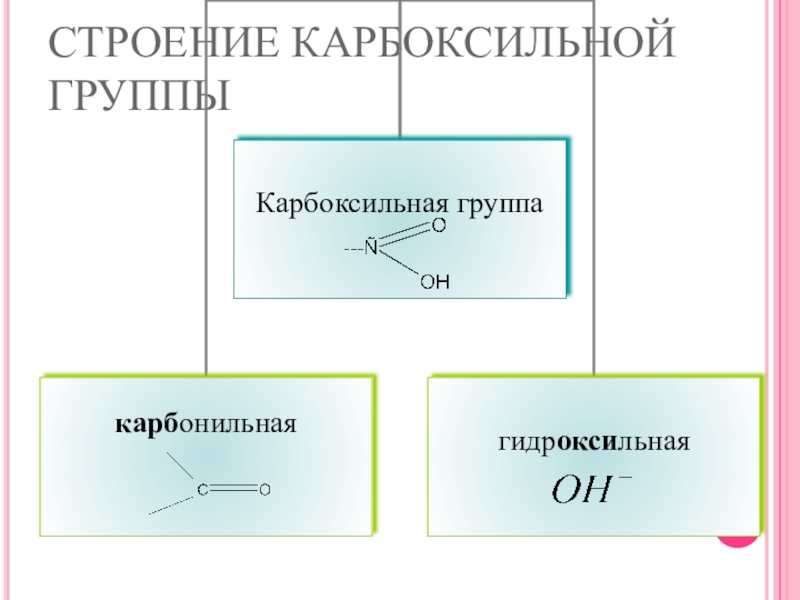
- 8. СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ
- 9. МЕЗОМЕРНЫЙ ЭФФЕКТ КАРБОКСИЛЬНОЙ ГРУППЫδ+ δ-
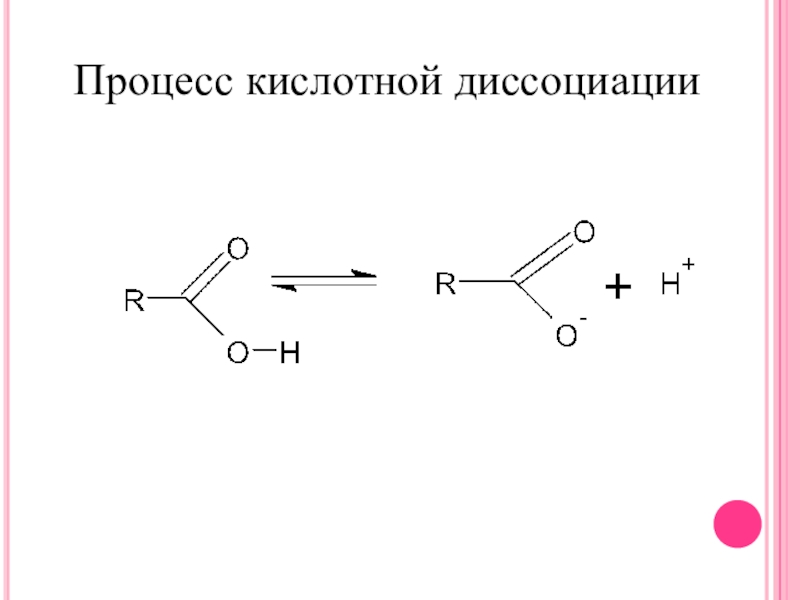
- 10. Процесс кислотной диссоциации
- 11. ИНДУКТИВНЫЙ ЭФФЕКТ КАРБОКСИЛЬНОЙ ГРУППИРОВКИ δ+ δ- - I индуктивный эффектЭлектроноакцепторные заместителиHal, NO2-, OH-, C6H5-, CH2=CH-.
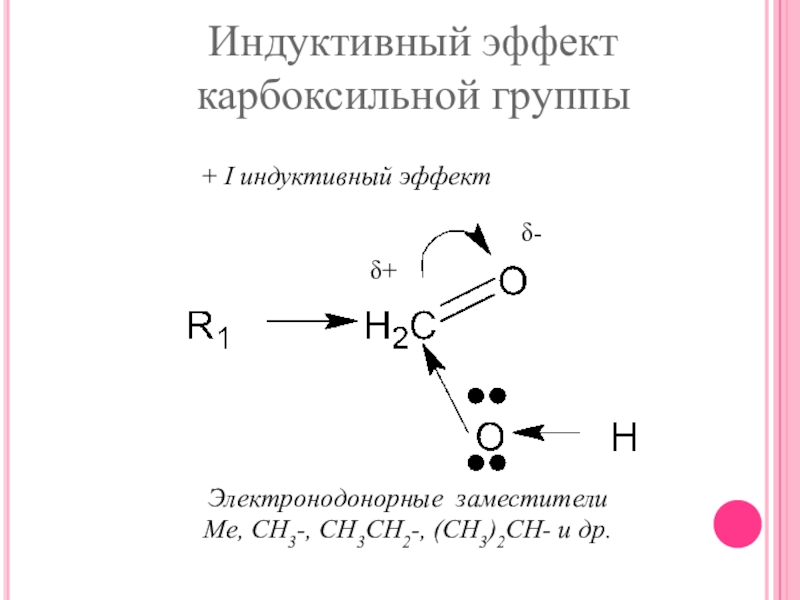
- 12. δ+ δ- + I индуктивный эффектЭлектронодонорные заместителиMe, CH3-, CH3CH2-, (CH3)2CH- и др.Индуктивный эффект карбоксильной группы
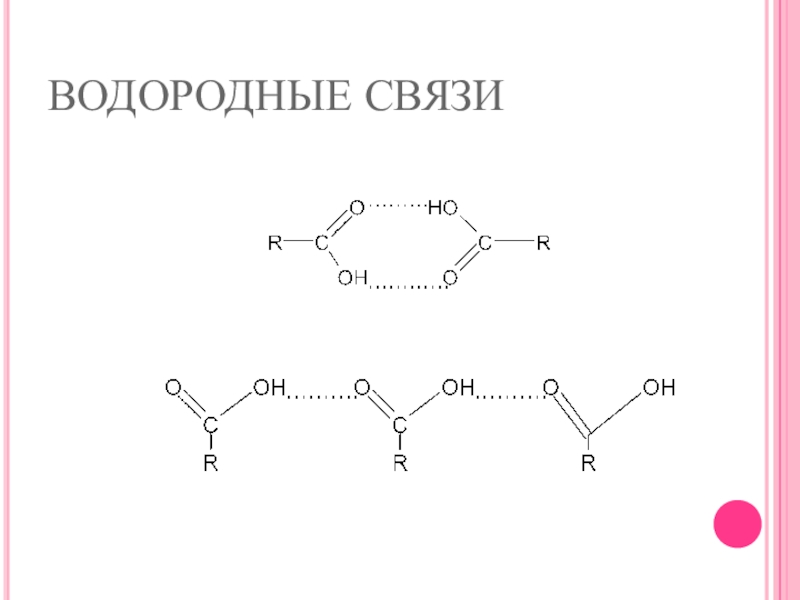
- 13. ВОДОРОДНЫЕ СВЯЗИ
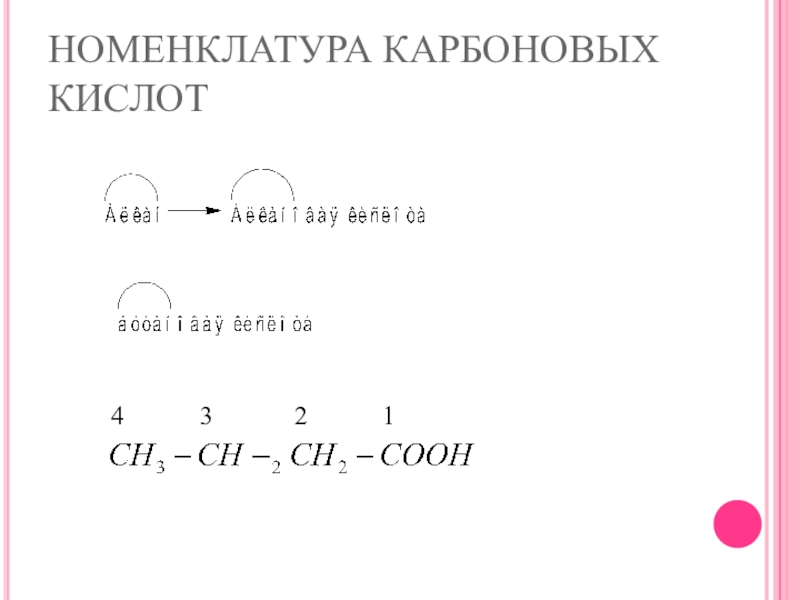
- 14. НОМЕНКЛАТУРА КАРБОНОВЫХ КИСЛОТ1234
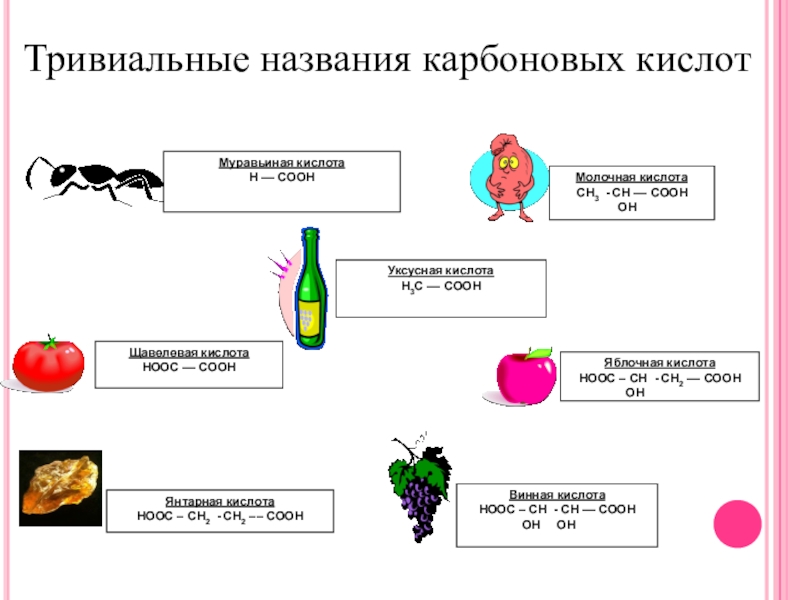
- 15. Тривиальные названия карбоновых кислот
- 16. Изомерия карбоновых кислот
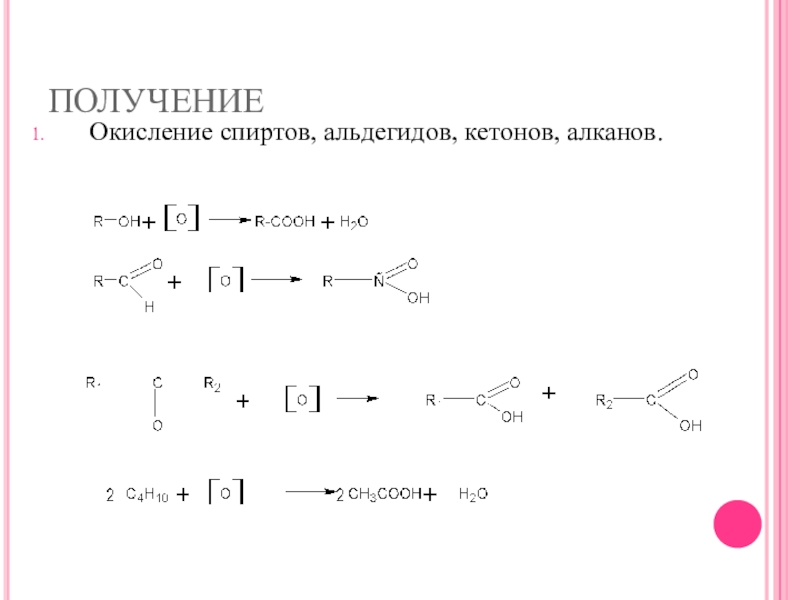
- 17. ПОЛУЧЕНИЕОкисление спиртов, альдегидов, кетонов, алканов.
- 18. 2. ГИДРОЛИЗ НИТРИЛОВ3. Гидролиз тригалогенпроизводных
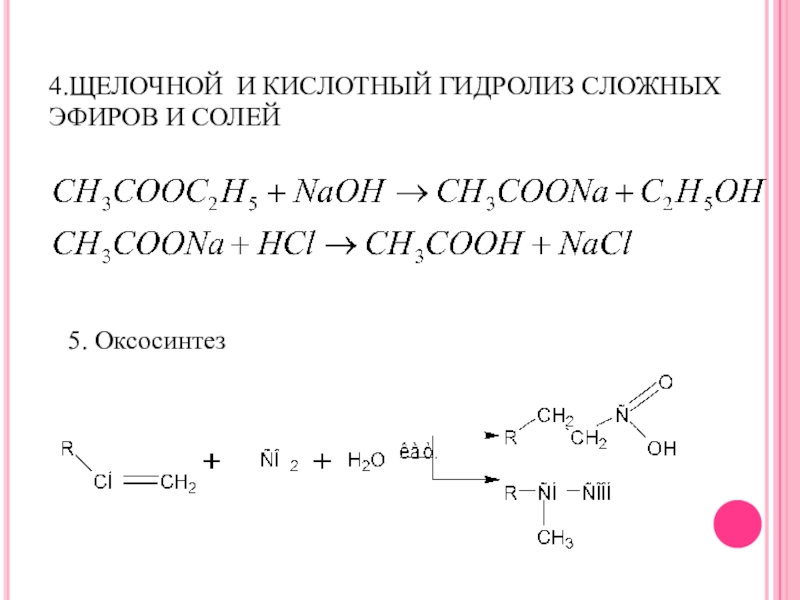
- 19. 4.ЩЕЛОЧНОЙ И КИСЛОТНЫЙ ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ И СОЛЕЙ5. Оксосинтез
- 20. Особенности строения и
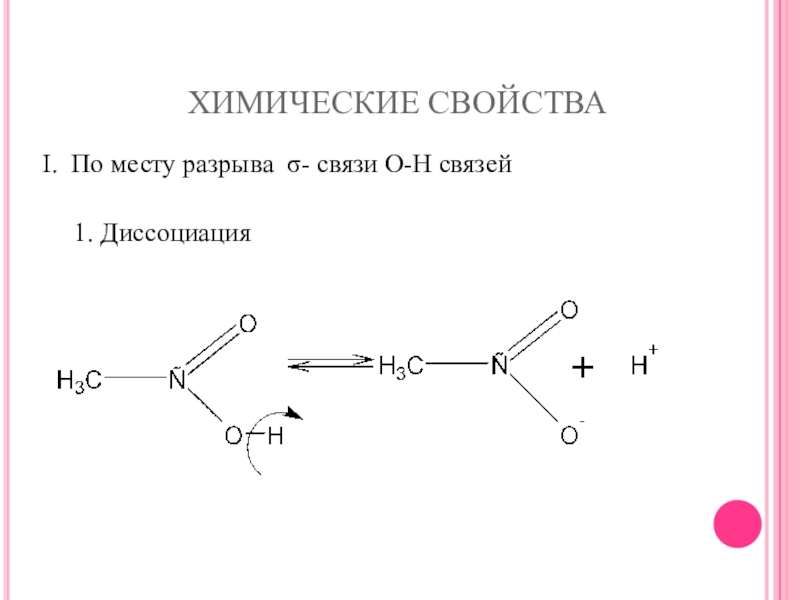
- 21. ХИМИЧЕСКИЕ СВОЙСТВА1. ДиссоциацияI. По месту разрыва σ- связи О-Н связей
- 22. 3. Взаимодействие с оксидами металлов4. Взаимодействие с основаниями2. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
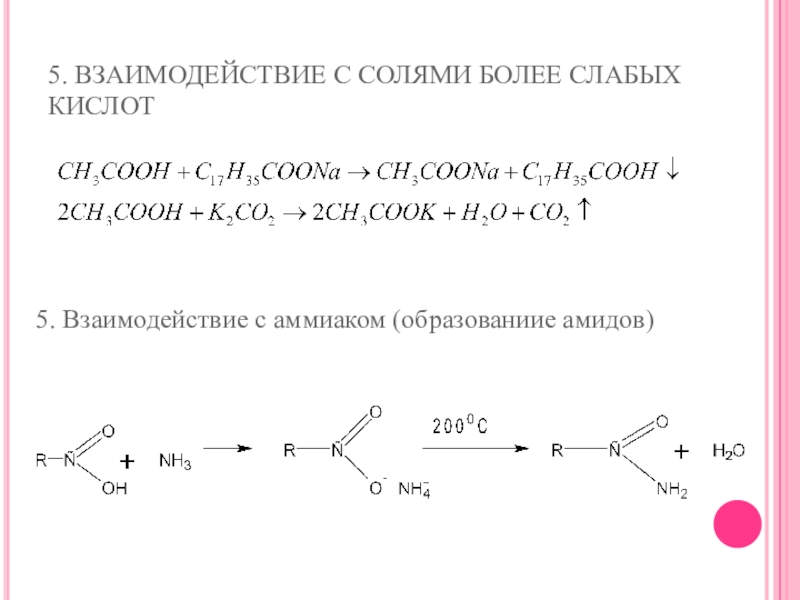
- 23. 5. ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ БОЛЕЕ СЛАБЫХ КИСЛОТ5. Взаимодействие с аммиаком (образованиие амидов)
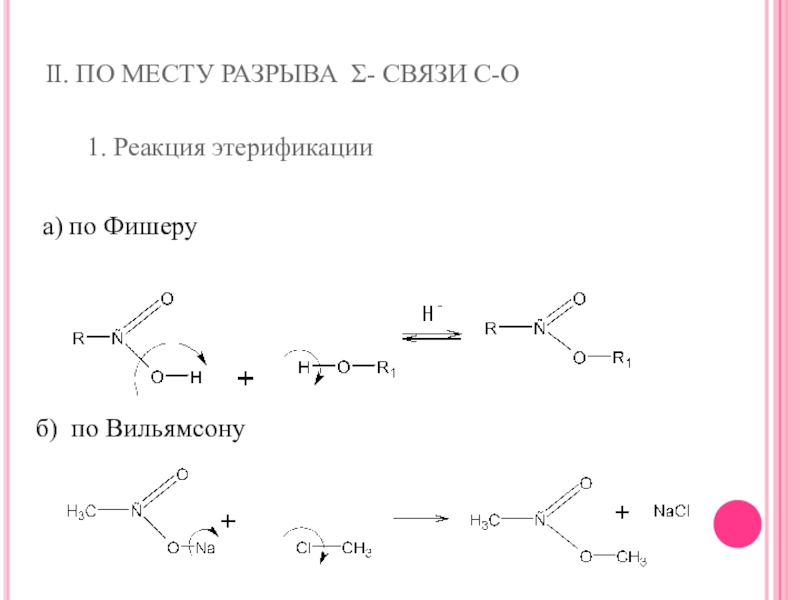
- 24. II. ПО МЕСТУ РАЗРЫВА Σ- СВЯЗИ С-О1. Реакция этерификацииа) по Фишеруб) по Вильямсону
- 25. 3. ОБРАЗОВАНИЕ АНГИДРИДОВа) внутримолекулярная дегидратацияб) межмолекулярная дегидратацияянтарная кислотаянтарный ангидридуксусная кислотауксусный ангидрид
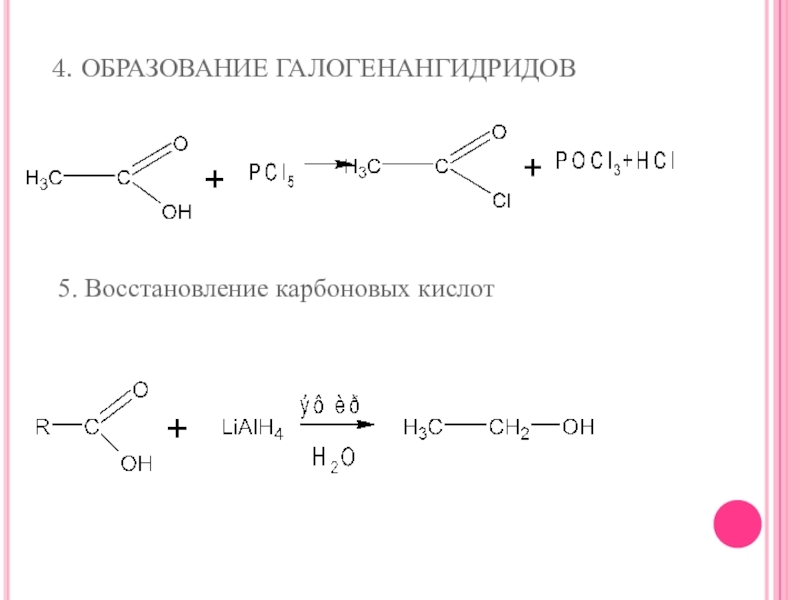
- 26. 4. ОБРАЗОВАНИЕ ГАЛОГЕНАНГИДРИДОВ5. Восстановление карбоновых кислот
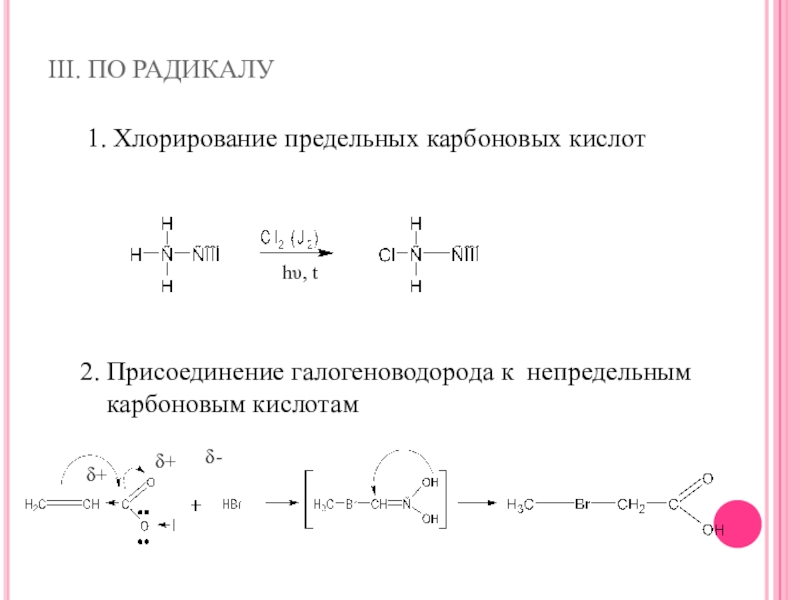
- 27. III. ПО РАДИКАЛУ1. Хлорирование предельных карбоновых кислот hυ, t2. Присоединение галогеноводорода к непредельным карбоновым кислотамδ+δ+δ-
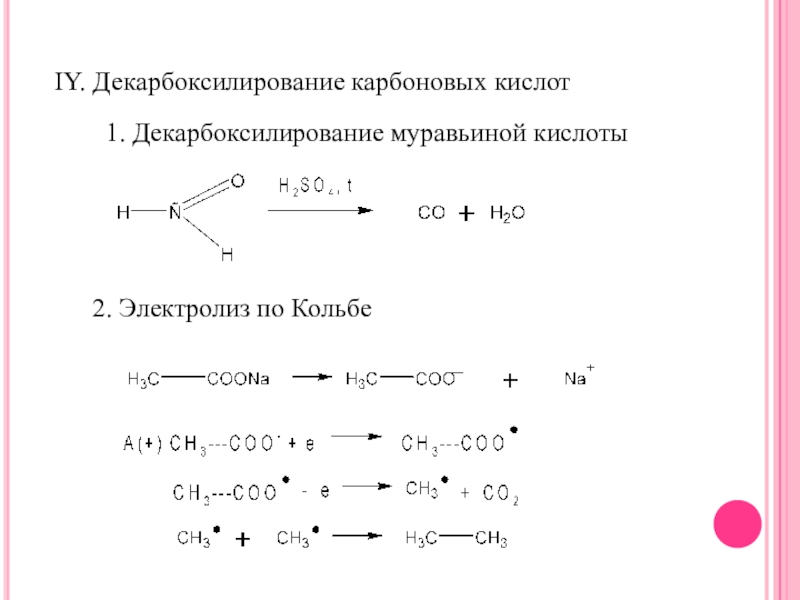
- 28. IY. Декарбоксилирование карбоновых кислот1. Декарбоксилирование муравьиной кислоты 2. Электролиз по Кольбе
- 29. ЛАБОРАТОРНАЯ РАБОТА№11
- 30. ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
- 31. ЦЕЛЬ: ИЗУЧЕНИЕ ХИМИЧЕСКИХ СВОЙСТВ КАРБОНОВЫХ КИСЛОТ.
- 32. ЗАДАНИЕ:1.Изучить торию химических свойств карбоновых кислот.2.Изучить методику
- 33. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ.
- 34. ОПЫТ 1. ОБРАЗОВАНИЕ СОЛЕЙ.К 0,5 мл 5%
- 35. ОПЫТ 2. ОБРАЗОВАНИЕ НЕРАСТВОРИМЫХ СОЛЕЙ ВЫСШИХ ЖИРНЫХ
- 36. ОПЫТ 3. ГИДРОЛИЗ МЫЛА.В пробирку с раствором
- 37. ОПЫТ 4.ОКИСЛЕНИЕ МУРАВЬИНОЙ КИСЛОТЫ ПЕРМАНГАНАТОМ КАЛИЯ.В пробирку
- 38. ОПЫТ 5. ОМЫЛЕНИЕ ЖИРА.К 0,5 мл подсолнечного
- 39. КОНТРОЛЬНЫЕ ВОПРОСЫ:1.Напишите уравнение реакции получения масляной кислоты
Слайд 2 КАРБОНОВЫЕ КИСЛОТЫ- ПРОИЗВОДНЫЕ
Слайд 41.В зависимости от природы углеводного радикала
а) предельные
б) непредельные
пропановая кислота
акриловая кислота
в) ароматические
бензойная
Классификация карбоновых кислот
Слайд 52. По числу атомов углерода в радикале
а) низшие
муравьиная кислота
б) высшие
α-линоленовая кислота
Слайд 63. По количеству карбоксильных групп
а) одноосновные
уксусная кислота
б) двухосновные
лимонная кислота
малоновая кислота
в) многоосновные
Слайд 11ИНДУКТИВНЫЙ ЭФФЕКТ КАРБОКСИЛЬНОЙ ГРУППИРОВКИ
δ+
δ-
- I индуктивный эффект
Электроноакцепторные заместители
Hal,
Слайд 12δ+
δ-
+ I индуктивный эффект
Электронодонорные заместители
Me, CH3-, CH3CH2-, (CH3)2CH- и
Индуктивный эффект карбоксильной группы
Слайд 20 Особенности строения и реакционная
способность предельных карбоновых
1.
Реакции сопровождающиеся разрывом О-Н связей
2.
Реакции по карбонильному углероду
3.
Декарбоксилирование
4.
Реакции по α- углеродному атому
Слайд 223. Взаимодействие с оксидами металлов
4. Взаимодействие с основаниями
2. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
Слайд 235. ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ БОЛЕЕ СЛАБЫХ КИСЛОТ
5. Взаимодействие с аммиаком (образованиие
Слайд 253. ОБРАЗОВАНИЕ АНГИДРИДОВ
а) внутримолекулярная дегидратация
б) межмолекулярная дегидратация
янтарная кислота
янтарный ангидрид
уксусная кислота
уксусный ангидрид
Слайд 27III. ПО РАДИКАЛУ
1. Хлорирование предельных карбоновых кислот
hυ, t
2. Присоединение галогеноводорода
карбоновым кислотам
δ+
δ+
δ-
Слайд 28IY. Декарбоксилирование карбоновых кислот
1. Декарбоксилирование муравьиной кислоты
2. Электролиз по Кольбе
Слайд 32ЗАДАНИЕ:
1.Изучить торию химических свойств карбоновых кислот.
2.Изучить методику выполнения лабораторной работы.
3.Изучить безопасные
4.Провести опыты.
5.Сопоставить уравнения реакции.
6.Описать продукты реакции.
7.Сделать вывод.
Слайд 34ОПЫТ 1. ОБРАЗОВАНИЕ СОЛЕЙ.
К 0,5 мл 5% раствора карбоната натрия приливают
Слайд 35ОПЫТ 2. ОБРАЗОВАНИЕ НЕРАСТВОРИМЫХ СОЛЕЙ ВЫСШИХ ЖИРНЫХ КИСЛОТ.
В пробирку с раствором
Слайд 36ОПЫТ 3. ГИДРОЛИЗ МЫЛА.
В пробирку с раствором мыла добавляют несколько капель
Слайд 37ОПЫТ 4.ОКИСЛЕНИЕ МУРАВЬИНОЙ КИСЛОТЫ ПЕРМАНГАНАТОМ КАЛИЯ.
В пробирку налить 1 мл муравьиной
Слайд 38ОПЫТ 5. ОМЫЛЕНИЕ ЖИРА.
К 0,5 мл подсолнечного ил другого растительного масла
Слайд 39КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Напишите уравнение реакции получения масляной кислоты из бутана.
2.Какое вещество получится,
3.Как обнаружить акриловую кислоту в смеси уксусной кислоты?
4.Какой необходимо взять кетон, чтобы при его окислении получить первые четыре гомологического ряда одноосновных насыщенных карбоновых кислот?
5.Получите стеариновую кислоту гидролизом соответствующего жира.
6.Как измеряется рКа карбоновых кислот с введением в радикал электронодонорных и электроноакцепторных заместителей? Привести пример.