- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Интегрированный урок по химии и биологии Галогены, их строение , свойства, применение
Содержание
- 1. Интегрированный урок по химии и биологии Галогены, их строение , свойства, применение
- 2. История открытия фтораВ 1886 году французский химик
- 3. Химические свойства фтораБудучи смешан с водородом, фтор
- 4. Слайд 4
- 5. Вариант №1Вариант №2
- 6. Качественное определение хлоридов и значения pH почвенной вытяжки
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. История открытия бромаВ 1825 году французский учёный
- 11. Химические свойства брома1. 2 Al + Br2
- 12. Получение брома в лаборатории Mn O2 + 4HBr= MnBr2+ Br2+2H2OCl2 + 2KBr= 2KCl+ Br2
- 13. История открытия йодаВ 1811 году открыл йод
- 14. Растворение йода
- 15. Химические свойства йода1. 3I2 +2Al = 2Al
- 16. В отличие от своих аналогов йод в
- 17. Суточная доза йода 50мкг. Для детей грудного
- 18. Источники йодаБурая водоросль ламинария (морская капуста)0,3% от общей массы
- 19. Морские рыбы
- 20. Слайд 20
- 21. Слайд 21
- 22. Ответы к загадкам
- 23. хурма
- 24. шампиньоны
- 25. чеснок
- 26. морковь
- 27. картофель
- 28. фасоль
- 29. томаты
- 30. лук
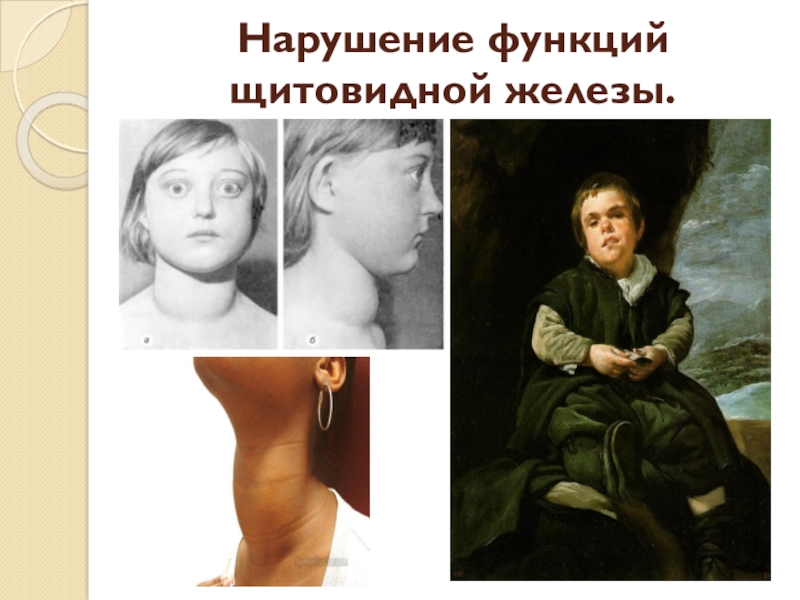
- 31. Нарушение функций щитовидной железы.
Слайд 2История открытия фтора
В 1886 году французский химик Анри Муассан смог получить
В 1906 году Муассан был удостоен Нобелевской премии.
Анри Муассан
(1852 – 1907)
F
2
Слайд 3Химические свойства фтора
Будучи смешан с водородом, фтор воспламеняется в темноте, часто
H2 + F2 = 2HF
Раствор фтора в воде получить нельзя, так как фтор окисляет из воды кислород.
2H2O + 2F2 =4HF +O2
SiO2 + F2 =SiF4 + O2
Xe +2F2 = XeF4
Cl2 + 3F2 = 2ClF3
2HCl + F2 =2HF +Cl2
2F2 + 2 KOH(p-p) = OF2 + 2KF + H2O
Слайд 10История открытия брома
В 1825 году французский учёный Антуан Балар получил бром
Антуан Жером Балар
(1802 – 1876)
Br
2
Слайд 11Химические свойства брома
1. 2 Al + Br2 = 2Al Br3
2. H2
3. 2P + 5Br2 = 2PBr5
4. Br2 + H2O = HBr + HBrO
6. Br2 + 2 KI = I2 + 2KBr
5. Br2 + 2NaOH(кон) = NaBrO +NaBr+H2O
20°C
7. Br2 + H2S= S+ 2HBr
Br2 реагирует с сильными восстановителями:
8. Br2 + 2HI= 2HBr+ I2
Слайд 13История открытия йода
В 1811 году открыл йод действуя на золу морских
Бернар Куртуа (1777 – 1838 )
I
2
Слайд 15Химические свойства йода
1. 3I2 +2Al = 2Al I3
2. I2 +Hg =
3. I2 +H2 = 2HI
4. I2 +H2S = S + 2HI
5. 3I2 +6NaOH = 5NaI + NaIO3 +3H2 O
Слайд 16В отличие от своих аналогов йод в виде иодид – иона
2 KI +H2O2 = 2KOH +I2
2 KI +2FeCl3 = I2 + 2KCl + 2FeCl2
2 KI +H2O2 = 2KOH +I2
4 KI +2CuSO4 = 2CuI + 2K2SO4 +I2
Йодокрахмальная бумага служит индикатором на окислители.
2 KI +O3 + H2O= 2KOH +O2+I2
Слайд 17Суточная доза йода
50мкг. Для детей грудного возраста (первые 12 месяцев)
90мкг. Для
120 мкг. Для детей школьного возраста (то 7 до 12 лет)
150 мкг для подростков (от 12 лет и старше) и взрослых
100 мкг. Для людей пожилого возраста
200 мкг. Для беременных и кормящих женщин.