- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Введение. Предмет органической химии.
Содержание
- 1. Введение. Предмет органической химии.
- 2. § 1. Предмет органической химии.§ 2. Теория строения органических соединений.
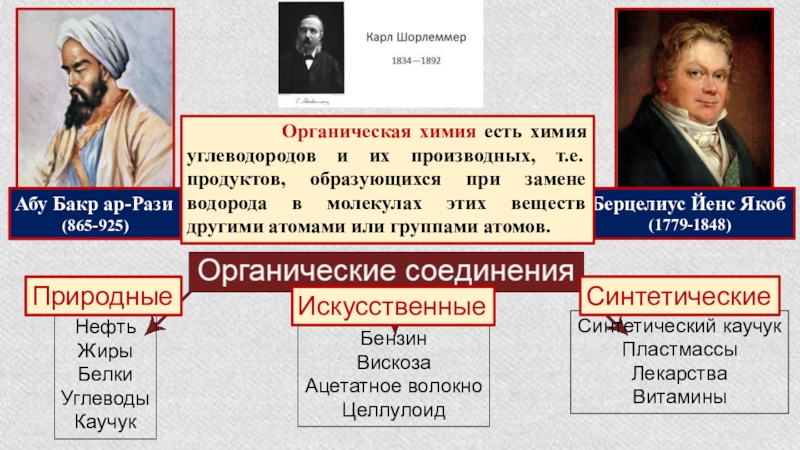
- 3. Предмет органической химии
- 4. Абу Бакр ар-Рази(865-925)Берцелиус Йенс Якоб(1779-1848)
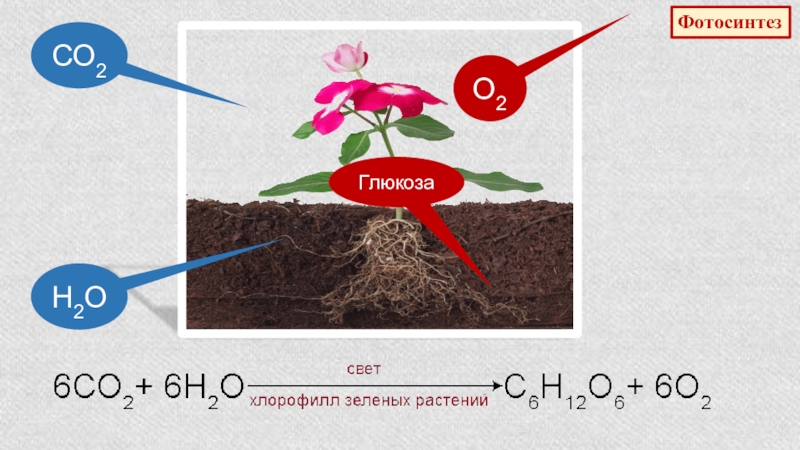
- 5. ФотосинтезО2ГлюкозаСО2Н2О
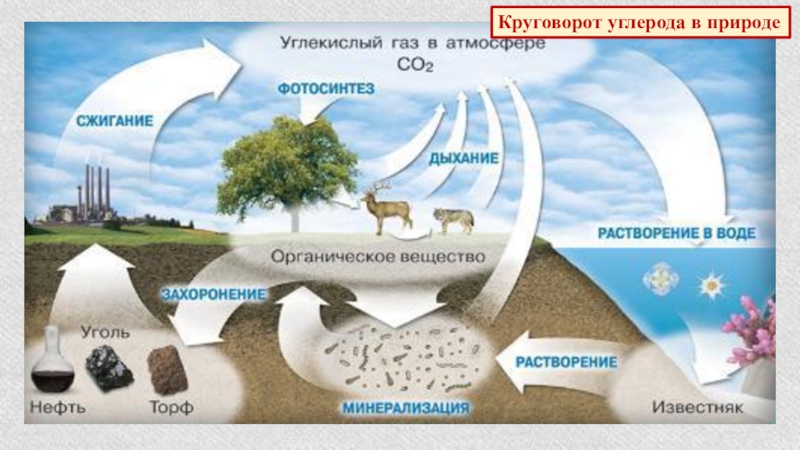
- 6. Круговорот углерода в природе
- 7. Основные классы углеводородов Алканы
- 8. Особенности органических соединенийПо причине наличия атомов углерода
- 9. Теория строения органических соединений
- 10. Фридрих Август Кекуле(1829-1896)В 1857 году установил, что
- 11. Основные положения теории строения органических веществ1. Все
- 12. 1. Все атомы, образующие молекулы органических веществ,
- 13. 2. Свойства вещества зависят не только от
- 14. Этиловый спиртДиметиловый эфирСН3 – СН2 – ОН
Слайд 4Абу Бакр ар-Рази
(865-925)
Берцелиус Йенс Якоб
(1779-1848)
Нефть
Жиры
Белки
Углеводы
Каучук
Бензин
Вискоза
Ацетатное волокно
Целлулоид
Синтетический каучук
Пластмассы
Лекарства
Витамины
Природные
Искусственные
Синтетические
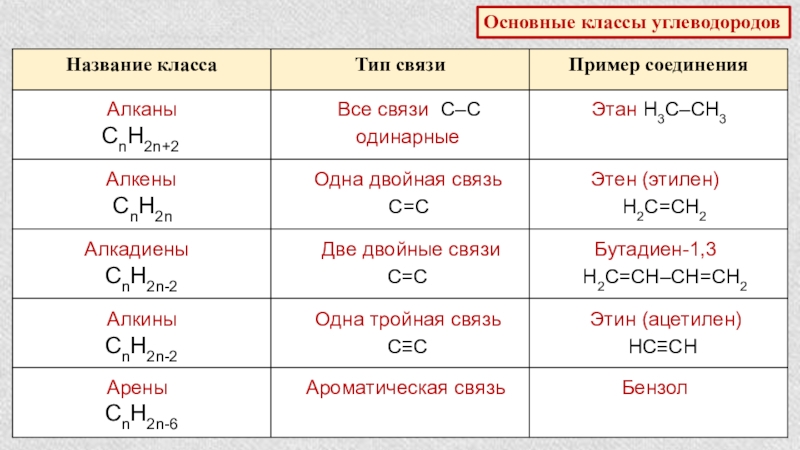
Слайд 7Основные классы углеводородов
Алканы
СnH2n+2 одинарные
Алкены Одна двойная связь Этен (этилен)
СnH2n С=С Н2С=СН2
Алкадиены Две двойные связи Бутадиен-1,3
СnH2n-2 С=С Н2С=СН–СН=СН2
Алкины Одна тройная связь Этин (ацетилен)
СnH2n-2 С≡С НС≡СН
Арены Ароматическая связь Бензол
СnH2n-6
Слайд 8Особенности органических соединений
По причине наличия атомов углерода и водорода большинство органических
Органические соединения более многообразны, чем неорганические вещества, в настоящее время их число составляет более 25 миллионов;
Органические соединения построены более сложно, чем неорганические вещества, многие из них имеют огромную молекулярную массу;
Органические соединения образованы, как правило, за счет ковалентных связей, и поэтому имеют молекулярное строение, следовательно, обладают невысокими температурами плавления и кипения, термически неустойчивы.
Слайд 10Фридрих Август Кекуле
(1829-1896)
В 1857 году установил, что углерод имеет валентность, равную
Арчибальд Скотт Купер
(1831-1892)
В 1858 году доказал, что углерод может образовывать различные цепи (объясняющие явление изомерии).
Предпосылки теории
А. М. Бутлеров
(1828-1886)
В 1861 году сформулировал основные идеи теории строения органических соединений.
Слайд 11Основные положения теории строения органических веществ
1. Все атомы, образующие молекулы органических
2. Свойства веществ зависят не только от того, какие атомы и сколько их входит в состав молекул, но и от порядка соединения атомов в молекулах.
3. Атомы и группы атомов в молекулах веществ взаимно влияют друг на друга.
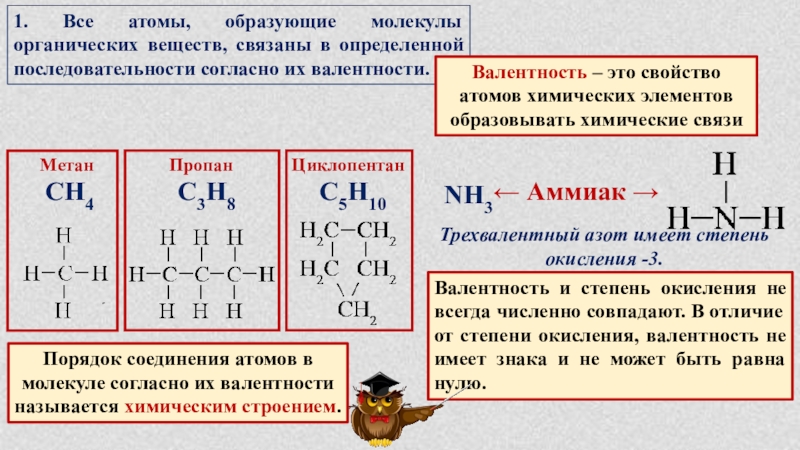
Слайд 121. Все атомы, образующие молекулы органических веществ, связаны в определенной последовательности
Валентность – это свойство атомов химических элементов образовывать химические связи
Метан
СН4
Пропан
С3Н8
Циклопентан
С5Н10
← Аммиак →
NH3
Трехвалентный азот имеет степень окисления -3.
Валентность и степень окисления не всегда численно совпадают. В отличие от степени окисления, валентность не имеет знака и не может быть равна нулю.
Порядок соединения атомов в молекуле согласно их валентности называется химическим строением.
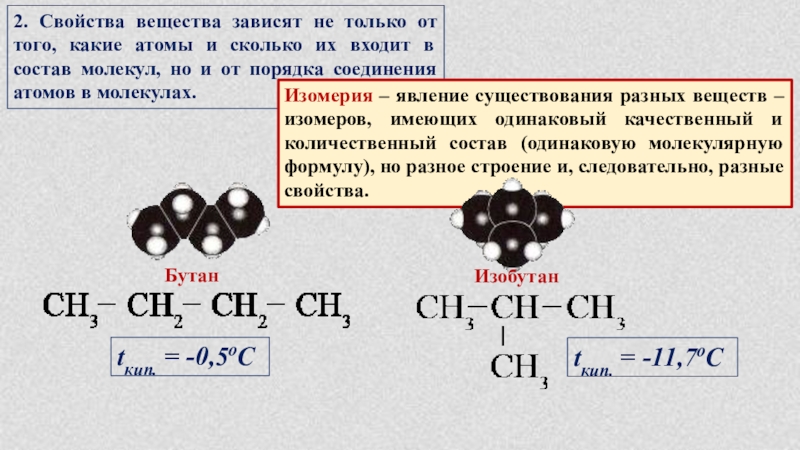
Слайд 132. Свойства вещества зависят не только от того, какие атомы и
Изомерия – явление существования разных веществ – изомеров, имеющих одинаковый качественный и количественный состав (одинаковую молекулярную формулу), но разное строение и, следовательно, разные свойства.
Бутан
Изобутан
tкип. = -0,5oC
tкип. = -11,7oC
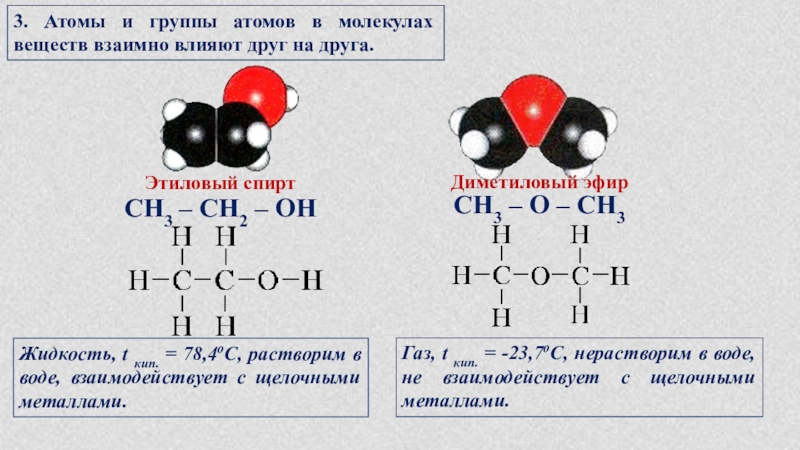
Слайд 14Этиловый спирт
Диметиловый эфир
СН3 – СН2 – ОН
СН3 – О –
Жидкость, t кип. = 78,4оС, растворим в воде, взаимодействует с щелочными металлами.
Газ, t кип. = -23,7оС, нерастворим в воде, не взаимодействует с щелочными металлами.
3. Атомы и группы атомов в молекулах веществ взаимно влияют друг на друга.