- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Вода – растворитель. Растворы
Содержание
- 1. Вода – растворитель. Растворы
- 2. Вода… Ты не имеешь ни вкуса, ни
- 3. Вода в природе
- 4. Вода - самое распространенное на Земле вещество, она
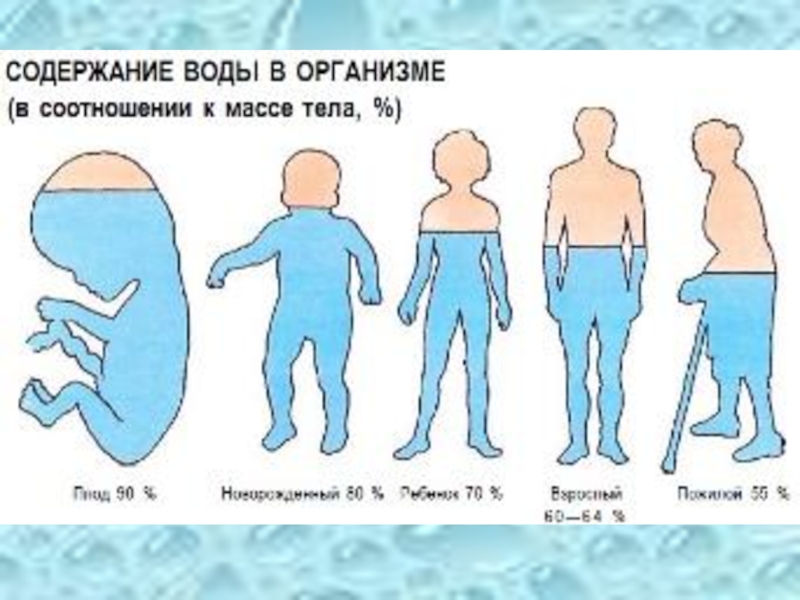
- 5. Вода обеспечивает доставку питательных веществ и кислорода
- 6. Слайд 6
- 7. Слайд 7
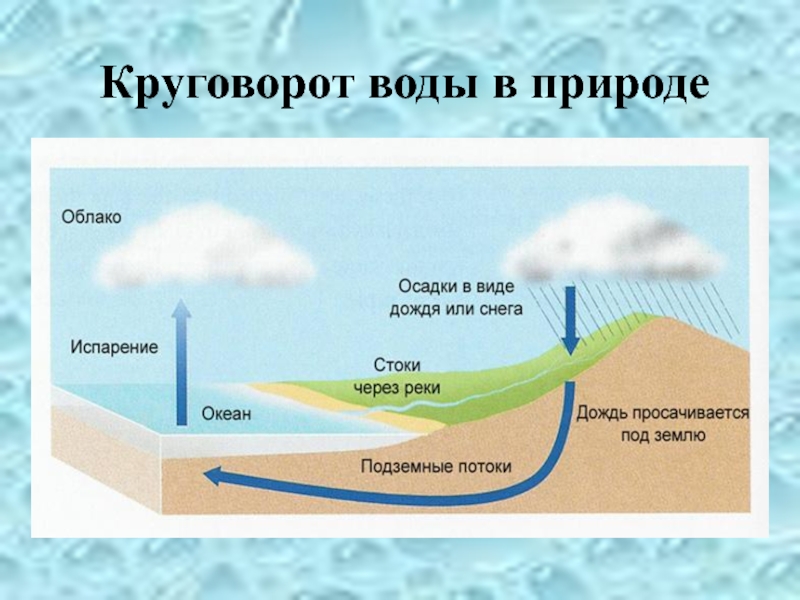
- 8. Круговорот воды в природе
- 9. Аномалии воды1. существует на Земле в 3
- 10. 4. особые тепловые свойства: высокая удельная теплоемкость.
- 11. Среди всех жидкостей вода имеет самое высокое поверхностное натяжение, исключение составляет только ртуть.
- 12. Физические свойства водыОсновными физическими свойствами воды являются
- 13. При комнатных условиях вода представляет собой жидкость
- 14. При комнатных условиях вода представляет собой жидкость
- 15. Максимальная плотность воды при 4 ºС. При
- 16. Лед легче воды, и поэтому
- 17. ЭлектропроводностьСовершенно чистая вода плохо проводит электрический ток.
- 18. Вязкость воды с ростом температуры быстро
- 19. Плотность воды При +4°С градусах плотность
- 20. Слайд 20
- 21. Опыт3 – взаимодействие воды с металлическим натрием:
- 22. ПроверкаCa + H2O = Ca(OH)2 + H2Разложение воды электрическим токомУравнение реакции:2Н2О = 2Н2 + О2
- 23. Слайд 23
- 24. Слайд 24
- 25. Слайд 25
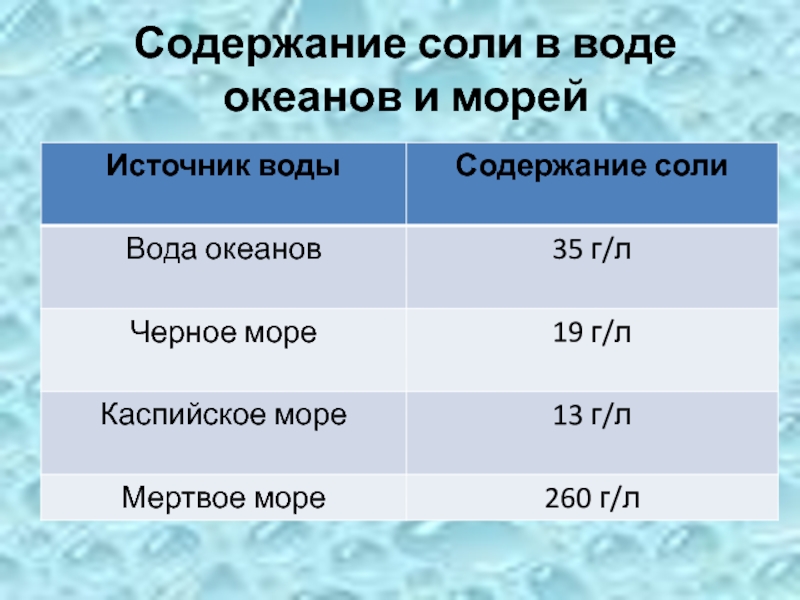
- 26. Чем природная вода (морская, речная, колодезная) отличается по вкусу от кипяченой воды?
- 27. Содержание соли в воде океанов и морей
- 28. Растворы – однородные системы, состоящие из молекул
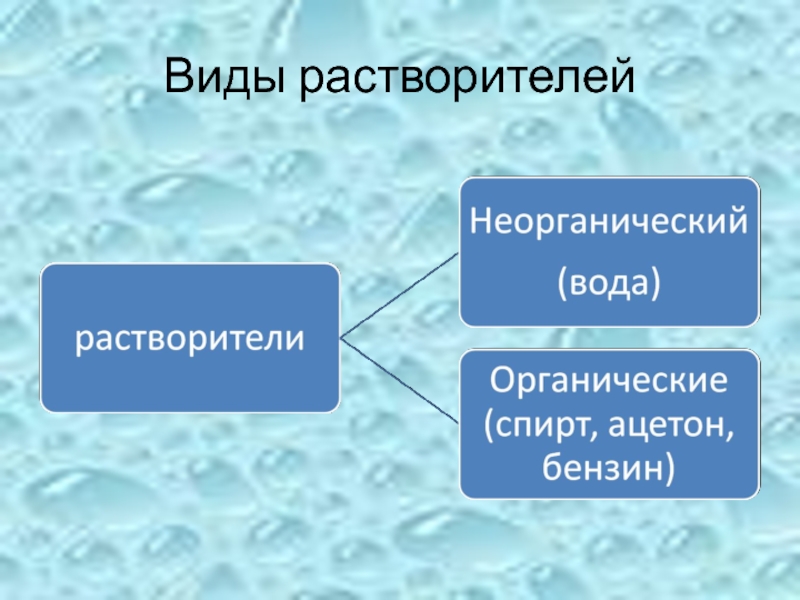
- 29. Виды растворителей
- 30. Виды растворов
- 31. Концентрированные растворы – растворы, содержащие много растворенного вещества и мало растворителя.
- 32. Разбавленные растворы – растворы, содержащие мало растворенного вещества и много растворителя
- 33. Насыщенные растворы – растворы, в которых при данной температуре вещество уже не может больше растворяться
- 34. Ненасыщенные растворы – растворы, в которых при данной температуре вещество еще может растворяться
- 35. Концентрация раствора Концентрация раствора – содержание растворенного вещества в растворе
- 36. Способы выражения концентрацииКоэффициент растворимости или растворимостьМассовая доля или процентная концентрация растворенного веществаМолярная концентрация
- 37. Коэффициент растворимости или растворимостьКоэффициент растворимости показывает, какая
- 38. ωв – ва - массовая доля
Вода… Ты не имеешь ни вкуса, ни цвета, ни запаха, тебя невозможно описать – тобой наслаждаешься, не ведая, что ты такое.Ты не просто необходима для жизни, ты и есть сама жизнь.Ты божество, ты совершенство, ты самое
Слайд 1*
Вода – растворитель.
Растворы
Подготовила преподаватель химии и биологии
ГАПОУ «Международный колледж сервиса»
Города Казани. 2016 год
Слайд 2Вода… Ты не имеешь ни вкуса, ни цвета, ни запаха, тебя
невозможно описать – тобой наслаждаешься, не ведая, что ты такое.
Ты не просто необходима для жизни, ты и есть сама жизнь.
Ты божество, ты совершенство, ты самое большое богатство на свете
А. де Сент-Экзюпери
Ты не просто необходима для жизни, ты и есть сама жизнь.
Ты божество, ты совершенство, ты самое большое богатство на свете
А. де Сент-Экзюпери
Слайд 4
Вода - самое распространенное на Земле вещество, она занимает более 70% площади
поверхности земли, и только около 30% приходится на долю суши. Вода придает Земле тот неповторимый вид, который отличает ее от других планет Солнечной системы.
Слайд 5
Вода обеспечивает доставку питательных веществ и кислорода ко всем клеткам тела,
защиту и буферизацию жизненно важных органов, регуляцию температуры тела, помогает в преобразовании пищи в энергию, усвоении питательных веществ органами, вывод шлаков и отходов в процессе жизнедеятельности и выполнение целого ряда других функций
Слайд 9Аномалии воды
1. существует на Земле в 3 агрегатных состояниях.
2. при нагревании
от 0 до 4 градусов Цельсия объем воды не увеличивается, а уменьшается. Максимальная плотность ее при температуре 4 градуса.
3.при замерзании вода расширяется, а не сжимается, как все другие тела.
3.при замерзании вода расширяется, а не сжимается, как все другие тела.
Слайд 104. особые тепловые свойства: высокая удельная теплоемкость. Поглощает тепло от Солнца,
а при охлаждении медленно отдает тепло, регулируя колебания температуры.
5Находясь в капиллярах образует вогнутый мениск.
6. температура замерзания воды с увеличением давления понижается, а не повышается как у других веществ.
5Находясь в капиллярах образует вогнутый мениск.
6. температура замерзания воды с увеличением давления понижается, а не повышается как у других веществ.
Слайд 11Среди всех жидкостей вода имеет самое высокое поверхностное натяжение, исключение составляет
только ртуть.
Слайд 12Физические свойства воды
Основными физическими свойствами воды являются – запах, цвет, прозрачность,
вкус, плотность, температура, вязкость, сжимаемость, электропроводность.
Слайд 13При комнатных условиях вода представляет собой жидкость без вкуса и запаха.
В тонком слое вода не имеет цвета.
Слайд 14При комнатных условиях вода представляет собой жидкость без вкуса и запаха.
В тонком слое вода не имеет цвета.
Слайд 15Максимальная плотность воды при 4 ºС. При замерзании вода расширяется. Лёд
легче воды.
Температура замерзания воды
Температура кипения воды
0 ºС
+100 ºС
Слайд 16 Лед легче воды, и поэтому он не тонет в
ней. Такая особенность воды объясняет, почему водоемы начинают замерзать не со дна, а с поверхности и очень редко промерзают до самого дна. Это защищает живые организмы, которые живут в реках и морях от гибели.
Слайд 17Электропроводность
Совершенно чистая вода плохо проводит электрический ток. По тому, как проводит
электрический ток вода, можно судит о ее чистоте: чем ниже электропроводность, тем чище вода.
Слайд 18Вязкость воды
с ростом температуры быстро уменьшается и при 100° С
оказывается в 8 раз меньше, чем при 0° С.
Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями.
Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями.
Слайд 19Плотность воды
При +4°С градусах плотность воды превышает плотность льда,
благодаря чему охлаждаясь сверху вода опускается на дно лишь до тех пор, пока ее температура не достигнет +4°С, вследствие чего лед остается на поверхности водоемов, что делает возможным жизнь под слоем льда водной флоры и фауны.
Слайд 21
Опыт3 – взаимодействие воды с металлическим натрием:
2H2O+2Na = 2NaOH +H2
опыт 4- взаимодействие воды с металлическим кальцием:
Составьте уравнение реакции
Составьте уравнение реакции
Слайд 22Проверка
Ca + H2O = Ca(OH)2 + H2
Разложение воды электрическим током
Уравнение реакции:
2Н2О
= 2Н2 + О2
Слайд 28Растворы – однородные системы, состоящие из молекул растворителя и частиц растворенного
вещества, между которыми происходят физические и химические взаимодействия.
Раствор = Растворитель + Растворенное вещество
Раствор = Растворитель + Растворенное вещество
Слайд 31Концентрированные растворы – растворы, содержащие много растворенного вещества и мало растворителя.
Слайд 32Разбавленные растворы – растворы, содержащие мало растворенного вещества и много растворителя
Слайд 33Насыщенные растворы – растворы, в которых при данной температуре вещество уже
не может больше растворяться
Слайд 34Ненасыщенные растворы – растворы, в которых при данной температуре вещество еще
может растворяться
Слайд 36Способы выражения концентрации
Коэффициент растворимости или растворимость
Массовая доля или процентная концентрация растворенного
вещества
Молярная концентрация
Молярная концентрация
Слайд 37Коэффициент растворимости или растворимость
Коэффициент растворимости показывает, какая максимальная масса вещества может
раствориться в 100 г (или 1000 г) растворителя
Растворимость веществ
(на 100 г воды при 20 ° С)
Растворимость веществ
(на 100 г воды при 20 ° С)
Хорошо растворимые
(больше 1 г)
Практически нерастворимые
меньше 0,01 г
Малорастворимые
(меньше 1 г)
Слайд 38 ωв – ва - массовая доля растворенного вещества в растворе
m в – ва – масса растворенного вещества
m р – ра – масса раствора
ωв – ва = m в – ва
m р – ра
m р – ра – масса раствора
ωв – ва = m в – ва
m р – ра