восьмиклассники помогите мне составить опорный конспект на тему:
Оксиды, состав, номенклатура, классификация.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок по химии 8 классе. Оксиды.
Содержание
- 1. Урок по химии 8 классе. Оксиды.
- 2. Инструкция. Как составить опорный КОНСПЕКТ
- 3. Причиной эффекта собачьей пещеры в Италии является
- 4. Кислотные дожди появляются, когда с атмосферным кислородом
- 5. Известно около 300 оксидов. Из железных руд,
- 6. Что общего из приведенных оксидов?
- 7. Расставьте степень окисления в оксидах:MgO, CaO, CuO,
- 8. Перезагрузка.
- 9. Продолжаем составлять конспект.
- 10. Напишите формулы оксидов и наоборот дайте название.Оксид
- 11. Классификация оксидов Все оксиды, по способности образовать
- 12. Слайд 12
- 13. Физические свойства оксидов Оксиды весьма разнообразны по
- 14. Слайд 14
- 15. Рефлексия. Итоги.
- 16. Ссылки использованных ресурсов.http://www.himikatus.ru/art/dif_news/vih.jpg https://avatars.mds.yandex.net/get-zen_doc/27036/pub_5b0e7ba248c85e2421e04039_5b0e7d1c40888a00a9101249/scale_1200 https://sc01.alicdn.com/kf/HTB1onTKXnHuK1RkSndVq6xVwpXaz/Color-pigment-iron-oxide-fe2o3-for-concrete.jpg https://ds02.infourok.ru/uploads/ex/0153/0005f4c2-335af2bc/img26.jpg
Инструкция. Как составить опорный КОНСПЕКТ Опорный конспект – это сокращенная символическая запись изучаемого материала, в которой сжато изображены основные смысловые вехи изучаемой темы. Составить такую «шпаргалку» - значит проработать весь необходимый
Слайд 2Инструкция. Как составить опорный КОНСПЕКТ
Опорный конспект – это
сокращенная символическая запись изучаемого материала, в которой сжато изображены основные смысловые вехи изучаемой темы.
Составить такую «шпаргалку» - значит проработать весь необходимый материал, структурировать свои знания, «разложить все по полочкам».
Главное условие: краткость, наглядность, минимум текстовой информации. Новые термины целесообразно записывать полностью.
Составить такую «шпаргалку» - значит проработать весь необходимый материал, структурировать свои знания, «разложить все по полочкам».
Главное условие: краткость, наглядность, минимум текстовой информации. Новые термины целесообразно записывать полностью.
Слайд 3Причиной эффекта собачьей пещеры в Италии является оксид углерода СО2. Он
тяжелее воздуха, поэтому получается так, что газ в пещере как раз покрывает собачью голову. Невысокие животные гибнут от удушья за несколько минут. А за счёт своего роста человек может легко пройти по ней.
Слайд 4Кислотные дожди появляются, когда с атмосферным кислородом и водяным паром соединяются
оксиды серы и азота. Эти оксиды выбрасываются в окружающую среду металлургическими предприятиями, электростанциями, автомобильным транспортом. Полученные таким образом кислоты имеют вид дождя и разносятся ветром.
Слайд 5Известно около 300 оксидов. Из железных руд, содержащих оксиды железа, получают
железо.
Песок, состоящий преимущественно состоит из SiO2, используют при производстве стекла.
Некоторые оксиды являются основой для красок: ZnO – белой, Fe2O3 – коричневой, Cr2O3 – зелёной. А природные и искусственные кристаллы оксидов алюминия, окрашенные примесями, используют для изготовления ювелирных украшений.
Песок, состоящий преимущественно состоит из SiO2, используют при производстве стекла.
Некоторые оксиды являются основой для красок: ZnO – белой, Fe2O3 – коричневой, Cr2O3 – зелёной. А природные и искусственные кристаллы оксидов алюминия, окрашенные примесями, используют для изготовления ювелирных украшений.
Слайд 7Расставьте степень окисления в оксидах:
MgO, CaO, CuO, Cu2O, Na2O, k2O, CO,
SO2, NO,
P2O5, Al2O3 BeO, MnO2, SiO2, Fe2O3, FeO, ZuO
P2O5, Al2O3 BeO, MnO2, SiO2, Fe2O3, FeO, ZuO
Слайд 10Напишите формулы оксидов и наоборот дайте название.
Оксид серы (IV), оксид фосфора(V),
оксид углерода(IV), оксид серы(VI)
MgO, CaO, CuO, Cu2O, Na2O, k2O, CO, SO2, NO, P2O5, Al2O3, BeO, MnO2, SiO2, Fe2O3, FeO, ZuO
MgO, CaO, CuO, Cu2O, Na2O, k2O, CO, SO2, NO, P2O5, Al2O3, BeO, MnO2, SiO2, Fe2O3, FeO, ZuO
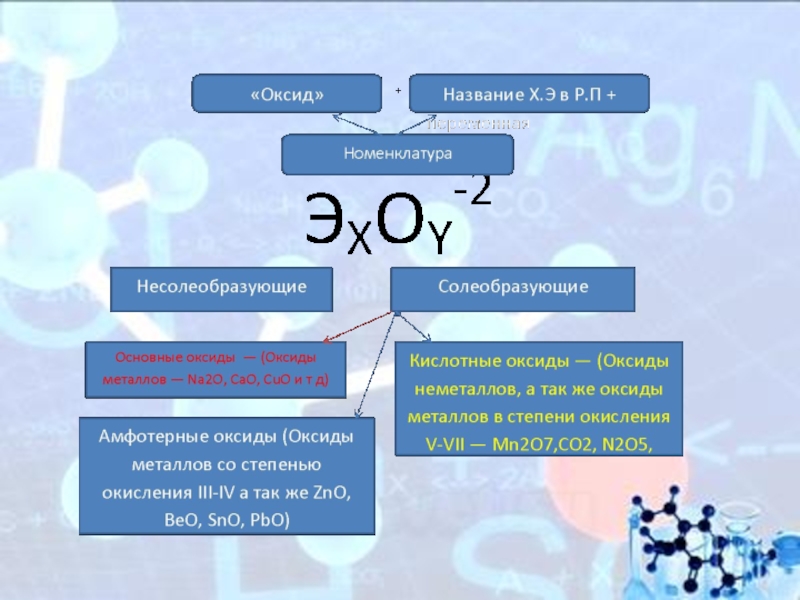
Слайд 11Классификация оксидов
Все оксиды, по способности образовать соли, можно разделить на две
группы:
Солеобразующие оксиды (CO2, N2O5,Na2O, SO3 и т. д.)
Несолеобразующие оксиды(CO, N2O,SiO, NO и т. д.)
В свою очередь, солеобразующие оксиды подразделяют на 3 группы:
Основные оксиды — (Оксиды металлов — Na2O, CaO,CuO)
Кислотные оксиды — (Оксиды неметаллов, а так же оксиды металлов в степени окисления V-VII — Mn2O7,CO2, N2O5, SO2, SO3 и т д)
Амфотерные оксиды (Оксиды металлов со степенью окисления III-IV а так же ZnO, BeO, SnO, PbO)
Солеобразующие оксиды (CO2, N2O5,Na2O, SO3 и т. д.)
Несолеобразующие оксиды(CO, N2O,SiO, NO и т. д.)
В свою очередь, солеобразующие оксиды подразделяют на 3 группы:
Основные оксиды — (Оксиды металлов — Na2O, CaO,CuO)
Кислотные оксиды — (Оксиды неметаллов, а так же оксиды металлов в степени окисления V-VII — Mn2O7,CO2, N2O5, SO2, SO3 и т д)
Амфотерные оксиды (Оксиды металлов со степенью окисления III-IV а так же ZnO, BeO, SnO, PbO)
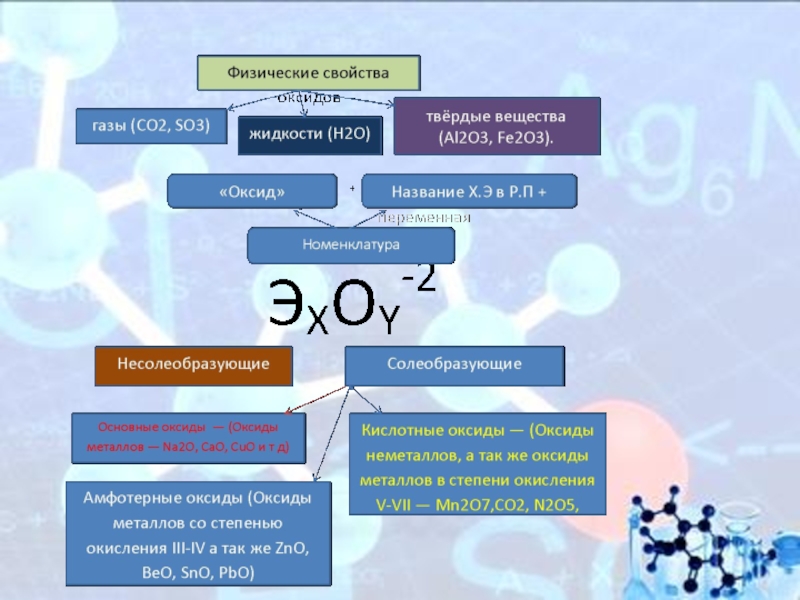
Слайд 13Физические свойства оксидов
Оксиды весьма разнообразны по своим физическим свойствам. Они могут
быть как жидкостями (Н2О), так и газами (СО2, SO3) или твёрдыми веществами (Al2O3, Fe2O3). Приэтом оснОвные оксиды, как правило, твёрдые вещества. Окраску оксиды также имеют самую разнообразную — от бесцветной (Н2О, СО) и белой (ZnO, TiO2) до зелёной (Cr2O3) и даже чёрной (CuO).