систематизировать знания по данной теме.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок химии в 8-м классе. Обобщение и систематизация знаний по теме Изменения, происходящие с веществами
Содержание
- 1. Урок химии в 8-м классе. Обобщение и систематизация знаний по теме Изменения, происходящие с веществами
- 2. Блиц - опросфизические явления
- 3. Химические явления
- 4. Химическое уравнениеУсловная запись химической реакции с помощью химических формул и математических знаков
- 5. Закон сохранения массы веществМасса веществ, вступивших в реакцию, равна массе образовавшихся веществ.
- 6. Экзотермические реакции
- 7. Эндотермические реакции
- 8. Простые вещества
- 9. Сложные вещества
- 10. Слайд 10
- 11. Физические и химические явленияА - физическоеБ -
- 12. Как очистить воду?Раствор CuSO4Смесь масла и водыСмесь
- 13. Слайд 13
- 14. Конкурс капитанов
- 15. «кто быстрее»Реакция соединения.Реакция разложения.Реакция обмена.Реакция замещения.Карбонат кальция.Соляная
- 16. Конкурс капитанов.2Al(OH)3 + 3H2SO4 = Al2(SO4)3 +
- 17. Практикум
- 18. Слайд 18
- 19. Самостоятельная работа3Fe + 2O2 =Fe3O4
- 20. Слайд 20
- 21. Домашнее задание:Провести домашний опыт- химическую реакцию уксусной
- 22. Спасибо за хорошую работу на уроке!
Блиц - опросфизические явления
Слайд 4Химическое уравнение
Условная запись химической реакции с помощью химических формул и математических
знаков
Слайд 5Закон сохранения массы веществ
Масса веществ, вступивших в реакцию, равна массе образовавшихся
веществ.
Слайд 11Физические и химические явления
А - физическое
Б - физическое
В – физическое
Г
–химическое
Д - физическое
Е - химическое
Ж - физическое
Д - физическое
Е - химическое
Ж - физическое
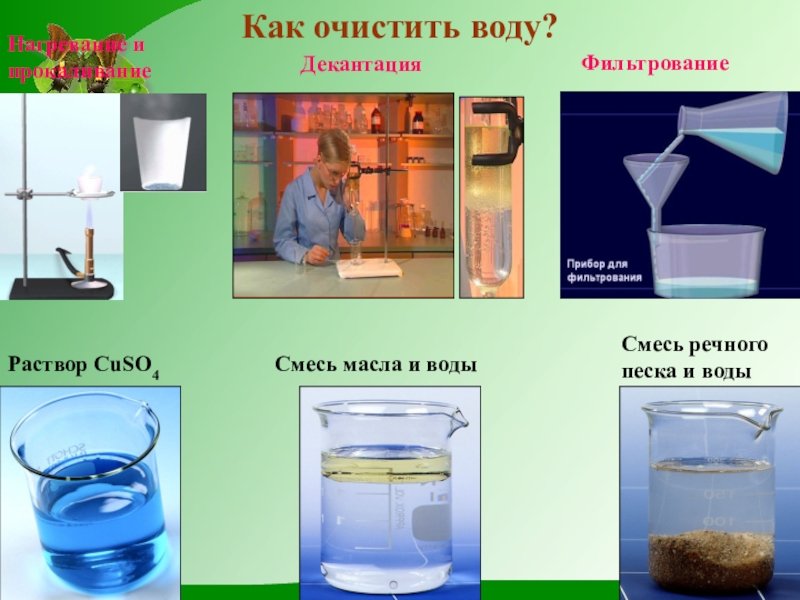
Слайд 12Как очистить воду?
Раствор CuSO4
Смесь масла и воды
Смесь речного песка и воды
Нагревание
и прокаливание
Декантация
Фильтрование
Слайд 15«кто быстрее»
Реакция соединения.
Реакция разложения.
Реакция обмена.
Реакция замещения.
Карбонат кальция.
Соляная кислота.
Сульфат меди (II).
Высшая
степень окисления серы.
Низшая степень окисления углерода.
Гидроксид железа (III).
Низшая степень окисления углерода.
Гидроксид железа (III).
Слайд 16Конкурс капитанов.
2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
NaOH + HCl =NaCl
+ H2O
BaCl2 + H2SO4 = BaSO4 + 2HCl
2Fe(OH)3 = Fe2O3 + 3H2O
BaCl2 + H2SO4 = BaSO4 + 2HCl
2Fe(OH)3 = Fe2O3 + 3H2O
Слайд 19Самостоятельная работа
3Fe + 2O2 =Fe3O4
1 вариант
Zn + CuCl2 = ZnCl2 + Cu
3Ba(OH)2 + P2O5 = Ba3(PO4)2 + 3H2O
2NaNO3 = 2NaNO2 + O2
2 вариант
Zn + CuCl2 = ZnCl2 + Cu
3Ba(OH)2 + P2O5 = Ba3(PO4)2 + 3H2O
2NaNO3 = 2NaNO2 + O2
2 вариант
CuSO4 + Fe = FeSO4 + Cu
4Li + O2 = 2Li2O
3AgNO3+ K3PO4 = 3KNO3+ Ag3PO4
2KClO3 = 2KCl + 3O2
Слайд 21Домашнее задание:
Провести домашний опыт- химическую реакцию уксусной кислоты и соды, результат
записать в виде уравнения.
Повторить формулы нахождения количества вещества и массовой доли вещества.
Повторить формулы нахождения количества вещества и массовой доли вещества.