- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Темір оның қосылыстары және физикалық қасиеттері
Содержание
- 1. Темір оның қосылыстары және физикалық қасиеттері
- 2. Мазмұны:Периодтық жүйедегі орны және атом құрылысыТабиғатта таралуыӨнеркәсіпте алынуыФизикалық қасиеттеріХимиялық қасиеттеріТемірдің маңызды қосылыстарыҚолданылуыҚұрамында темірі бар қосылыстар
- 3. Жалпы сипаттама. Периодтық жүйедегі орны және атом
- 4. Электрондық формуласы:1s2 2s2 2p6 3s2 3p6 3d6 4s21s22s22p63s23p63d64s2Next
- 5. Темір химиялық реакцияларда 2 немесе 3 электрон
- 6. Табиғатта таралуы Темір – табиғатта таралуы бойынша екінші
- 7. Next
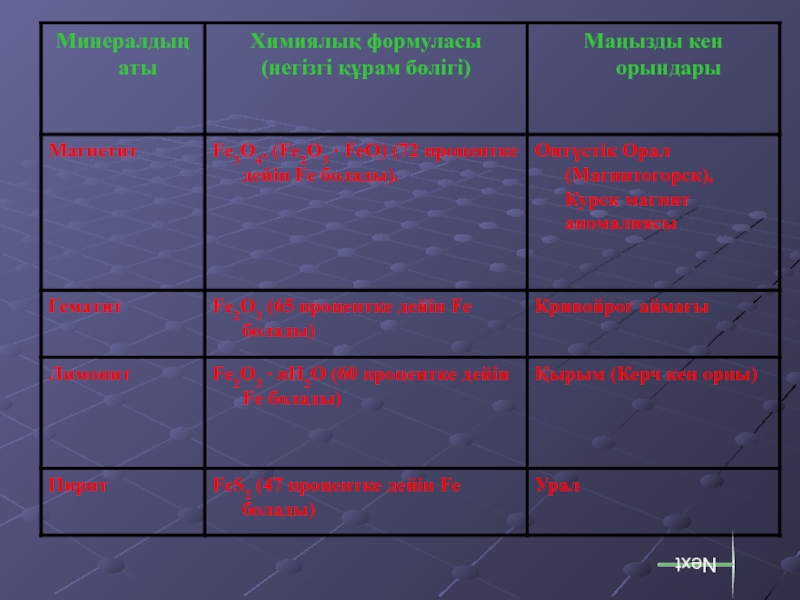
- 8. Минералдар:Магнетит Гематит Next
- 9. Лимонит Пирит
- 10. Қазақстанда темірдің бай қоры бар, ол Торғай
- 11. Өнеркәсіпте алынуы:Темірді 3 түрлі әдіспен алуға болады:Пирометаллургиялық
- 12. Физикалық қасиеттері: Темір – жылтыр, күміс түстес ақ
- 13. Химиялық қасиеттері:I. Жай заттармен әрекеттесуі:Темір оттекте жанғанда
- 14. Ылғалды ауада тат түзеді: 4Fe + 2H2O +
- 15. II. Күрделі заттармен әрекеттесуі:Қатты қыздырылған темір су
- 16. Темірдің маңызды қосылыстары:Темір (ІІ) оксиді немесе (FeO)
- 17. Темір (ІІІ) оксиді Fe2O3 – амфотерлі оксид,
- 18. Темірдің гидроксидтеріТемірдің ІІ және ІІІ валентті оксидтеріне
- 19. Темірдің маңызды қосылыстарын анықтау:Fe+2 және Fe+3 иондарын
- 20. Қолданылуы:Темір купоросы (FeSO4 ∙ 7H2O) – ағаш
- 21. Ат әбзелдері. Құрамы: темір, күміс және т.б. Ұзындығы 24 см. ХІ ғ-да жасалған. Next
- 22. Ерте кездегі темірден жасалған қайшы. Ұзындығы – 15,5 см. XIV ғасырдың екінші жартысы.Next
- 23. Next
- 24. Балта. Ұзындығы – 16 см. ХІ ғасыр.Next
- 25. Темірден жасалған құлып. Ұзындығы – 8,5 см.ХІІ ғасыр.Next
- 26. Next
- 27. Темірден жасалған әр түрлі қару-жарақтар.Х – ХІІ ғасырлар.Next
- 28. Темірден жасалған кілттерBack
- 29. Құрамында темір бар қосылыстар.Кальций силикаты және темірХром
- 30. Back
- 31. Next
- 32. Next
- 33. Back
- 34. Back
- 35. Back
- 36. Back
- 37. Back
- 38. Темірдің құймалары: Next
- 39. Слайд 39
Слайд 2Мазмұны:
Периодтық жүйедегі орны және атом құрылысы
Табиғатта таралуы
Өнеркәсіпте алынуы
Физикалық қасиеттері
Химиялық қасиеттері
Темірдің маңызды
Қолданылуы
Құрамында темірі бар қосылыстар
Слайд 3Жалпы сипаттама. Периодтық жүйедегі орны және атом құрылысы
Темір – VIIIБ топ
Next
Слайд 5 Темір химиялық реакцияларда 2 немесе 3 электрон беріп, өзінің тұрақты қосылыстарында
Fe0 – 2e Fe2+
Fe0 – 3e Fe3+
Темірдің тотығу дәрежесі +6 (K2FeO4 – калий ферраты) болатын тұрақтылығы төмен қосылыстары белгілі.
Back
Слайд 6Табиғатта таралуы
Темір – табиғатта таралуы бойынша екінші металл. Оның жер қыртысындағы
Темір минералды сулардың құрамына сульфат (FeSO4) және гидрокарбонат Fe(HCO3)2 түрінде кіреді.
Темір тұздары теңіз суларында бар, мұхит түбінде темірге бай табиғи шөгінділер кездеседі.
Next
Слайд 10 Қазақстанда темірдің бай қоры бар, ол Торғай темір кенді бассейнінде және
Темір сульфат және гидрокарбонат түрінде минералды сулардың құрамына кіреді. Темір тұздары теңіз суларында да бар, сол сияқты мұхиттардың түбінде де темірге әжептәуір бай табиғи шөгінділер кездеседі.
Темір тірі организмдерде де болады. Ересек адамның денесінде 4-5 грамм темір бар. Оның 65%-і қандағы гемоглобиннің құрамына кіреді. Гемоглобин қанға қызыл түс береді және тыныс алу процесінде оттекті әр түрлі ұлпаларға тасымалдайды. Қанның құрамында темірдің жетіспеуі қан азаюына әкеліп, адам денсаулығын әлсіретеді.
Байланысқан күйдегі темір көптеген тағамдық өнімдерде: қара нан, картоп, алма, өрік, қарақұмық жармасында кездеседі. Бұл өнімдерді әркім өзінің тамақтану рационына кіргізіп, қан азаюының алдын алуға тиісті.
Back
Слайд 11Өнеркәсіпте алынуы:
Темірді 3 түрлі әдіспен алуға болады:
Пирометаллургиялық әдіспен:
оксидінен тотықсыздандыру арқылы:
Fe2O3 +
соның ішінде алюминтермиялық әдіспен:
Fe2O3 + 2Al = Al2O3 + 2Fe
және көміртек (ІІ) оксидімен тотықсыздан-дыру арқылы:
Fe3O4 + 4CO = 3Fe + 4CO2
Back
Слайд 12Физикалық қасиеттері:
Темір – жылтыр, күміс түстес ақ металл, оның тығыздығы –
Back
Слайд 13Химиялық қасиеттері:
I. Жай заттармен әрекеттесуі:
Темір оттекте жанғанда екі тотығу дәрежесін де
3Fe + 2O2 = Fe3O4
Next
Слайд 14Ылғалды ауада тат түзеді:
4Fe + 2H2O + 3O2 = 4FeO(OH)
Белсенді бейметалдар
2Fe + 3Cl2 = 2Fe3+ Cl3-
Fe + S = FeS
3Fe + C = Fe3C
Next
Слайд 15II. Күрделі заттармен әрекеттесуі:
Қатты қыздырылған темір су буымен әрекеттеседі:
Fe + H2O
Концентрлі азот және күкірт қышқылдарында темір енжарланады, өйткені ерімейтін қосылыстардың қорғағыш қабатшасымен қапталады.
Сұйылтылған азот және күкірт қышқылдарымен әрекеттесіп, темір тотықсызданады:
Fe + 4HNO3(сұйық) = Fe(NO3)3 + NO + 2H2O
Fe + H2SO4(сұйық) = FeSO4 + H2
Темір белсенділігі төмен металдарды олардың тұздарынан тотықсыздандырып, ығыстырып шығарады:
Fe + CuCl2 = FeCl2 + Cu
Back
Слайд 16Темірдің маңызды қосылыстары:
Темір (ІІ) оксиді немесе (FeO) – негіздік оксид, оңай
Fe2O3 + CO 2FeO + CO2
Қышқылдармен және қышқылдық оксидтермен әрекеттесіп тұз түзеді:
FeO + 2HCl = FeCl2 + H2O
FeO + CO2 = FeCO3
Next
Слайд 17Темір (ІІІ) оксиді Fe2O3 – амфотерлі оксид, бірақ негіздік қасиеті басымдау,
І. Алынуы: 1) 2Fe(OH)3 = Fe2O3 + 3H2O
2) 3Fe + 2O2 = Fe3O4
3) 3Fe + 4HOH = Fe3O4 + 4H2
ІІ. Химиялық қасиеттері:
қышқылмен Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
қышқылдық оксидпен Fe2O3 + 3SO3 = Fe2(SO4)3
негізбен Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Next
Слайд 18Темірдің гидроксидтері
Темірдің ІІ және ІІІ валентті оксидтеріне екі түрлі гидроксидтері сәйкес
Fe (II) гидроксиді – ақ түсті, ал Fe (III) гидроксиді – қызыл-қоңыр түсті. Олар суда ерімейтін заттар.
І. Алынуы. FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl
FeCl3 + 2NaOH = Fe(OH)3 + 3NaCl
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
Next
Слайд 19Темірдің маңызды қосылыстарын анықтау:
Fe+2 және Fe+3 иондарын сары және қызыл қан
3FeCl2 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2 + 6KCl
турунбул көгі
4FeCl3 + 3K4[Fe(CN)6] = Fe4[Fe(CN)6]3 + 12KCl
берлин көгі
Back
Слайд 20Қолданылуы:
Темір купоросы (FeSO4 ∙ 7H2O) – ағаш сүрлеуде;
Fe3C – цементит шойында
(NH4)2SO4 ∙ FeSO4 ∙ 6H2O – Мор тұзы, тотықсыздандырғыш ретінде пайдаланылады.
Fe(NH4)2 ∙ (SO4)2 ∙ 12H2O – темір-аммонийлі ашудас, тері илеуде қолданылады.
Fe2O3 – темір сүрегі (бояу) шатырларды бояуда, болат пен шыны беттерін тегістеуде, термиялық пісіруде қолданылады.
Next
Слайд 29Құрамында темір бар қосылыстар.
Кальций силикаты
және темір
Хром және темір
қосылыстары
Темір, ванадий
Темір, марганец
және стронций
Темір және
алюминий қосылысы
Құрамында 9%-дық
темірі бар қоспа
Next

















![Темір оның қосылыстары және физикалық қасиеттері Темірдің маңызды қосылыстарын анықтау:Fe+2 және Fe+3 иондарын сары және қызыл қан Темірдің маңызды қосылыстарын анықтау:Fe+2 және Fe+3 иондарын сары және қызыл қан тұздарының көмегімен анықтайды.3FeCl2 + 2K3[Fe(CN)6] =](/img/tmb/1/46296/78c2e87db5399b7191a7fb8e3a84aa5e-800x.jpg)

























