- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Решение задач на растворы
Содержание
- 1. Решение задач на растворы
- 2. изучить возможные способы решения задач по химии
- 3. отработать навыки решения задач с использованием конверта
- 4. Использование альтернативных способов решения задач по химии
- 5. Физиологический раствор – 0,9 % NaCl в
- 6. 5 % = 0,05 10 % = 0,1 20
- 7. Как найти % от числа? Чтобы найти
- 8. Ответ: m р.в.= m раств.· ω р.в =
- 9. Какой объем Н2О нужно прилить к 16
- 10. Если обозначить массу первого раствора через m1,
- 11. m1• ω1 + m2•ω2 = = ω3•(m1+m2)Отсюдаm1(ω1
- 12. М (CuSO4· 5Н2О)= 160 + 90 =
- 13. m раств. = 16 г + 1008
- 14. Какую массу 3 % раствора нужно прилить
- 15. Решение: m 3% раств. = 100 г- 1 часть – 50 г- 2 части – 100 г
- 16. 50 г 30% р-ра содержит 15 г Н2О100
- 17. Смешали 220 г 5% раствора и
- 18. Составляем пропорцию и решаем уравнение: X –
- 19. Имеется 2 сплава, в одном из которых
- 20. Решение Пусть к 24 кг первого сплава нужно
- 21. Составим и решим уравнение: 9,6 + 0,2х
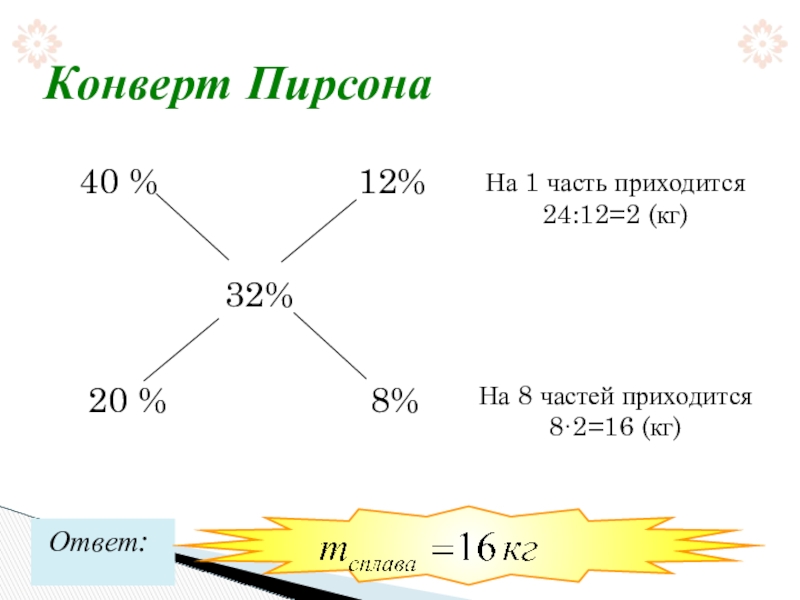
- 22. Конверт ПирсонаНа 1 часть приходится 24:12=2 (кг)На 8 частей приходится 8·2=16 (кг)Ответ:
- 23. К 10%-ному раствору соли
- 24. Пусть добавили х л 5%-ного раствора
- 25. Составим и решим уравнение. 1,5 +
- 26. Конверт Пирсона Всего 5 частейНа 1 часть приходится 20:5=4 (л)Ответ:
- 27. Какой будет массовая доля раствора нитратной кислоты,
- 28. Спасибо за внимание!
Слайд 1Творческая лаборатория
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ РЕШЕНИЕ ЗАДАЧ ПО ХИМИИ
ПО ПРАВИЛУ КРЕСТА
(КОНВЕРТ ПИРСОНА)
Глухова
Красногвардейская ОШ №1
Слайд 2изучить возможные способы решения задач по химии с использованием математических приёмов.
рассмотреть наиболее эффективные способы решения задач.
Задачи:
Слайд 3
отработать навыки решения задач с использованием конверта Пирсона (правила креста)
систематизировать типичные
Слайд 4Использование альтернативных способов решения задач по химии и математике.
Умение ориентироваться
Необходимый минимум для успешного обучения в высших учебных заведениях, подготовка к ГИА и ВНО.
Практическая значимость:
Слайд 5
Физиологический раствор – 0,9 % NaCl в дистиллированной воде Н2О.
Как приготовить
Задача №1
Слайд 6
5 % = 0,05
10 % = 0,1
20 % = 0,2
38 %
130%= 1,3
Повторение:
ПЕРЕВОД ПРОЦЕНТОВ В ДЕСЯТИЧНУЮ ДРОБЬ
Слайд 7
Как найти % от числа?
Чтобы найти процент от данного числа,
Найти 0,9% от 2 кг.
0,9%=0,009,
Значит: 2000 г · 0,009 = 18 г
Повторение:
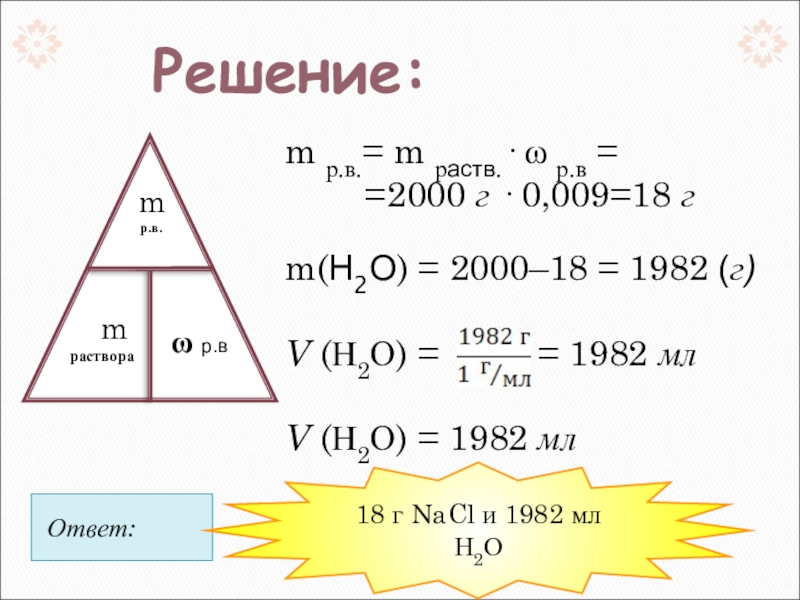
Слайд 8Ответ:
m р.в.= m раств.· ω р.в =
=2000 г · 0,009=18
m(Н2О) = 2000–18 = 1982 (г)
V (Н2О) = = 1982 мл
V (Н2О) = 1982 мл
Решение:
18 г NaCl и 1982 мл Н2О
Слайд 9
Какой объем Н2О нужно прилить к 16 г медного купороса, чтобы
1 % - ный раствор для обработки растений?
Задача № 2
Слайд 10
Если обозначить массу первого раствора через m1, а второго – через
Пусть массовая доля растворенного вещества в І растворе – ω1, во ІІ – ω2, а в их смеси – ω3.
Справка:
КОНВЕРТ ПИРСОНА
(МЕТОД КРЕСТА)
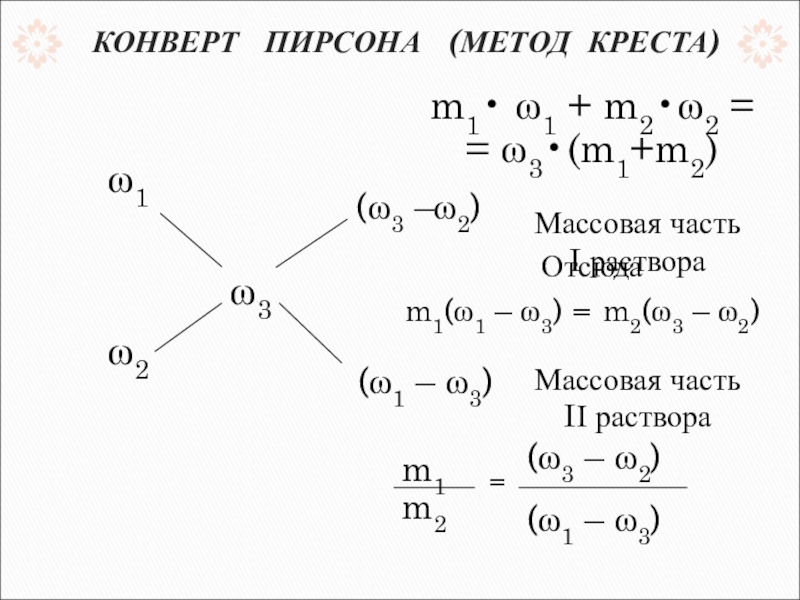
Слайд 11m1• ω1 + m2•ω2 =
= ω3•(m1+m2)
Отсюда
m1(ω1 – ω3) = m2(ω3
=
КОНВЕРТ ПИРСОНА (МЕТОД КРЕСТА)
m1
m2
(ω3 – ω2)
(ω1 – ω3)
Массовая часть
I раствора
Массовая часть
IІ раствора
Слайд 12
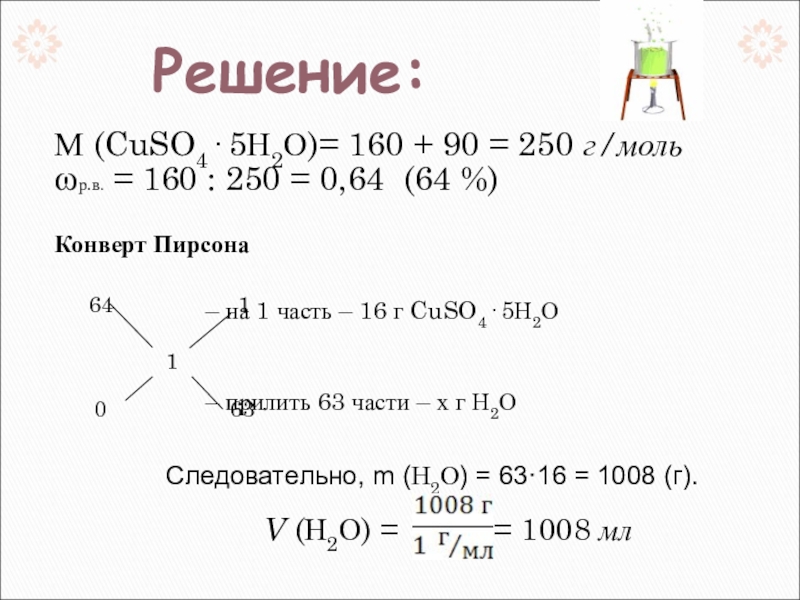
М (CuSO4· 5Н2О)= 160 + 90 = 250 г/моль
ωр.в. = 160
Конверт Пирсона
– на 1 часть – 16 г CuSO4· 5Н2О
– прилить 63 части – х г Н2О
Следовательно, m (Н2О) = 63·16 = 1008 (г).
Решение:
V (Н2О) = = 1008 мл
Слайд 13
m раств. = 16 г + 1008 г = 1024 г
250
16 г х
х = m р.в.= = 10,24 г
ω = = 0,01 или 1%
Проверка:
16 · 160
250
10,24 г
1024 г
Ответ:
1008 мл Н2О
Слайд 14
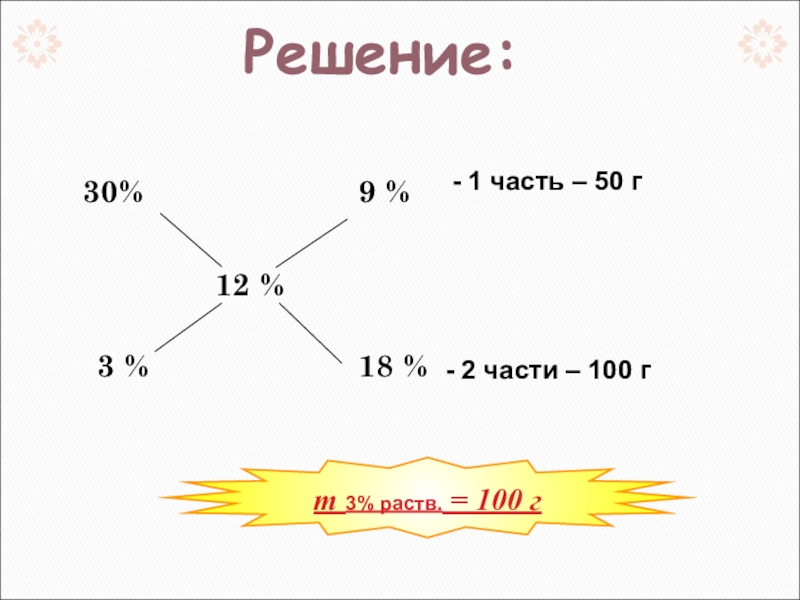
Какую массу 3 % раствора нужно прилить к 50 г 30%
Задача №3
Слайд 16
50 г 30% р-ра содержит 15 г Н2О
100 г 3 % р-р
m раств. = 50 + 100 = 150 (г)
m р.в.= 15 + 3 = 18 (г)
ω = = 0,12 или 12 %
Проверка:
Ответ:
100 г
18 г
150 г
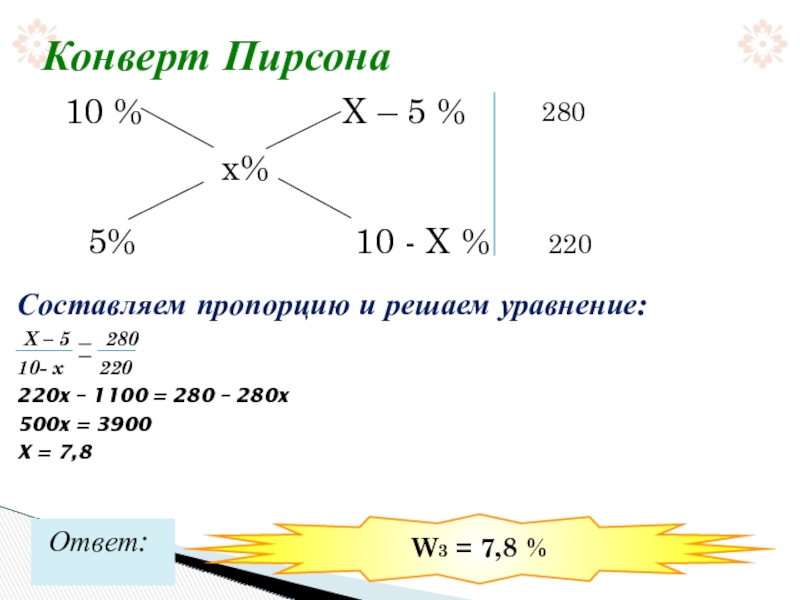
Слайд 17 Смешали 220 г 5% раствора и 280 г 10 % раствора
Задача №4
Слайд 18Составляем пропорцию и решаем уравнение:
X – 5 280
10- x 220
220x – 1100 = 280 – 280x
500x = 3900
X = 7,8
Конверт Пирсона
280
220
Ответ:
W3 = 7,8 %
Слайд 19
Имеется 2 сплава, в одном из которых содержится 40%, а в
Мастер – класс
Задача № 1
Слайд 20Решение
Пусть к 24 кг первого сплава нужно добавить х кг второго
В 24 кг первого сплава содержится:
0,4·24 = 9,6 (кг) серебра, в х кг второго сплава содержится 0,2х кг серебра, а в (24+х) кг нового сплава содержится 0,32·(24+х) кг серебра.
Решение:
Слайд 21 Составим и решим уравнение:
9,6 + 0,2х = 0,32·(24 +х);
9,6 +
1,92 = 0,12х
х = 1,92 : 0,12
Ответ:
16 кг второго сплава
х = 16
Решение:
Слайд 23 К 10%-ному раствору соли добавили 5%-ный раствор соли
Задача № 2
Слайд 24 Пусть добавили х л 5%-ного раствора соли,
в х л 5%-ного
0,05х (л) соли.
Второго 10%-ного раствора добавили
(20 – х) л , а в нём содержится
(20 – х)· 0,1 = 2 – 0,1х (л) соли
Нового раствора – 20 л, в котором содержится 0,08·20 = 1,6 л соли.
,
Решение:
Слайд 25 Составим и решим уравнение.
1,5 + 0,05х = 0,08 ·(15
1,5 + 0,05х = 1,2 + 0,08 х
0,03х =0,3
х = 0,3 : 0,03
Решение:
Ответ:
10 л 5%-ного раствора
х = 10
Слайд 27Какой будет массовая доля раствора нитратной кислоты, если к 40 мл
Задача № 3