- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад урока химии Классификация веществ (11 класс)
Содержание
- 1. Презентация урока химии Классификация веществ (11 класс)
- 2. Цели урокаОбобщить знания учащихся о классах неорганических
- 3. Классификация неорганических веществ
- 4. Оксиды ЭаОс - ?
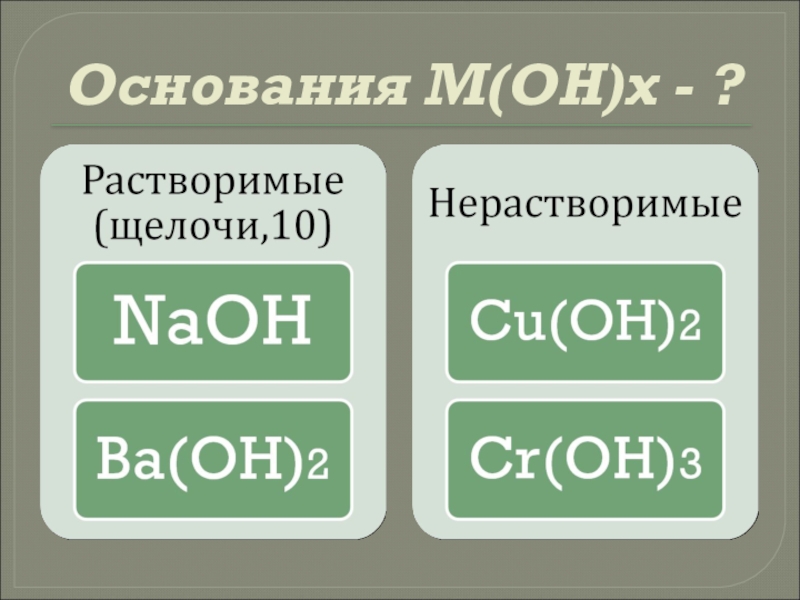
- 5. Основания М(ОН)x - ?
- 6. Амфотерные гидроксиды проявляют и свойства
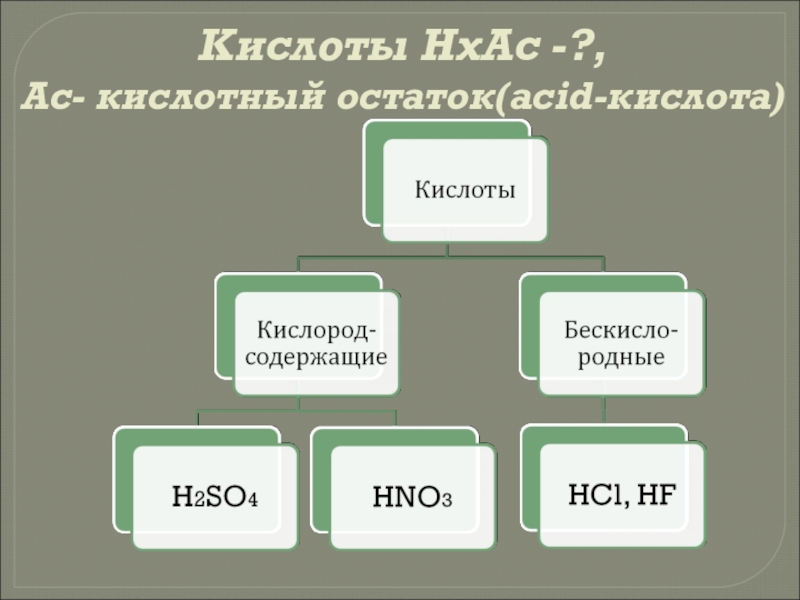
- 7. Кислоты НxАс -?, Ас- кислотный остаток(acid-кислота)
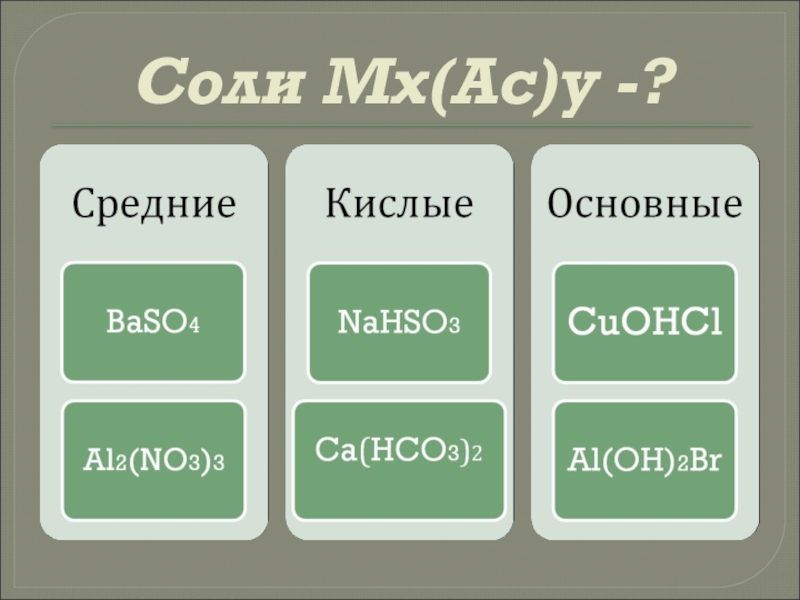
- 8. Соли Мx(Ас)y -?
- 9. Классификация органических веществ
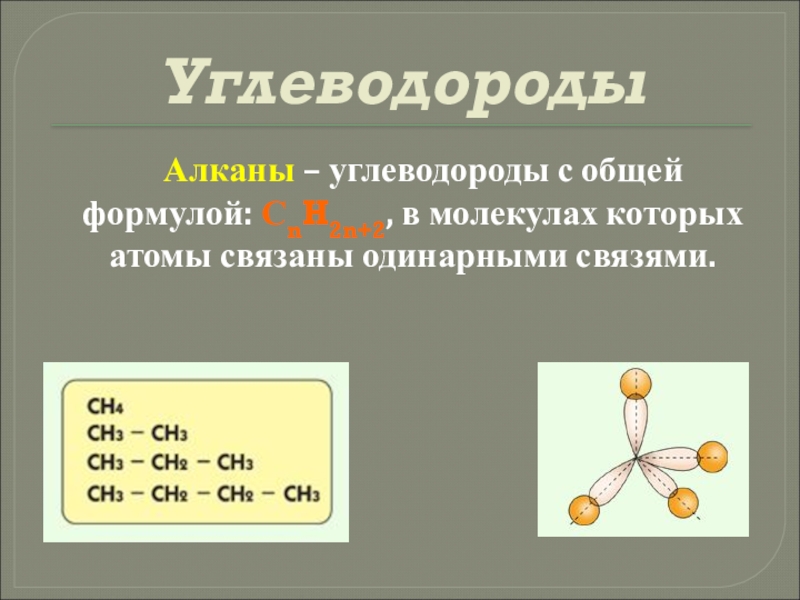
- 10. Углеводороды Алканы – углеводороды с
- 11. Алкены (этиленовые углеводороды, олефины) –
- 12. Алкадиены – это соединения с двумя двойными
- 13. Алкины – непредельные
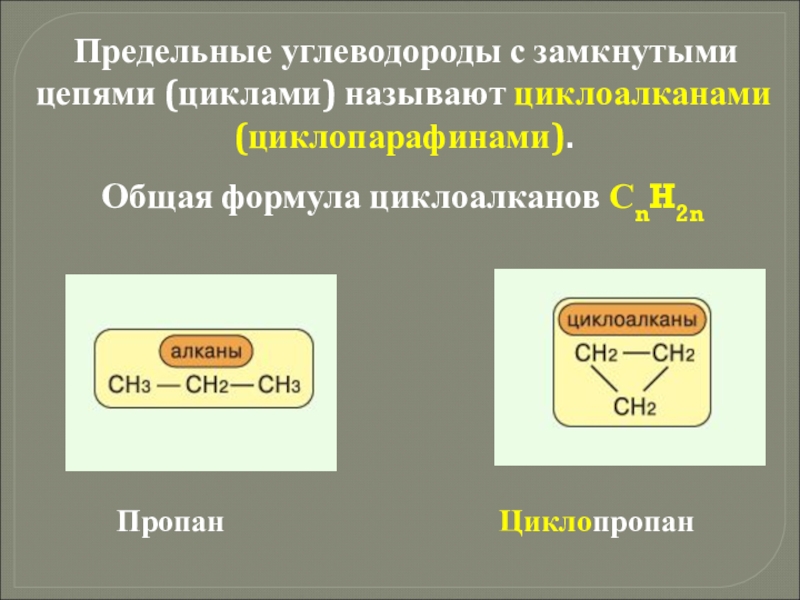
- 14. Предельные углеводороды с замкнутыми цепями
- 15. Слайд 15
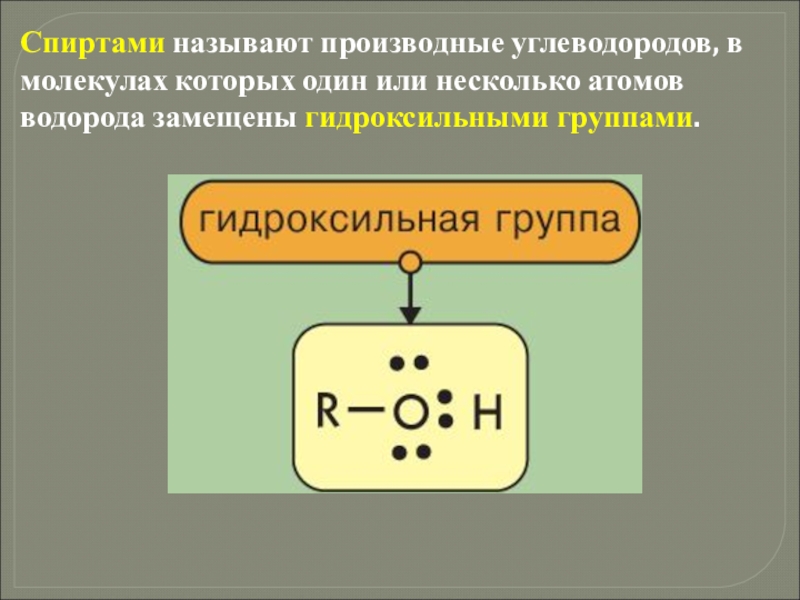
- 16. Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами.
- 17. По числу гидроксильных групп
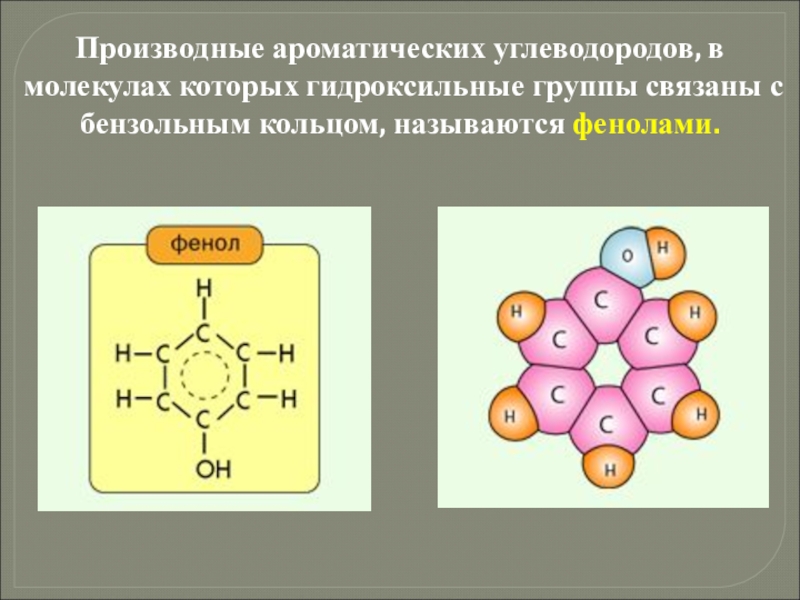
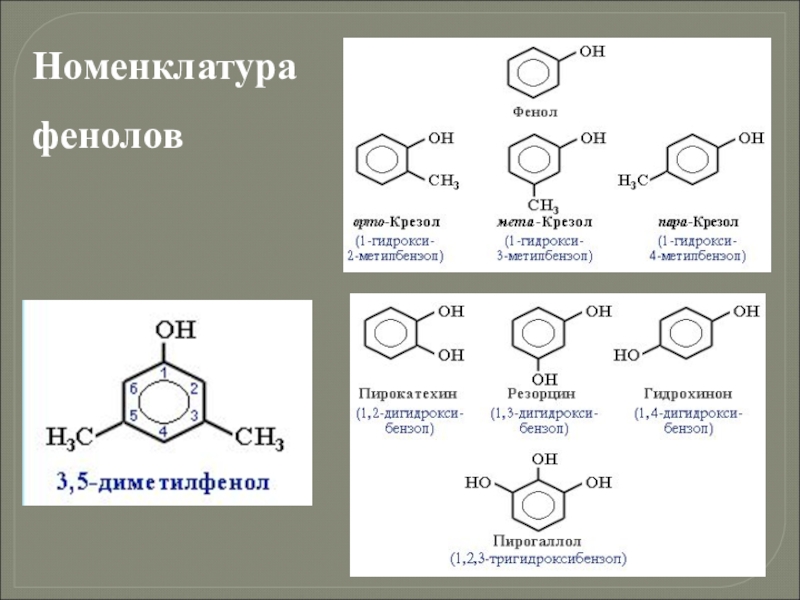
- 18. Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным кольцом, называются фенолами.
- 19. Номенклатурафенолов
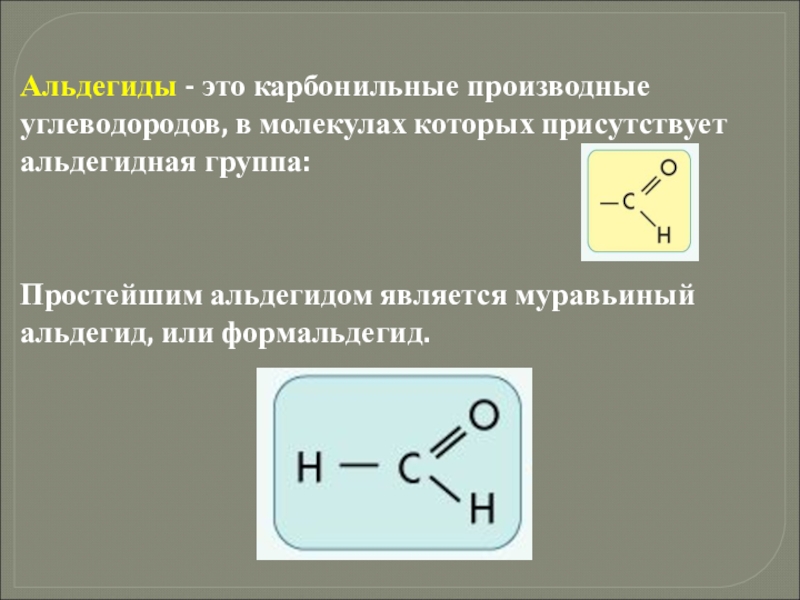
- 20. Альдегиды - это карбонильные производные углеводородов, в
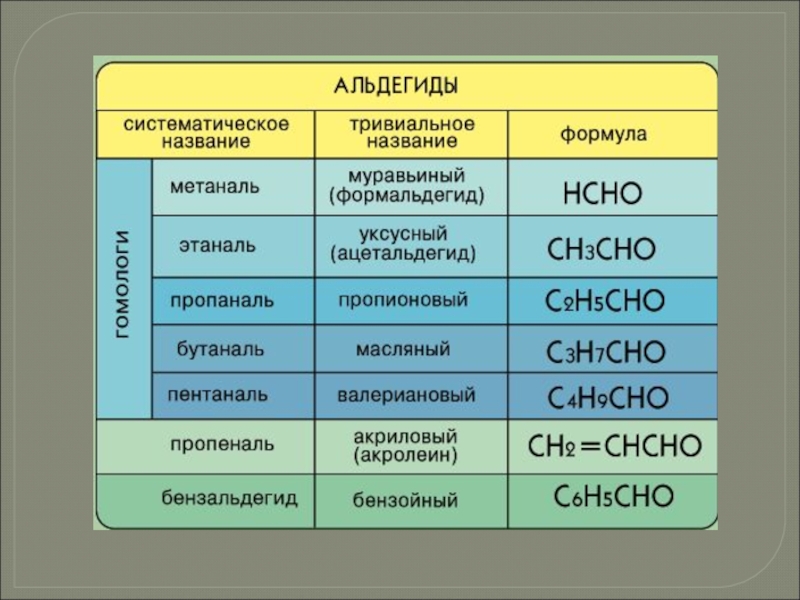
- 21. Слайд 21
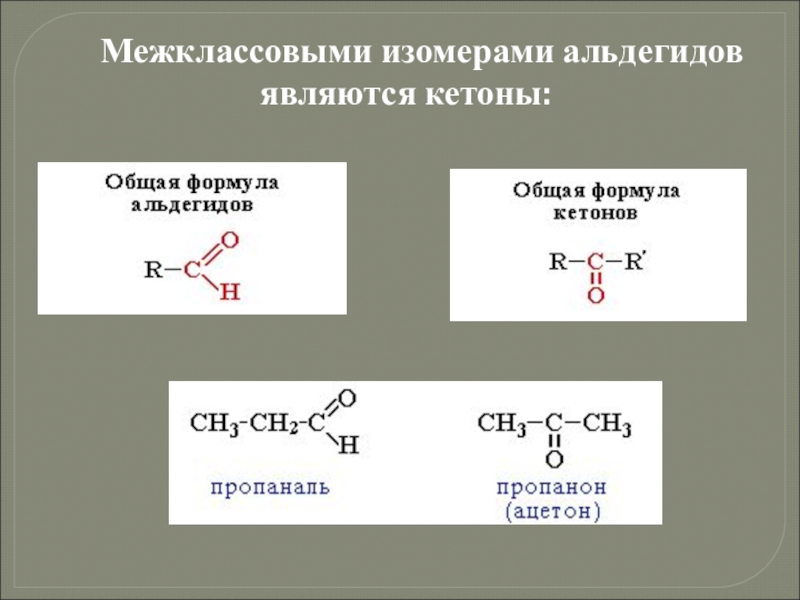
- 22. Межклассовыми изомерами альдегидов являются кетоны:
- 23. Карбоновые кислоты – это сложные органические вещества,
- 24. Простые эфиры Простые эфиры – органические
- 25. Сложными эфирами называются производные кислородосодержащих кислот, в
- 26. Свойства эфиров Сложные эфиры представляют собой легковоспламеняющиеся
- 27. Слайд 27
- 28. Жиры - это сложные эфиры трехатомного спирта
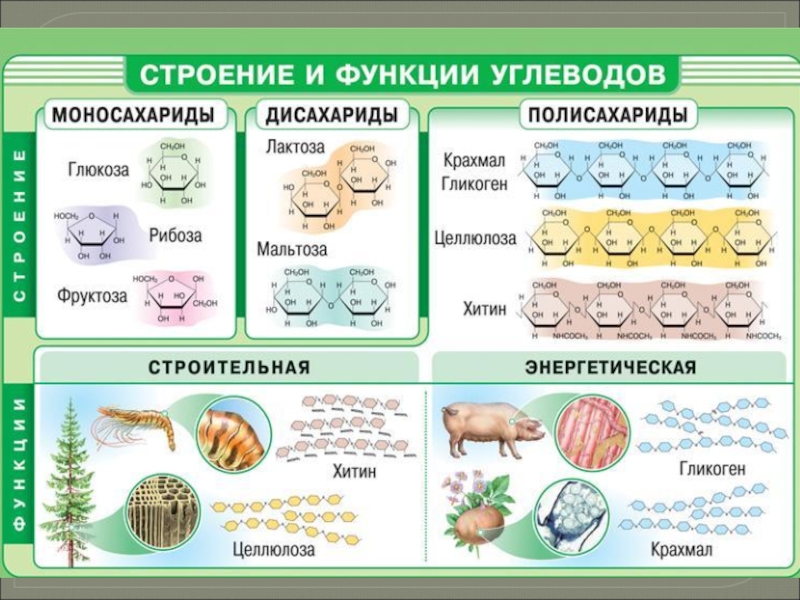
- 29. Углеводы (сахара) - органические вещества, составкоторых выражается
- 30. Слайд 30
- 31. Азотсодержащие соединения
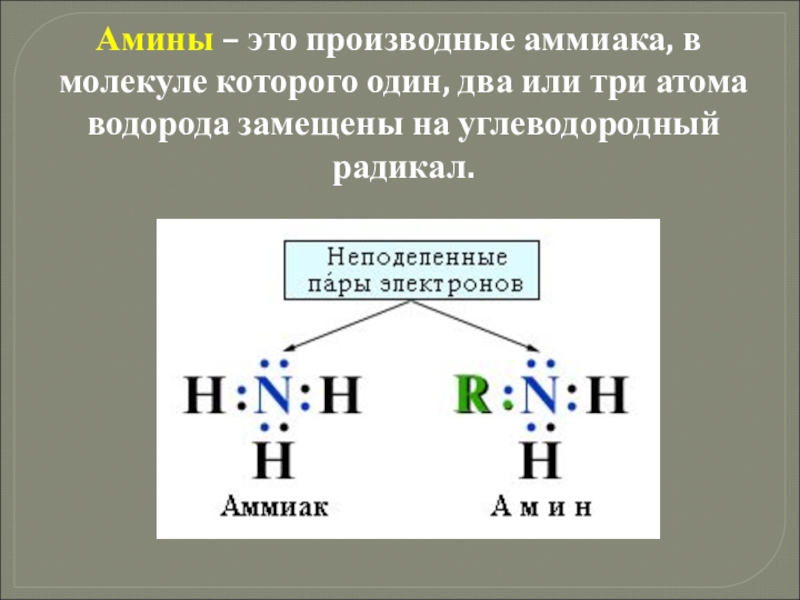
- 32. Амины – это производные аммиака, в
- 33. Номенклатура аминов
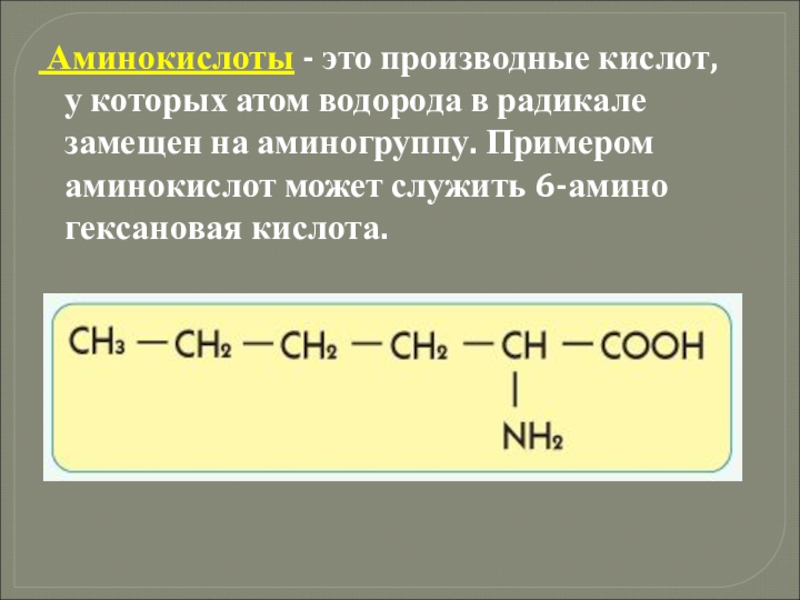
- 34. Аминокислоты - это производные кислот, у
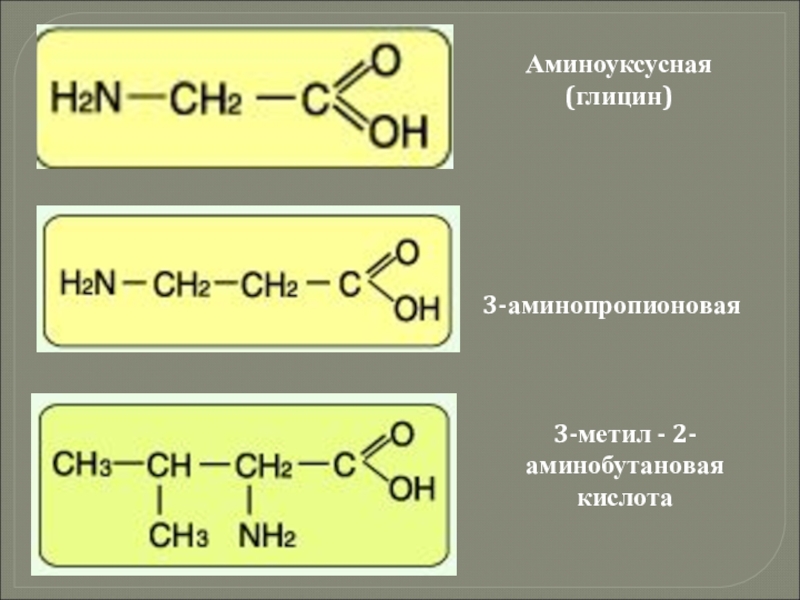
- 35. Аминоуксусная (глицин)3-аминопропионовая 3-метил - 2-аминобутановая кислота
- 36. В зависимости от положения аминогруппы относительно карбоксильной
- 37. Белки (полипептиды) − биополимеры, построенные
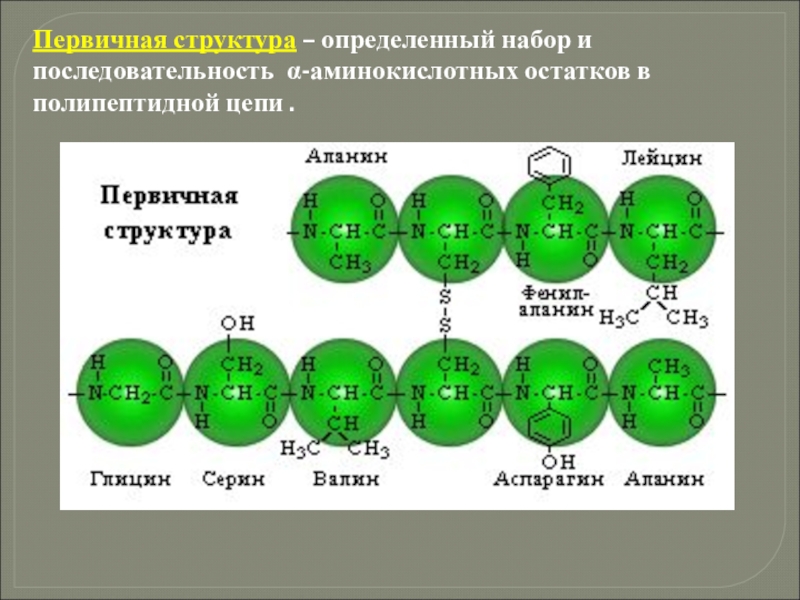
- 38. Первичная структура – определенный набор и последовательность α-аминокислотных остатков в полипептидной цепи .
- 39. Слайд 39
- 40. Слайд 40
- 41. Слайд 41
- 42. Слайд 42
- 43. Макромолекула ДНК представляет собой две параллельные неразветвленные
- 44. Слайд 44
- 45. Способность ДНК не только хранить, но и
- 46. Изомерия Явление изомерии состоит в
- 47. Слайд 47
- 48. ЗакреплениеНапишите структурные формулы состава С4Н10О.Какие вещества имеют
- 49. Домашнее задание § 25, упражнения 1 -3
Слайд 2Цели урока
Обобщить знания учащихся о классах неорганических и органических соединений.
Продолжить формирование
Установить взаимосвязь строения и свойств веществ.
Слайд 3
Классификация
неорганических веществ
Простые вещества состоят из атомов одного химического
Сложные вещества состоят из
атомов разных элементов,
химически связанных
друг с другом.
Слайд 6 Амфотерные гидроксиды проявляют и свойства кислот и оснований, поэтому
Zn(OH)2 или H2ZnO2 –гидроксид цинка
Be(OH)2 или H2BeO2 – гидроксид бериллия
AL(OH)3 или H3AlO3 – гидроксид алюминия
Слайд 10Углеводороды
Алканы – углеводороды с общей формулой: СnH2n+2, в
Слайд 11 Алкены (этиленовые углеводороды, олефины) – непредельные алифатические углеводороды, молекулы
Общая формула ряда алкенов СnH2n
С2Н4 С3Н6 С4Н8
СН2=СН2 СН2=СН–СН3 СН2=СН–СН2–СН3
этилен пропилен бутилен-1
(этен) (пропен) (бутен-1)
Слайд 12
Алкадиены – это соединения с двумя двойными связями. Общая формула алкадиенов
СН2=СН–СН=СН2 бутадиен-1,3
Слайд 13
Алкины – непредельные углеводороды с общей
Простейший представитель –ацетилен
С2Н2
Слайд 14 Предельные углеводороды с замкнутыми цепями (циклами) называют циклоалканами (циклопарафинами).
Пропан Циклопропан
Слайд 15
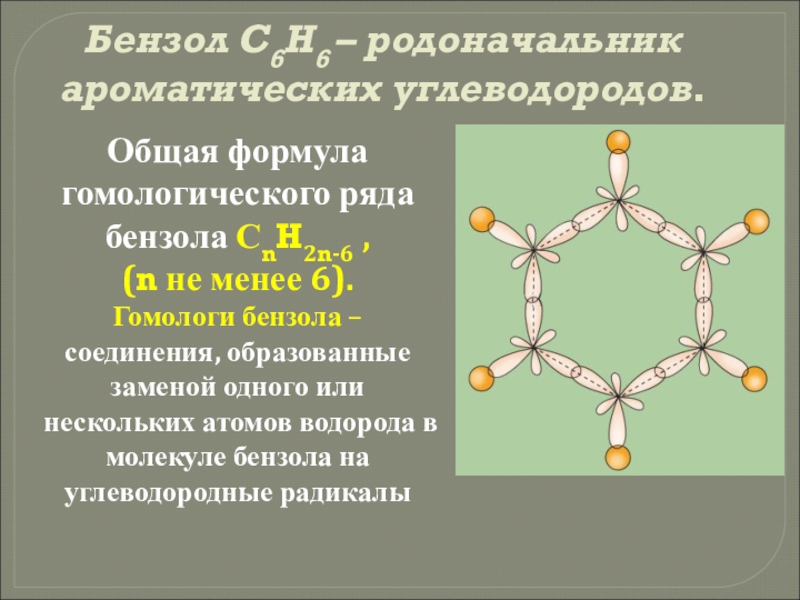
Бензол С6Н6 – родоначальник ароматических углеводородов.
Общая формула гомологического ряда бензола СnH2n-6
(n не менее 6).
Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы
Слайд 16Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов
Слайд 17 По числу гидроксильных групп спирты подразделяются на одноатомные
двухатомный спирт – этиленгликоль (этандиол-1,2)
HO–СH2–CH2–OH
трехатомный спирт – глицерин (пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
По строению радикалов, связанных с атомом кислорода
различают спирты:
предельные, или алканолы (например, СH3CH2–OH)
непредельные, или алкенолы (CH2=CH–CH2–OH)
ароматические (C6H5CH2–OH).
Слайд 18Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным
Слайд 20
Альдегиды - это карбонильные производные углеводородов, в молекулах которых присутствует альдегидная
Простейшим альдегидом является муравьиный альдегид, или формальдегид.
Слайд 23Карбоновые кислоты – это сложные органические вещества, в которых углеводородный радикал
Кислоты классифицируют
По радикалу: По количеству
карбоксильных групп
Предельные - одноосновные
Непредельные - двухосновные
Ароматические - многоосновные
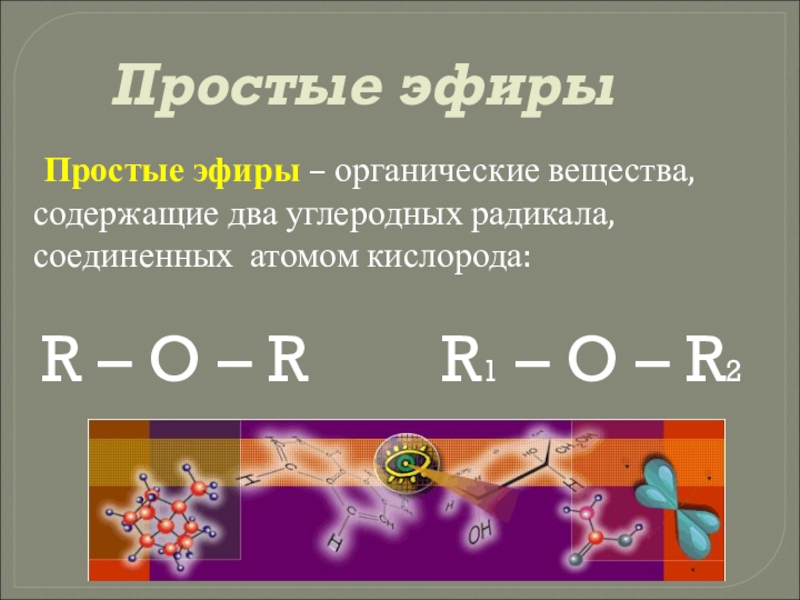
Слайд 24Простые эфиры
Простые эфиры – органические вещества, содержащие два углеродных
R – O – R R1 – O – R2
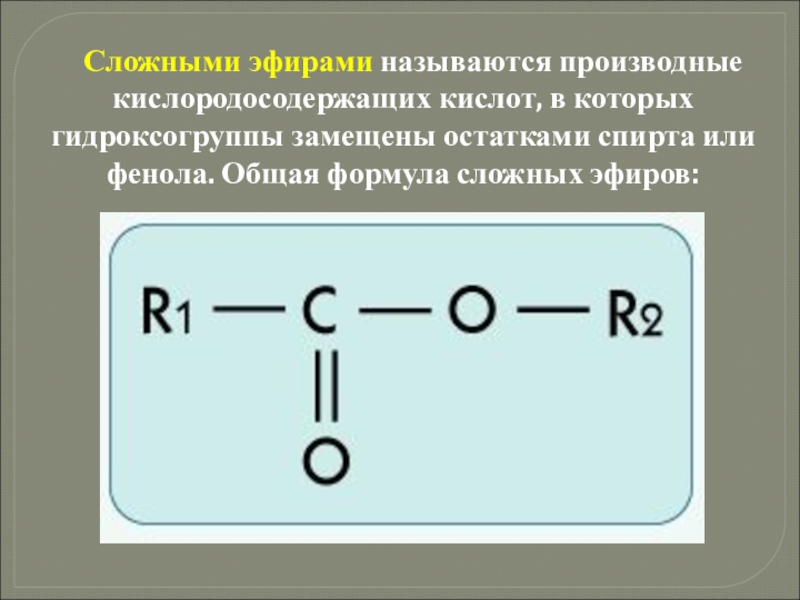
Слайд 25Сложными эфирами называются производные кислородосодержащих кислот, в которых гидроксогруппы замещены остатками
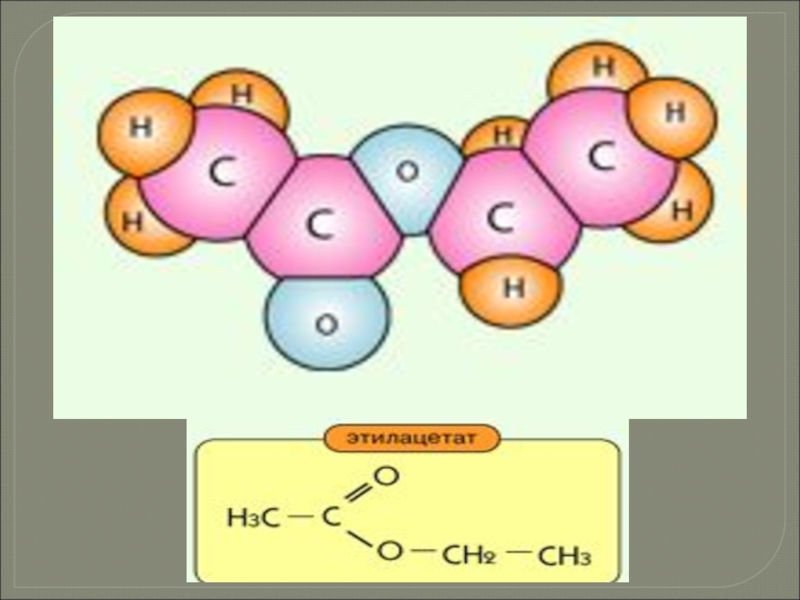
Слайд 26Свойства эфиров
Сложные эфиры представляют собой легковоспламеняющиеся жидкости с невысокими температурами
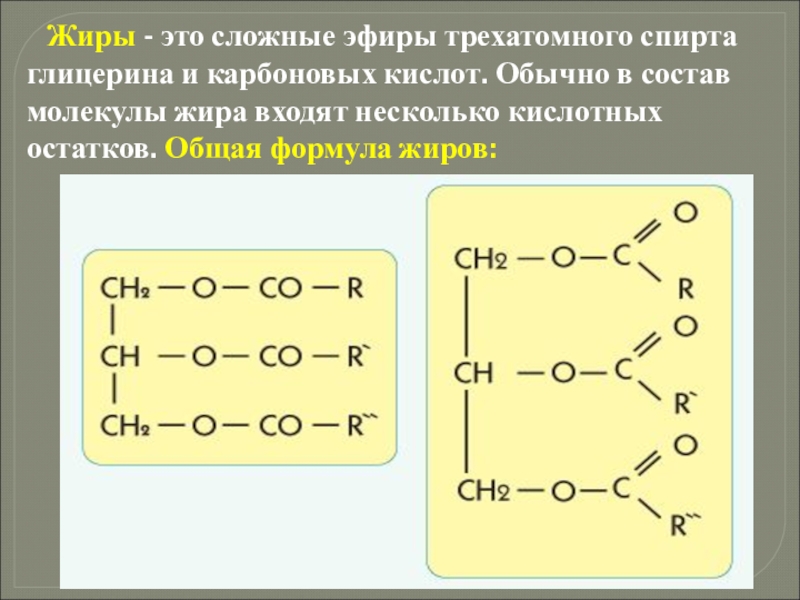
Слайд 28Жиры - это сложные эфиры трехатомного спирта глицерина и карбоновых кислот.
Слайд 29Углеводы (сахара) - органические вещества, состав
которых выражается формулой
Cx(H2O)y, где x
По способности к гидролизу углеводы делятся на две группы:
простые и сложные
моносахариды; олигосахариды и полисахариды
Углеводы образуются растениями в процессе фотосинтеза из углекислого газа и воды.
ФОТОСИНТЕЗ:
xCO2 + yH2O + энергия → Cx(H2O)y + xO2
углеводы
Слайд 32 Амины – это производные аммиака, в молекуле которого один, два
Слайд 34 Аминокислоты - это производные кислот, у которых атом водорода в
Слайд 36В зависимости от положения аминогруппы относительно карбоксильной группы, различают α-, β-,
В состав белков входят только α- аминокислоты.
α-аминокислоты очень распространены в природе, так как являются составными частями молекул белка и основой жизни на Земле.
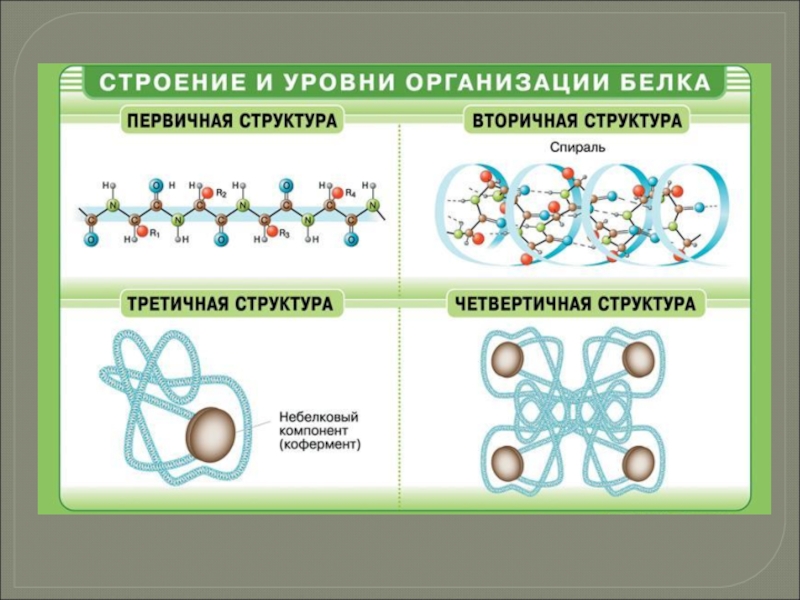
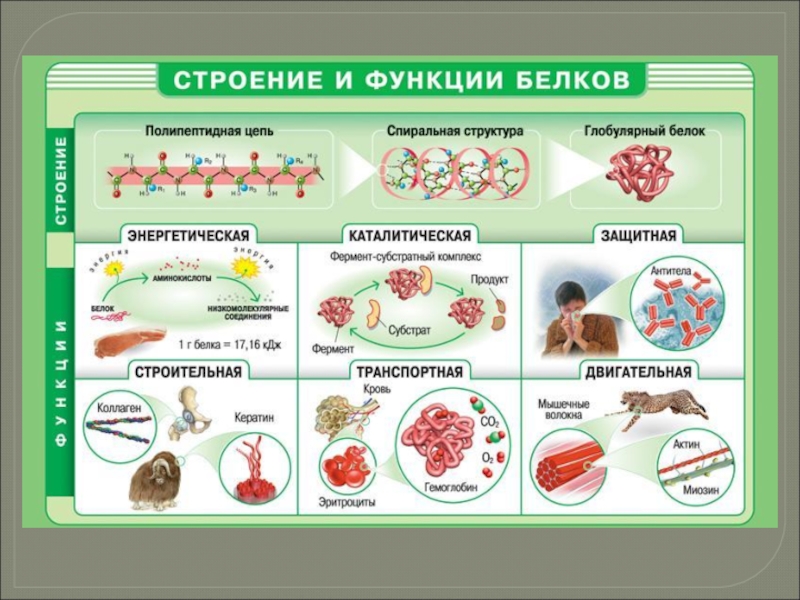
Слайд 37 Белки (полипептиды) − биополимеры, построенные из остатков α-аминокислот, соединенных
Пептидной связью называют амидную связь –CO–NH–, образованную при взаимодействии α-аминокислот за счет реакции между аминогруппой - NH2 одной молекулы и карбоксильной группы -COOH – другой.
Слайд 38Первичная структура – определенный набор и последовательность α-аминокислотных остатков в полипептидной
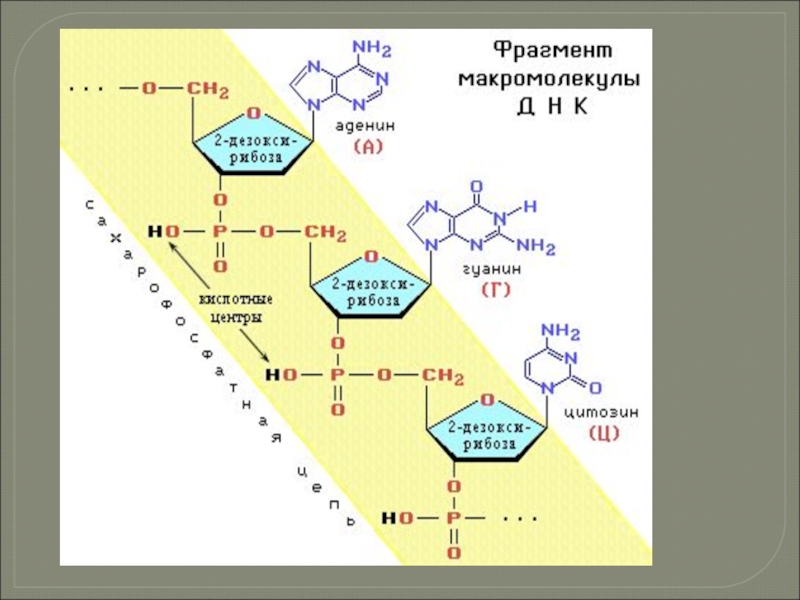
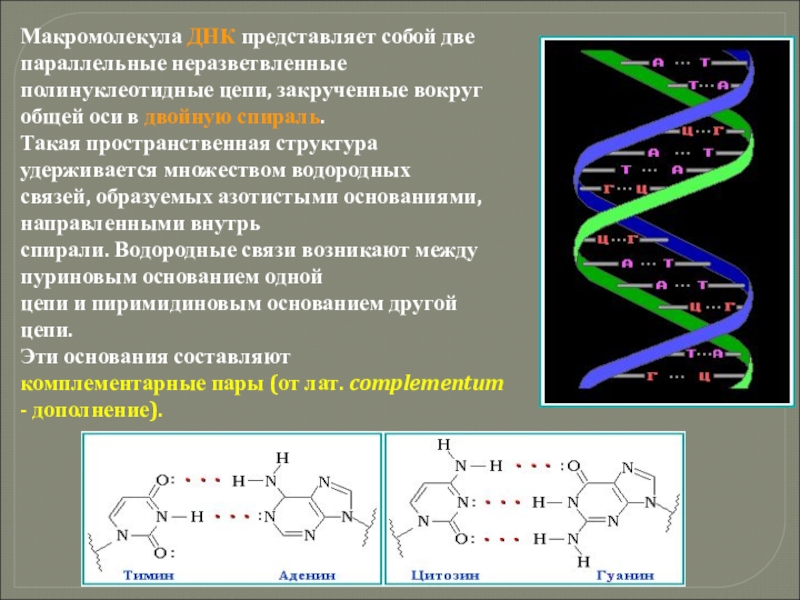
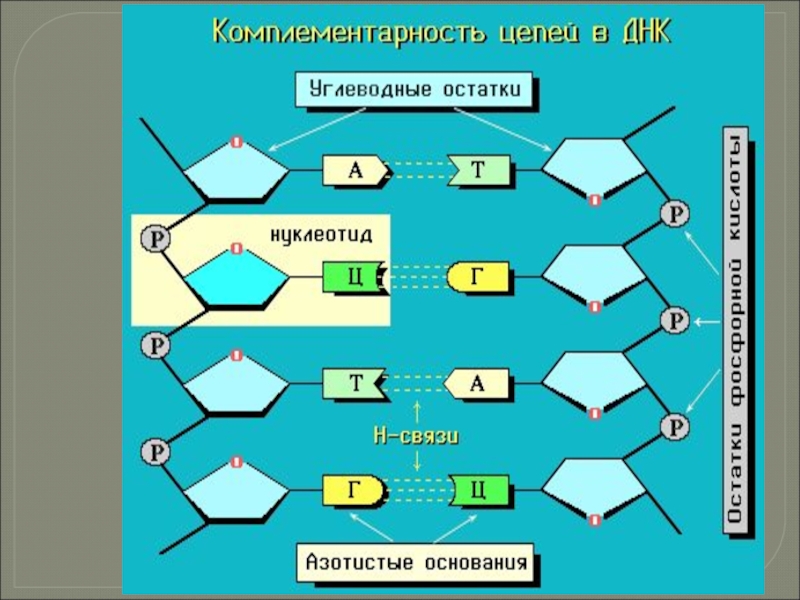
Слайд 43Макромолекула ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг
Такая пространственная структура удерживается множеством водородных
связей, образуемых азотистыми основаниями, направленными внутрь
спирали. Водородные связи возникают между пуриновым основанием одной
цепи и пиримидиновым основанием другой цепи.
Эти основания составляют
комплементарные пары (от лат. complementum - дополнение).
Слайд 45Способность ДНК не только хранить, но и использовать генетическую информацию определяется
1. Молекулы ДНК способны к репликации (удвоению), т.е. могут обеспечить
возможность синтеза других молекул ДНК, идентичных исходным .
2. Молекулы ДНК могут направлять совершенно точным и определенным
образом синтез белков, специфичных для организмов данного вида.
Слайд 46Изомерия
Явление изомерии состоит в том, что могут существовать
Слайд 47 Структурная изомерия
СН2=СН–СН=СН–СН2–СН3 СН3–СН=СН–СН=СН–СН3
гексадиен-1,3 гексадиен-2,4
2. Изомерия углеродного скелета:
СН2=СН–СН=СН–СН3 СН2=С–СН=СН2
пентадиен-1,3 ⏐
СН3
2-метилбутадиен-1,3 (изопрен)
3. Межклассовая изомерия с алкинами и циклоалкенами.
Например, формуле С4Н6 соответствуют следующие соединения:
СН = СН
СН2=СН–СН=СН2 СН≡С–СН2–СН3 ⏐ ⏐
СН2 –СН2
бутадиен-1,3 бутин-1 циклобутен
4.Пространственная изомерия -?
Слайд 48Закрепление
Напишите структурные формулы состава С4Н10О.
Какие вещества имеют двойственную номенклатуру? Привести примеры
Написать по три примера изомеров и гомологов 4-метил-2-аминогексановой кислоты.