- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад : урок-повторение в форме игры Основные классы неорганических соединений (8 кл.)
Содержание
- 1. Презентация : урок-повторение в форме игры Основные классы неорганических соединений (8 кл.)
- 2. Цель урока: обобщение темы «Основные классы неорганических
- 3. Вопросы разминки №11. Что общего в составе
- 4. 7. Карбонаты – это соли какой кислоты?(
- 5. Вопросы разминки №21. Бинарные соединения, содержащие кислород?(оксиды)2.
- 6. 7. Формула гидроксида алюминия?(Al(OH)₃ )8. Кислотный оксид,
- 7. Вопросы разминки №31. Цвет лакмуса в нейтральной
- 8. 7. Ангидрид фосфорной кислоты?( P₂O₅ )8. Оксиды
- 9. Вопросы разминки №41. Вещества, состоящие из атомов
- 10. 7. Ангидрид соляной кислоты?( не существует)8. Цвет
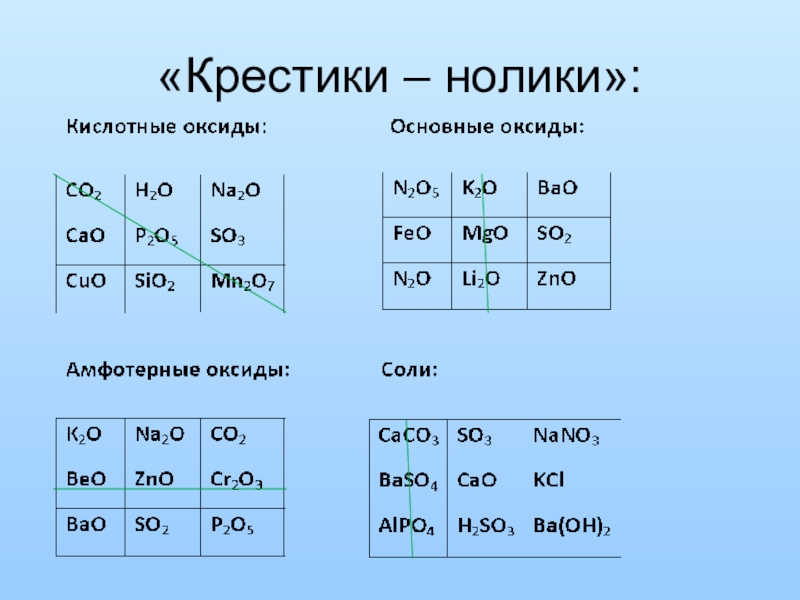
- 11. «Крестики – нолики»:
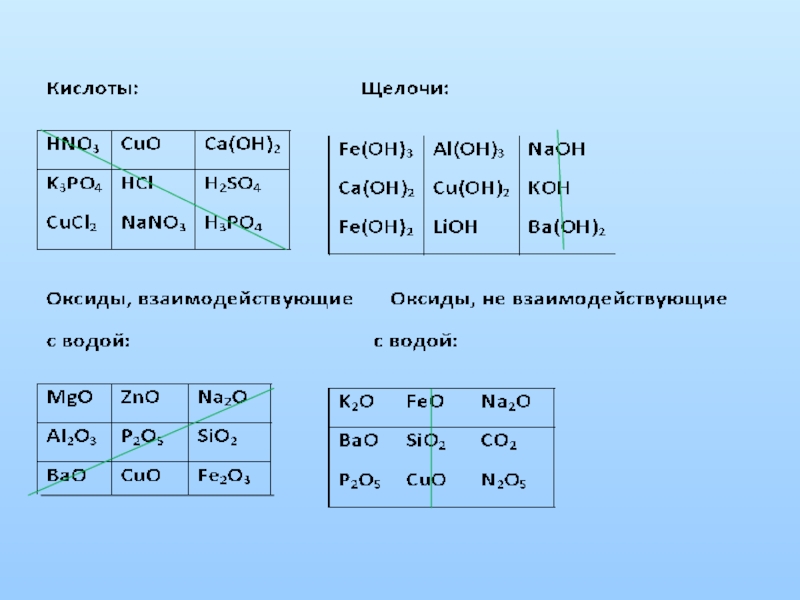
- 12. Слайд 12
- 13. Химическая рыбалкаCu(OH)₂→ CuO + H₂O2Fe(OH)₃→ Fe₂O₃ +
- 14. Демонстрационная цепочка-эксперимент №1 «Генетическая связь между классами
- 15. Демонстрационная цепочка-эксперимент №2 «Генетическая связь между классами
- 16. Задание – эксперимент «Получение хлорида
- 17. Задание – эксперимент «Получение гидроксида
- 18. Задание – эксперимент «Получение сульфата
- 19. Задание – эксперимент «Получение оксида
- 20. Игра «Термины – синонимы»Карбонат натрия
- 21. Тест по теме «Основные классы неорганических соединений».
- 22. 3. Выберите формулу оксида:а) MgO б)
- 23. 5. Выбери соль серной кислоты:а) сульфид меди
- 24. 7. В какой схеме правильно записаны формулы
- 25. 9. Выбери последовательность формул, отражающих генетический ряд
- 26. Домашнее задание:Подготовиться к контрольной работе, повт. §
Слайд 1Урок – повторение в форме игры «Основные классы неорганических соединений»
Казанцева Евгения Андреевна
Учитель химии
МОУ школа №12 г.о. Жуковский
Слайд 2Цель урока: обобщение темы «Основные классы неорганических соединений и подготовка к
Задачи урока:
образовательные: повторение, обобщение и систематизация знаний по теме «Основные классы неорганических соединений»
развивающие: развитие способности к анализу; развитие познавательных способностей, мышления, внимания, умения использовать изученный материал для решения поставленной задачи.
Воспитательные: воспитание самостоятельности, сотрудничества, нравственных качеств - коллективизма, способности к взаимовыручке, адекватной самооценке.
Слайд 3Вопросы разминки №1
1. Что общего в составе всех кислот?
( атомы водорода)
2.
( синий)
3. Реакция с выделением тепла и света?
(горение)
4. Формула сульфата натрия?
( Na₂SO₄)
5. Реакции, входе которых из нескольких веществ образуется одно?
( соединение)
6. Формула нерастворимой в воде кислоты?
( кремниевая H₂SiO₃ )
Слайд 47. Карбонаты – это соли какой кислоты?
( угольной)
8. Формула ангидрида азотной
( N₂O₅ )
9. Формула хлорида железа (3)?
( FeCl₃)
10. Реакции между кислородом и веществом?
( окисление)
11.Из чего состоит генетический ряд металла?
(металл, основный оксид, основание, соль)
12. Формула гидроксида натрия?
(NаOH)
Слайд 5Вопросы разминки №2
1. Бинарные соединения, содержащие кислород?
(оксиды)
2. Цвет лакмуса в кислой
(красный)
3. Отрицательно заряженный ион?
(анион)
4. Формула карбоната кальция?
(CaCO₃ )
5. Реакция между кислотой и основанием?
(нейтрализации, обмена)
6. Растворимые в воде основания?
( щелочи)
Слайд 67. Формула гидроксида алюминия?
(Al(OH)₃ )
8. Кислотный оксид, нерастворимый в воде?
( SiO₂
9. Соли серной кислоты?
( сульфаты)
10. Вещества, состоящие из атомов водорода и кислотного остатка?
( кислоты)
11. Из чего состоит генетический ряд неметалла?
( неметалл, кислотный оксид, кислота, соль)
12. Основание, соответствующее оксиду бария?
( Ba(OH)₂ )
Слайд 7Вопросы разминки №3
1. Цвет лакмуса в нейтральной среде?
(фиолетовый)
2. Вещества, состоящие из
( соли)
3. Как называются заряженные частицы?
( ионы)
4. Соли соляной кислоты?
(хлориды)
5. Реакции между простым и сложным веществами?
( замещения)
6. Формула оксида , соответствующего гидроксиду натрия?
( Na₂O)
Слайд 87. Ангидрид фосфорной кислоты?
( P₂O₅ )
8. Оксиды каких металлов могут восстанавливаться
( расположенных после марганца в ряду активности)
9. На какие группы делятся кислоты по содержанию кислорода?
( бескислородные и кислородсодержащие)
10. Формула гидроксида калия?
(КОН)
11. От чего зависит валентность кислотного остатка?
( от количества атомов водорода)
12. С какими металлами могут взаимодействуют кислоты?
( в ряду активности до водорода)
Слайд 9Вопросы разминки №4
1. Вещества, состоящие из атомов металла и гидроксогрупп?
( основания)
2.
( основные, амфотерные и кислотные)
3.Реакции, в ходе которых из одного вещества образуется несколько новых?
( разложения)
4. Соли фосфорной кислоты?
( фосфаты)
5. Формула сульфата меди (2)?
(CuSO₄ )
6. В каких случаях реакции обмена практически осуществимы?
( если образуется газ, осадок или вода)
Слайд 107. Ангидрид соляной кислоты?
( не существует)
8. Цвет фенолфталеина в щелочной среде?
(
9. Положительно заряженные ионы?
(катионы)
10. К какому типу относятся реакции между двумя солями?
( обмен)
Основание, соответствующее оксиду меди(2)?
(CU(OH)₂ )
12. Какие металлы могут замещать другие металлы в составе соли?
(более активные; расположенные в ряду активности левее, чем в самой соли)
Слайд 13Химическая рыбалка
Cu(OH)₂→ CuO + H₂O
2Fe(OH)₃→ Fe₂O₃ + 3 H₂O
K₂O + N₂O₅
K₂O + 2HNO₃ →2 KNO₃ + H₂O
Na₂O +SO₃ → Na₂SO₄
2NaOH + SO₃ → Na₂SO₄ + H₂O
2NaOH + H₂SO₄ → Na₂SO₄ + 2H₂O
Na₂O + H₂O → 2NaOH
2Na + 2H₂O → 2NaOH + 2H₂↑
P₂O₅ + 3H₂O → 2H₃PO₄
P₂O₅ + 3BaO → Ba₃ (PO₄)₂
2H₃PO₄ + 3BaO → Ba₃ (PO₄)₂ + 3 H₂O
2Al + 6HCl → 2AlCl₃ + 3H₂↑
2Al₂O₃ + 6HCl → 2AlCl₃ + 3H₂O
H₂CO₃ → CO₂ + H₂O
CaO + CO₂→ CaCO₃
Ca(OH)₂ + CO₂→ CaCO₃ + H₂O
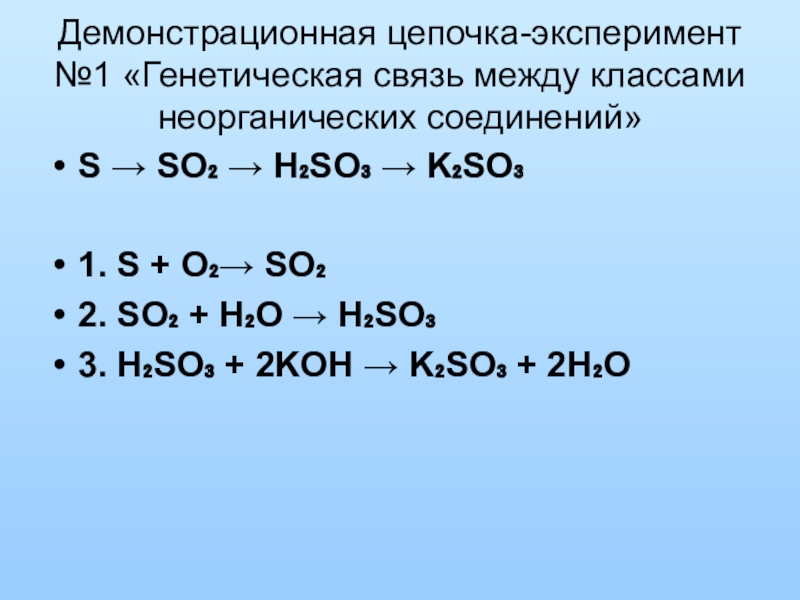
Слайд 14Демонстрационная цепочка-эксперимент №1 «Генетическая связь между классами неорганических соединений»
S → SO₂
1. S + O₂→ SO₂
2. SO₂ + H₂O → H₂SO₃
3. H₂SO₃ + 2KOH → K₂SO₃ + 2H₂O
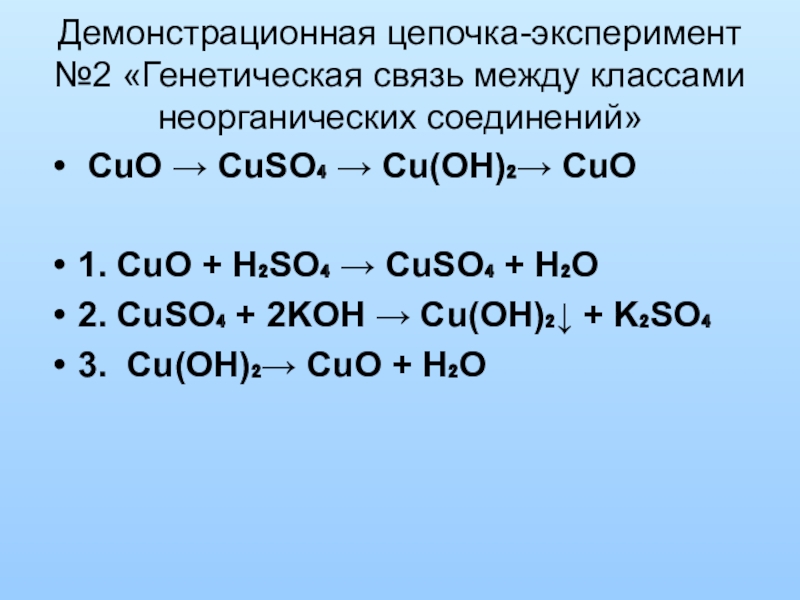
Слайд 15Демонстрационная цепочка-эксперимент №2 «Генетическая связь между классами неорганических соединений»
CuO →
1. CuO + H₂SO₄ → CuSO₄ + H₂O
2. CuSO₄ + 2KOH → Cu(OH)₂↓ + K₂SO₄
3. Cu(OH)₂→ CuO + H₂O
Слайд 16
Задание – эксперимент
«Получение хлорида серебра»
Используя необходимые реактивы из стоящих на
BaCl₂ + 2AgNO₃→2AgCl↓ + Ba(NO₃)₂
Слайд 17
Задание – эксперимент
«Получение гидроксида железа(II)»
Используя необходимые реактивы из стоящих на
FeSO₄ + 2KOH→ Fe(OH)₂↓+ 2KCL
Слайд 18
Задание – эксперимент
«Получение сульфата бария»
Используя необходимые реактивы из стоящих
BaCl₂ + H₂SO₄→ BaSO₄↓ + 2HCl
Слайд 19
Задание – эксперимент
«Получение оксида углерода(IV)».
Используя необходимые реактивы из стоящих
Na₂CO₃ + H₂SO₄→ Na₂SO₄ + CO₂↑ + H₂O
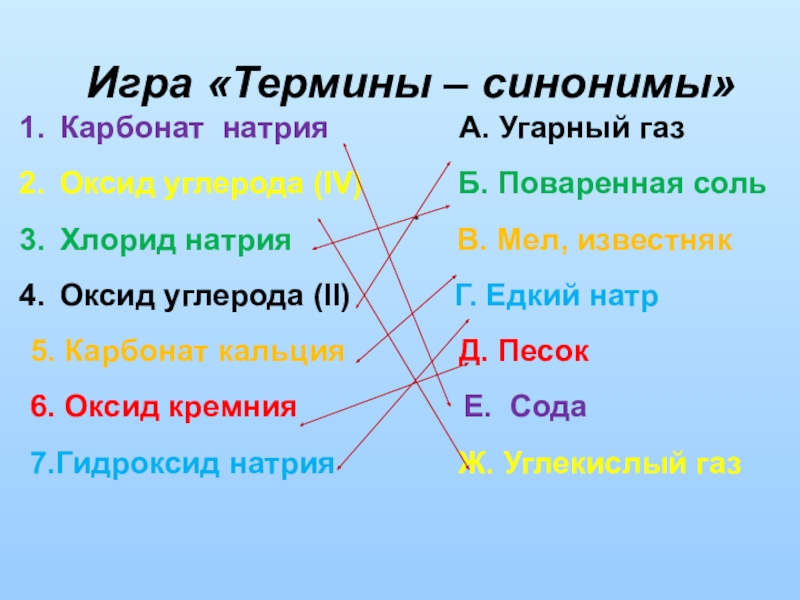
Слайд 20Игра «Термины – синонимы»
Карбонат натрия
Оксид углерода (IV) Б. Поваренная соль
Хлорид натрия В. Мел, известняк
Оксид углерода (II) Г. Едкий натр
5. Карбонат кальция Д. Песок
6. Оксид кремния Е. Сода
7.Гидроксид натрия Ж. Углекислый газ
Слайд 21Тест по теме «Основные классы неорганических соединений».
1. Выберите формулу кислоты:
а) CuO
2. Выберите формулу основания:
а) Mg(NO3)2 б) Al2O3 в) HNO3 г) KOH
Слайд 223. Выберите формулу оксида:
а) MgO
б) AlPO4
в) H2SiO3
г) ZnCl2
4. Выберите
а) CO2 б) CH4 в) BaS г) FeO
Слайд 235. Выбери соль серной кислоты:
а) сульфид меди (II)
б) сульфит меди (II)
в)
6. Выбери формулу гидроксида натрия, записанную правильно:
а) Na2OH б) NaOH в) Na(OH)2 г) Na(OH)3
Слайд 247. В какой схеме правильно записаны формулы продуктов химической реакции:
а) CaO
8. Из рядов веществ – выберите последовательность: кислотный оксид-кислота-соль.
а) CaO, H2SO4, NaCl б) SO3, HCl, CuSO4 в) BaO, HCl, K2SO4 г) FeO, NaOH, KCl
Слайд 259. Выбери последовательность формул, отражающих генетический ряд калия:
а) KOH, K₂SO₄ ,K,
10. Выбери последовательность формул, отражающих генетический ряд азота:
а) N₂, NaNO₃, HNO₃, N₂O₅ б) N₂O₅, HNO₃, N₂, NaNO₃ в) HNO₃, N₂, NaNO₃, N₂O₅ г) N₂, N₂O₅, HNO₃, NaNO₃
Слайд 26Домашнее задание:
Подготовиться к контрольной работе, повт. § 40 – 47, упр.
СПАСИБО ЗА РАБОТУ НА УРОКЕ!