- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад урок по химии 8 класс Массовая доля
Содержание
- 1. Презентация урок по химии 8 класс Массовая доля
- 2. Цели урока:1) Учебно-образовательные: формирование понятий раствор, массовая
- 3. 1. Классификация задач по
- 4. Используемые интернет ресурсыhttp://files.school-collection.edu.ru/dlrstore/0ab791e0-4185-11db-b0de-0800200c9a66/index_mht.htmhttp://files.school-collection.edu.ru/dlrstore/0ab791e1-4185-11db-b0de-0800200c9a66/index_mht.htmhttp://fcior.edu.ru/card/7359/laboratornaya-rabota-prigotovlenie-rastvora-s-zadannoy-massovoy-doley-rastvorennogo-veshestva.html http://fcior.edu.ru/card/7528/testy-po-teme-rastvorimost-veshestv-v-vode.html
- 5. Что такое раствор?mр-ра = mр.в. + mр-теляmр-теля=
- 6. Что означает 9%-ый раствор?В 100г раствора содержится
- 7. http://files.school-collection.edu.ru/dlrstore/0ab791e0-4185-11db-b0de-0800200c9a66/index_mht.htm
- 8. В 800г раствора содержится 40г поваренной соли.
- 9. Приготовление растворов.Для полоскания горла используют 4% раствор
- 10. Разбавление растворов.К 200мл 5%-ного с ρ =
- 11. Добавление вещества в раствор.К 300г 40%-ного раствора
- 12. Решение задач «Смешивание растворов»m2р-раω2m1р-раω1m3р-раm3р.в.ω3 = m3р-раm3р-ра
- 13. Какую массу P2O5 следует добавить к 200г
- 14. Как из 36%-ого раствора уксусной кислоты приготовить
- 15. ТАК ЧТО СКАЖЕМ «СПАСИБО» ВОДЕ ЗА ЕЁ СПОСОБНОСТЬ ОБРАЗОВЫВАТЬ РАСТВОРЫ!
Слайд 1«Массовая доля вещества в растворе». Разработала: учитель химии МКОУ Богучарская СОШ№1 Слепых Людмила
Слайд 2Цели урока:
1) Учебно-образовательные: формирование понятий раствор, массовая доля вещества в растворе,
2) Учебно-развивающие: развитие самостоятельной деятельности, развитие умений и навыков решать расчетные задачи
Основные понятия: раствор, растворитель, массовая доля вещества в растворе.
Планируемые результаты обучения: Научиться решать задачи, используя понятие «Массовая доля вещества в растворе».
Слайд 3 1. Классификация задач по типам. 2. Классификация по уровням
Разбираем условие задачи
Анализируем проблемную ситуацию
Находим способ решения. Составляем план-схему
Решаем задачу
Слайд 4Используемые интернет ресурсы
http://files.school-collection.edu.ru/dlrstore/0ab791e0-4185-11db-b0de-0800200c9a66/index_mht.htm
http://files.school-collection.edu.ru/dlrstore/0ab791e1-4185-11db-b0de-0800200c9a66/index_mht.htm
http://fcior.edu.ru/card/7359/laboratornaya-rabota-prigotovlenie-rastvora-s-zadannoy-massovoy-doley-rastvorennogo-veshestva.html
http://fcior.edu.ru/card/7528/testy-po-teme-rastvorimost-veshestv-v-vode.html
Слайд 5Что такое раствор?
mр-ра = mр.в. + mр-теля
mр-теля= mр-ра - mр.в
http://fcior.edu.ru/card/3651/istinnye-rastvory.html
Слайд 6Что означает 9%-ый раствор?
В 100г раствора содержится 9г вещества и 91г
А в 500г раствора?
В 100г раствора- 9г в-ва и 91гН₂О
В 500г раствора- x г в-ва и y г Н₂О
Х= 9·500:100;
X= 45г в-ва
m(Н₂О)= 500-45=455г
Слайд 7
http://files.school-collection.edu.ru/dlrstore/0ab791e0-4185-11db-b0de-0800200c9a66/index_mht.htm
Слайд 8В 800г раствора содержится 40г поваренной соли. Какова массовая доля соли
Дано:
mр-ра = 800 г
m(NaCl)=40 г
Найти ω (NaCl)
Решение.
ω =
ω (NaCl) = = 0,05 (5%)
Ответ: ω (NaCl) = 5 %
Слайд 9Приготовление растворов.
Для полоскания горла используют 4% раствор соды (NaHCO3). Приготовить 50
Вопрос: Что значит приготовить раствор?
Ответ: Найти массу соды и объем воды.
Дано:
mр-ра = 50 г
ω (NaHCO3) = 4 %
Найти
m (NaHCO3)
V(H2O)
Решение.
mр.в. = mр-ра • ω
m (NaHCO3) = 50 г • 0,04 = 2 г
mр-теля = mр-ра – mр.в.
m (H2O) = 50 г – 2 г = 48 г
V = m : ρ
V (H2O) = 48 г : 1 г/мл = 48 мл
Ответ: 2 г NaHCO3 , 48 мл H2O
Слайд 10Разбавление растворов.
К 200мл 5%-ного с ρ = 1,1 г/мл прилили 40г
Vр-ра = 200 мл
ρ р-ра = 1,1 г/мл
ω1 (соли) = 5 %
Найти ω2 (соли)
m (H2O) = 40 г
Изменилась ли масса раствора?
Ответ: да, на массу добавленной воды
mр-ра (конеч.) = mр-ра исх. + m (H2O)
V • ρ
m р.в. = m р-ра • ω1 = V • ρ • ω1
Изменилась ли масса растворенного вещества?
Ответ: нет
ω2 =
ω2 = = = 0,04 (4%)
Слайд 11Добавление вещества в раствор.
К 300г 40%-ного раствора добавили 20г соли. Найти
mр-ра = 300 г
ω1 (соли) = 40 %
m (соли) = 20 г
Найти ω2 (соли)
Изменилась ли масса раствора?
Ответ: да, на массу добавленной соли
mр-ра (конеч.) = mр-ра исх. + m (соли)
Изменилась ли масса растворимого вещества?
Ответ: да, на массу добавленной соли
m р.в. = m р-ра • ω1 + mдобавл.соли
ω2 =
ω2 = = = 0,44 (44%)
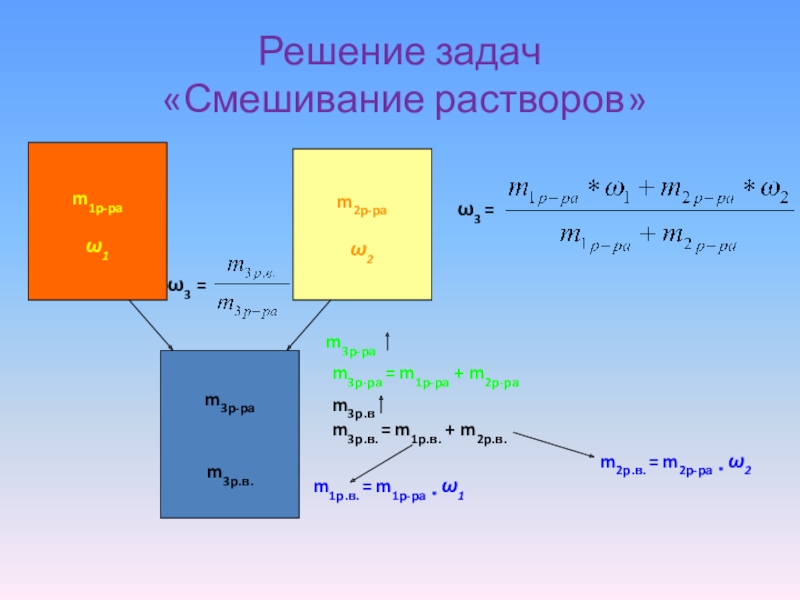
Слайд 12Решение задач
«Смешивание растворов»
m2р-ра
ω2
m1р-ра
ω1
m3р-ра
m3р.в.
ω3 =
m3р-ра
m3р-ра = m1р-ра + m2р-ра
m3р.в
m3р.в. =
m1р.в. = m1р-ра * ω1
m2р.в. = m2р-ра * ω2
ω3 =
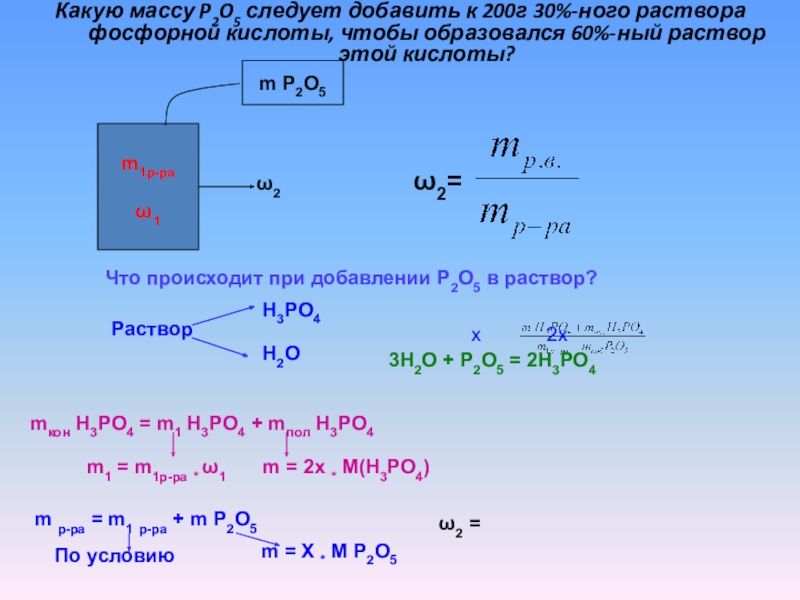
Слайд 13Какую массу P2O5 следует добавить к 200г 30%-ного раствора фосфорной кислоты,
m1р-ра
ω1
m P2O5
ω2
ω2=
Что происходит при добавлении P2O5 в раствор?
Раствор
H3PO4
H2O
3H2O + P2O5 = 2H3PO4
mкон H3PO4 = m1 H3PO4 + mпол H3PO4
m1 = m1р-ра * ω1
x
2x
m = 2x * M(H3PO4)
m р-ра = m1 р-ра + m P2O5
По условию
m = X * M P2O5
ω2 =
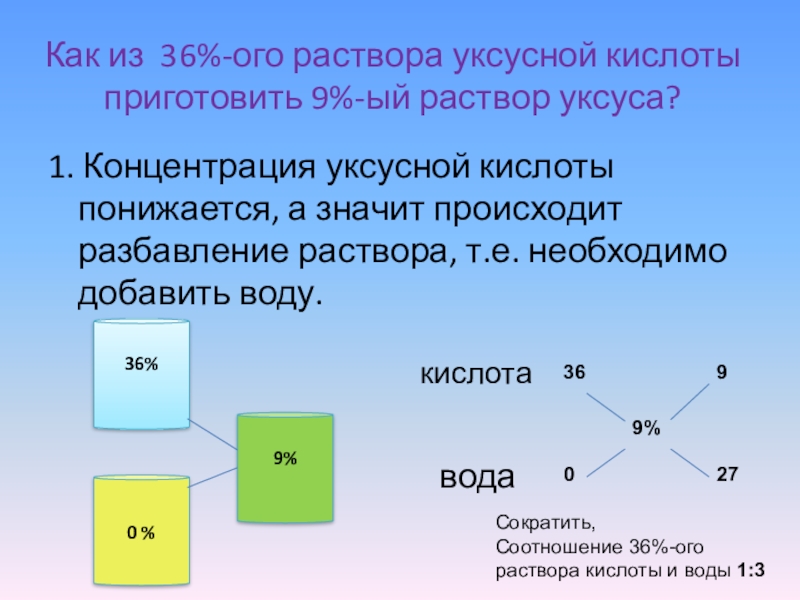
Слайд 14Как из 36%-ого раствора уксусной кислоты приготовить 9%-ый раствор уксуса?
1. Концентрация
Сократить,
Соотношение 36%-ого раствора кислоты и воды 1:3