- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Путешествие в мир химических реакций
Содержание
- 1. Презентация Путешествие в мир химических реакций
- 2. «Деятельность заключает награду в самой себе.
- 3. «Разминка»
- 4. «Руки вверх»
- 5. Выделение или поглощение теплотыИзменение цветаВыпадение (растворение) осадкаВыделение газаВыделение запахаПризнаки химической реакции
- 6. Классификация реакцийреакция соединенияреакция разложенияреакция замещенияреакция обмена
- 7. «Установите соответствие»
- 8. Слайд 8
- 9. 1 – В2 – А3 – Г4 – Б
- 10. «Кто быстрее? -эстафета» 1) P + O2
- 11. «Кто быстрее? -эстафета» 1) 4P + 5O2
- 12. «Верни потерю» C + … → CO2 KI
- 13. «Верни потерю» C + O2 → CO2 2KI
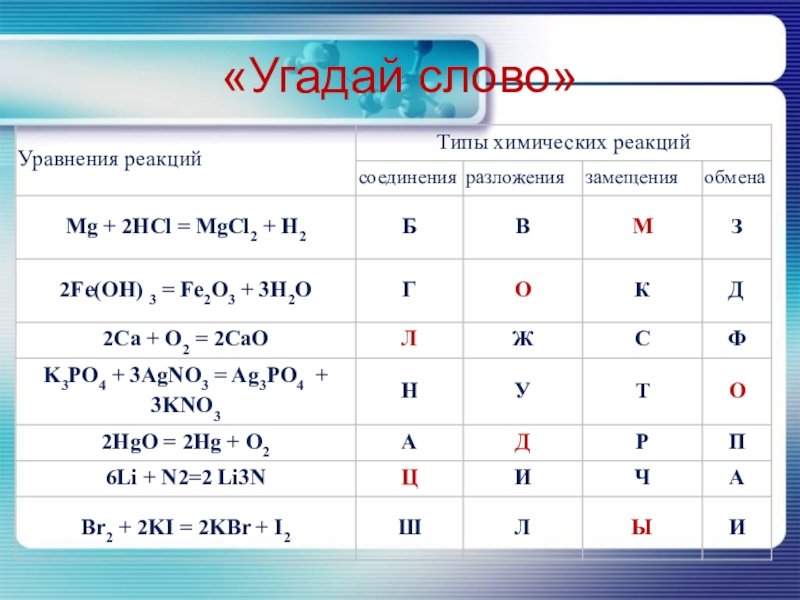
- 14. «Угадай слово»
- 15. «Угадай слово»
- 16. «Химические реакции вокруг нас»
- 17. Рефлексия
- 18. Домашнее заданиеСпасибо за работу на уроке!Составить по 2 уравнения на каждый тип химической реакции
- 19. Слайд 19
«Деятельность заключает награду в самой себе. Действовать, создавать, вступать в борьбу с обстоятельствами, побеждать их или чувствовать себя побежденным - вот вся радость, все человеческое здоровье заключается в этом» (Э. Золя).
Слайд 1Путешествие в мир химических реакций
Чонтай Ирина Владимировна
Учитель химии, биологии и географии
Слайд 2
«Деятельность заключает награду в самой себе. Действовать, создавать, вступать в
борьбу с обстоятельствами, побеждать их или чувствовать себя побежденным - вот вся радость, все человеческое здоровье заключается в этом» (Э. Золя).
Слайд 5Выделение или поглощение теплоты
Изменение
цвета
Выпадение (растворение) осадка
Выделение
газа
Выделение
запаха
Признаки химической реакции
Слайд 10«Кто быстрее? -эстафета»
1) P + O2 → P2O5
2) NH4Cl →
NH3 + HCl
3) K2O + H3PO4 → K3PO4 + H2O
4) CuO + H2SO4 → CuSO4 + H2O
5) MnO2 + Al → Al2O3 + Mn
6) Ca + O2 → CaO
3) K2O + H3PO4 → K3PO4 + H2O
4) CuO + H2SO4 → CuSO4 + H2O
5) MnO2 + Al → Al2O3 + Mn
6) Ca + O2 → CaO
1. N2 + O2 → NO
2. FeCl3 + NaOH → Fe(OH)3 + NaCl
3. P2O5 + H2O → H3PO4
4. Al + HCl → AlCl3 + H2
5. CaCO3 → CaO + CO2
6. NaOH + CuSO4 → Cu(OH)2 + Na2SO4
Слайд 11«Кто быстрее? -эстафета»
1) 4P + 5O2 → 2P2O5
2) NH4Cl →
NH3 + HCl
3) 3K2O + 2H3PO4 → 2K3PO4 + 3H2O
4) CuO + H2SO4 → CuSO4 + H2O
5) 3MnO2 + 4Al → 2Al2O3 + 3Mn
6) 2Ca + O2 → 2CaO
3) 3K2O + 2H3PO4 → 2K3PO4 + 3H2O
4) CuO + H2SO4 → CuSO4 + H2O
5) 3MnO2 + 4Al → 2Al2O3 + 3Mn
6) 2Ca + O2 → 2CaO
1. N2 + O2 → 2NO
2. FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
3. P2O5 + 3H2O → 2H3PO4
4. 2Al + 6HCl → 2AlCl3 + 3H2
5.CaCO3 → CaO + CO2
6. 2NaOH + CuSO4 → Cu(OH)2 + Na2SO4
Слайд 12«Верни потерю»
C + … → CO2
KI + Cl2 → …
+ I2
MnO2 + Al → Al2O3 + …
BaO + H2SO4 → BaSO4 + …
H2O → … + O2
MnO2 + Al → Al2O3 + …
BaO + H2SO4 → BaSO4 + …
H2O → … + O2
Слайд 13«Верни потерю»
C + O2 → CO2
2KI + Cl2 → 2KCl
+ I2
3MnO2 + 4Al → 2Al2O3 + 3Mn
BaO + H2SO4 → BaSO4 + H2O
2H2O → 2H2 + O2
Сумма - 12
3MnO2 + 4Al → 2Al2O3 + 3Mn
BaO + H2SO4 → BaSO4 + H2O
2H2O → 2H2 + O2
Сумма - 12
Слайд 18 Домашнее задание
Спасибо за работу на уроке!
Составить по 2 уравнения
на каждый тип химической реакции