- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Нитраты (9 класс)
Содержание
- 1. Презентация по теме Нитраты (9 класс)
- 2. Получение нитратов. Получить нитраты можно взаимодействием металлов
- 3. Получение нитратов. 3. Взаимодействием азотной кислоты с
- 4. Свойства, похожие на свойства других солей1. Взаимодействуют
- 5. Свойства, похожие на свойства других солей3. Взаимодействуют
- 6. Специфические химические свойства нитратов. Нитраты, в состав
- 7. Специфические химические свойства нитратов.2. Нитраты, в состав
- 8. Специфические химические свойства нитратов.Нитраты, в состав которых
- 9. Специфические химические свойства нитратов.Разложение нитрата аммония: NH4NO3 (кр.) = N2O + 2H2O.
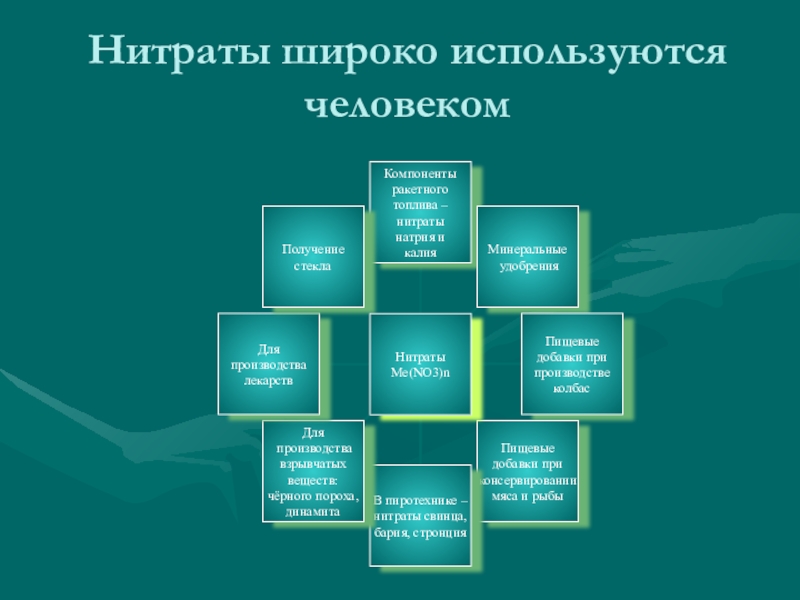
- 10. Нитраты широко используются человеком
- 11. «Думать и действовать, действовать и думать
- 12. Нитраты создают и оберегаютNaNO3 используется при производстве
- 13. Нитраты уничтожаютВ ІХ веке китайцы изобрели
- 14. НИТРАТЫ И ЭКОЛОГИЯВ наше время нет причин
- 15. Содержание нитратов в продуктах питанияУ свеклы нитраты
- 16. Допустимое содержание нитратов(в мг/кг по нитрат –
- 17. Причины превышения нормы содержания нитратов в продуктах:-нарушение
- 18. Человек должен спасти
- 19. При выращивании растений нужно придерживаться норм внесения
Получение нитратов. Получить нитраты можно взаимодействием металлов с азотной кислотой: Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + H2O 2. Взаимодействием азотной кислоты с оксидами металлов: Fe2O3 + 6HNO3 = 2Fe(NO3)3 +3H2O
Слайд 2Получение нитратов.
Получить нитраты можно взаимодействием металлов с азотной кислотой:
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + H2O
2. Взаимодействием азотной кислоты с оксидами металлов: Fe2O3 + 6HNO3 = 2Fe(NO3)3 +3H2O
2. Взаимодействием азотной кислоты с оксидами металлов: Fe2O3 + 6HNO3 = 2Fe(NO3)3 +3H2O
Слайд 3Получение нитратов.
3. Взаимодействием азотной кислоты с основаниями :
Ba (OH)2 + 2HNO3 = Ba(NO3)2
+2H2O
4. Взаимодействием азотной кислоты с солями: CuCO3 + 2HNO3 = Сu(NO3)2 +CO2 + H2O
4. Взаимодействием азотной кислоты с солями: CuCO3 + 2HNO3 = Сu(NO3)2 +CO2 + H2O
Слайд 4Свойства, похожие на свойства других солей
1. Взаимодействуют с металлами
Cu (NO3)2 +
Fe = Fe(NO3)2 + Cu
Взаимодействуют с кислотами, если образуется осадок Ba (NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
Взаимодействуют с кислотами, если образуется осадок Ba (NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
Слайд 5Свойства, похожие на свойства других солей
3. Взаимодействуют с солями,если образуется осадок
3Zn
(NO3)2 + 2Na3PO4 = Zn3(PO4)2↓ + 6NaNO3
Слайд 6Специфические химические свойства нитратов.
Нитраты, в состав которых входит маталл, находящийся в
ряду напряжений до магния разлагаются при нагревании с образованием нитритов и кислорода, например,
2NaNO3 = 2NaNO2 + O2
2NaNO3 = 2NaNO2 + O2
Слайд 7Специфические химические свойства нитратов.
2. Нитраты, в состав которых входит маталл, находящийся
в ряду напряжений от магния до водрода разлагаются при нагревании с образованием оксида металла, оксида азота (IV) и кислорода, например,
2Zn(NO3)2 = 2ZnO + 4NO2 + O2
2Zn(NO3)2 = 2ZnO + 4NO2 + O2
Слайд 8Специфические химические свойства нитратов.
Нитраты, в состав которых входит маталл, находящийся в
ряду напряжений правее меди разлагаются при нагревании с образованием металла, оксида азота (IV) и кислорода, например, 2AgNO3 = 2Ag + 2NO2 + O2
Слайд 9Специфические химические свойства нитратов.
Разложение нитрата аммония:
NH4NO3 (кр.) = N2O + 2H2O.
Слайд 12Нитраты создают и оберегают
NaNO3 используется при производстве колбас, шинки, рыбы, сыра.
Он восстанавливается до NaNO2 , который не даёт портиться мясу, сохраняет его цвет и запах.
NaNO2 уничтожает бактерии ботулизма.
1 грамма яда ботулизма достаточно для уничтожения всего человечества.
Нельзя использовать нитраты
в домашних условиях!
Это создаёт угрозу жизни!
Предельно допустимая суточная
норма употребления нитратов –
5 мг на 1 кг массы тела!
NaNO2 уничтожает бактерии ботулизма.
1 грамма яда ботулизма достаточно для уничтожения всего человечества.
Нельзя использовать нитраты
в домашних условиях!
Это создаёт угрозу жизни!
Предельно допустимая суточная
норма употребления нитратов –
5 мг на 1 кг массы тела!
Слайд 13Нитраты уничтожают
В ІХ веке китайцы изобрели порох. Это смесь нитрата
калия, серы и угля в соотношении 2:1:3.
Пороховые снаряды сжигали всё в радиусе 15 метров, а осколки пробивали броню воина.
Шесть столетий порох
использовался в военном
деле, его состав не менялся,
а менялся только способ
производства.
Представьте,
сколько жизней было
уничтожено за это
время!
Пороховые снаряды сжигали всё в радиусе 15 метров, а осколки пробивали броню воина.
Шесть столетий порох
использовался в военном
деле, его состав не менялся,
а менялся только способ
производства.
Представьте,
сколько жизней было
уничтожено за это
время!
Слайд 14НИТРАТЫ И ЭКОЛОГИЯ
В наше время нет причин бояться «азотного голода»
В наше
время возникла угроза – экологическая.
Использование азотных удобрений нарушает естественный круговорот.
Жизненно необходимый азот отнесён к «врагам» окружающей среды.
Нитраты легко растворяются в почвенной воде и вымываются в водоёмы.
В последнее время установлены предельно допустимые нормы содержания нитратов в растениях и в воде.
КТО СПАСЁТ
ЧЕЛОВЕКА
ОТ ЭТОЙ УГРОЗЫ?
Использование азотных удобрений нарушает естественный круговорот.
Жизненно необходимый азот отнесён к «врагам» окружающей среды.
Нитраты легко растворяются в почвенной воде и вымываются в водоёмы.
В последнее время установлены предельно допустимые нормы содержания нитратов в растениях и в воде.
КТО СПАСЁТ
ЧЕЛОВЕКА
ОТ ЭТОЙ УГРОЗЫ?
Слайд 15Содержание нитратов в продуктах питания
У свеклы нитраты сконцентрированы в верхней части
корнеплода
У моркови: в сердцевине - 90% и в наружной части -10%.
У капусты - в кочерыжке и в толстых черешках листьев.
У кабачков, огурцов, арбузов, дыни, картофеле - в кожуре.
У картофеля в мелких клубнях нитратов больше, чем в крупных.
Маленькие огурцы содержат нитратов меньше, чем большие, в огурце, сорванном утром, нитратов меньше.
У зеленных культур нитраты накапливаются в стеблях(петрушка, салат, укроп, сельдерей).
У моркови: в сердцевине - 90% и в наружной части -10%.
У капусты - в кочерыжке и в толстых черешках листьев.
У кабачков, огурцов, арбузов, дыни, картофеле - в кожуре.
У картофеля в мелких клубнях нитратов больше, чем в крупных.
Маленькие огурцы содержат нитратов меньше, чем большие, в огурце, сорванном утром, нитратов меньше.
У зеленных культур нитраты накапливаются в стеблях(петрушка, салат, укроп, сельдерей).
Слайд 16Допустимое содержание нитратов(в мг/кг по нитрат – иону NO3)
лук на перо
– 400
капуста белокочанная – 300
морковь – 30
огурцы – 150
свекла – 140
картофель – 80
помидор – 60
арбуз – 45
дыня – 45
капуста белокочанная – 300
морковь – 30
огурцы – 150
свекла – 140
картофель – 80
помидор – 60
арбуз – 45
дыня – 45
Слайд 17Причины превышения нормы содержания нитратов в продуктах:
-нарушение технологии внесения минеральных удобрений,
бесконтрольное внесение их в почву большими дозами (больше – не значит лучше);
-характер почвы, природные условия, густота посевов;
-низкая солнечная радиация, излишек влаги;
- содержание нитратов увеличивается в июне – июле перед сбором урожая, особенно во время последней подкормки удобрениями;
-незрелые овощи содержат больше нитратов, чем зрелые
-характер почвы, природные условия, густота посевов;
-низкая солнечная радиация, излишек влаги;
- содержание нитратов увеличивается в июне – июле перед сбором урожая, особенно во время последней подкормки удобрениями;
-незрелые овощи содержат больше нитратов, чем зрелые
Слайд 18 Человек должен спасти себя сам
Правила грамотного поведения с нитратами:
Неукоснительно придерживаться норм внесения нитратов в почву.
Нитраты хорошо растворяются в воде. Поэтому овощи и фрукты перед употреблением мыть горячей водой, а зелень вымачивать в воде 2 – 3 часа.
Нельзя варить овощи в алюминиевой посуде, т.к. алюминий ускоряет переход нитратов в нитриты.
Овощи и фрукты перед едой чистить, а у моркови и капусты удалять сердцевину.
При засолке нитраты уходят в рассол, поэтому его нельзя употреблять в пищу.
Если перед варкой картофель залить на 15 мин водой, то содержание нитратов уменьшается на 30%.
Неукоснительно придерживаться норм внесения нитратов в почву.
Нитраты хорошо растворяются в воде. Поэтому овощи и фрукты перед употреблением мыть горячей водой, а зелень вымачивать в воде 2 – 3 часа.
Нельзя варить овощи в алюминиевой посуде, т.к. алюминий ускоряет переход нитратов в нитриты.
Овощи и фрукты перед едой чистить, а у моркови и капусты удалять сердцевину.
При засолке нитраты уходят в рассол, поэтому его нельзя употреблять в пищу.
Если перед варкой картофель залить на 15 мин водой, то содержание нитратов уменьшается на 30%.
Слайд 19При выращивании растений нужно придерживаться норм внесения азотных удобрений.
Санэпидемстанции должны контролировать
нормы содержания нитратов в продуктах питания.
Вывод