Бозаджи Н.М.
учитель химии
высшей категории
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химми на тему Вода. Физические и химические свойства воды (8 кл.
Содержание
- 1. Презентация по химми на тему Вода. Физические и химические свойства воды (8 кл.
- 2. Воде была дана волшебная власть стать соком жизни на Земле.Леонардо да Винчи
- 3. Описывать распространение воды в природе.2.Рассматривать воду
- 4. Содержание Вода в природеПрименение и значение водыРефлексияКруговорот водыФизические св-ва водыХимическиесв-ва воды
- 5. I.Вода в природе Большая часть поверхности Землипокрыта
- 6. 1.Вода́ (оксид водорода) —Н2O. Mr (H2O)=M
- 7. II.2Физические свойства воды Вода – единственное вещество
- 8. Вода в организме человека Кровь человека на
- 9. Вода в организме человека Обезвоживание организма на
- 10. III.Химические свойства воды
- 11. а) очень активные металлы при взаимодействии с
- 12. б) металлы средней активности взаимодействуют с водой
- 13. III.2 Взаимодействие с неметаллами Получающиеся продукты взаимодействия
- 14. В результате образуются кислоты:IV.4 Взаимодействие с основными
- 15. Слайд 15
- 16. IV.Круговорот воды в природе Вода постоянно испаряется
- 17. Вопрос 1Вопрос 2Вопрос 3Вопрос 4Вопрос 5Вопрос 6Вопрос
- 18. 1.При обычных условиях вода может реагировать с: a)ZnO
- 19. 5.При растворении в воде основного оксида образуется:а)кислота b)соль
- 20. ВодаВ жизни растений и животныхВ быту человекаДля
- 21. Вода необходима всем живым организмам: растениям,
- 22. Берегите воду
- 23. Пожалуй, ни одна проблема не вызывает сейчас
- 24. Попадают ли отходы в океан? Оказывается, 75
- 25. « Вода – у тебя нет ни
- 26. Вода в природе
- 27. Научно-фантастическое будущее медленно, но верно пробирается в
- 28. Японский исследователь Масару Эмото (Masaru Emoto) приводит
- 29. Слайд 29
- 30. Закончите уравнения реакций, расставьте коэффициенты:а) Li2O +
- 31. Составьте уравнения реакций взаимодействия с водой следующих
- 32. Укажите физическое свойство воды:голубой цвет 2) имеет
- 33. В процессе взаимодействия двух веществ образовались гидроксид
- 34. Выберите формулу гидроксида, который можно получить реакцией
- 35. ТестЗадание№6Какие вещества обозначены « Х» и
- 36. ТестОтвет:1 - 42 - 33 - 24 - 25 - 46 - 2
- 37. Рефлексия 1.На уроке я работал… 2.Своей работой
- 38. Разобрать конспект.Повторить параграф: § 5.1-5.3Выполнить задания:
Слайд 1Вода вокруг нас. Физические и химические свойства воды.
8 класс
Слайд 3Описывать распространение
воды в природе.
2.Рассматривать воду как простое
вещество(
3.Описывать физические свойства воды.
4.Записывать уравнения хим.реакций, демонстрирующих хим. свойства воды.
5.Рассматривать применение воды и её
значение
6.Осуществлять рефлексию
своей деятельности
В результате изучения темы, вы будете способны:
Слайд 4Содержание
Вода в природе
Применение и
значение воды
Рефлексия
Круговорот воды
Физические
св-ва воды
Химические
св-ва воды
Слайд 5I.Вода в природе
Большая часть поверхности Земли
покрыта морями и океанами -
71%
Морская вода – 97% - 98%
Пресная вода – 2% - 3%
75% - ее сковано льдом, находится под землей
Таким образом человек может пользоваться только 0,02% – 0,03%
всей воды на нашей планете.
Слайд 61.Вода́ (оксид водорода) —Н2O.
Mr (H2O)=
M (H2O)=
Связь между атомами водорода и кислорода
II.1 Вода – простое вещество
18
18 г/моль
Слайд 7II.2Физические свойства воды
Вода – единственное вещество в природе, которое в
Пар
Жидкость
Лед
Ж
Ц
З
Слайд 8Вода в организме человека
Кровь человека на 90% состоит из воды
Мышцы
Кости на 28%
Стекловидное тело глаза на 99%
Слайд 9Вода в организме человека
Обезвоживание организма
на 12 – 15 %
А потеря до 25 % воды –
к гибели организма
Без воды человек может прожить 3 дня,
в то время, как без пищи
30 – 50 дней
Слайд 11
а) очень активные металлы при взаимодействии с водой образуют Р.основания-( щелочь
2Na + 2H2O = 2NaOH + H2 ↑
гидроксид
натрия
2K + 2H2O = 2KOH + H2 ↑
гидроксид
калия
Ca + 2H2O = Ca(OH)2 + H2 ↑
гидроксид
кальция
III.1Взаимодействие с металлами
Слайд 12
б) металлы средней активности взаимодействуют с водой при нагревании, образуя оксид
Zn + H2O = ZnO + H2
оксид
цинка
3Fe + 4H2O = Fe3O4 (FeO•Fe2O3) +4H2
железная
окалина
в) малоактивные металлы с водой
не реагируют:
Cu + H2O =
III.1Взаимодействие с металлами
t0↑
t0↑
Слайд 13III.2 Взаимодействие с неметаллами
Получающиеся продукты взаимодействия очень разнообразны:
C + H2О
Cl2 + H2О = HClO + HCl
III.3 Реакция разложения воды
Под действием постоянного электрического тока или высокой температуры вода разлагается на кислород и водород:
2Н2О =
эл.ток
2Н2 + О2
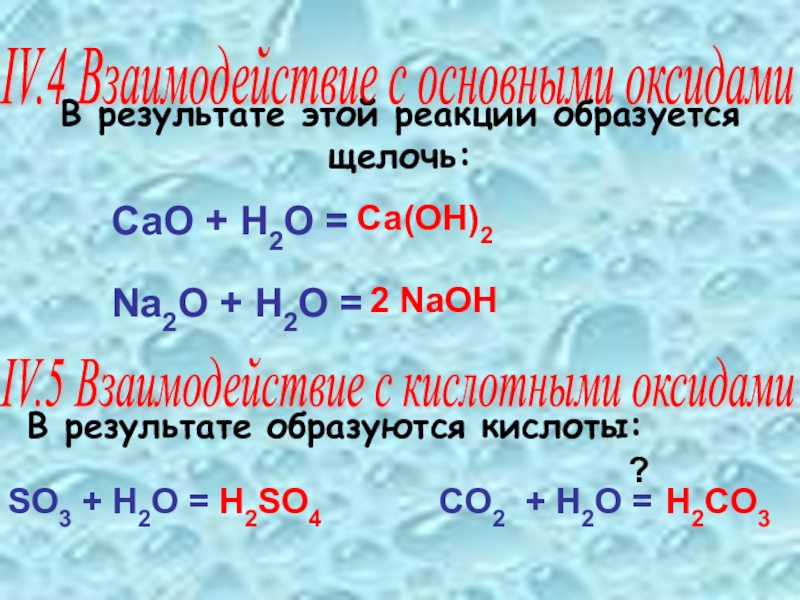
Слайд 14В результате образуются кислоты:
IV.4 Взаимодействие с основными оксидами
IV.5 Взаимодействие с
В результате этой реакции образуется щелочь:
SO3 + H2O =
CO2 + H2O =
СаО + Н2О =
Na2O + H2O =
Са(ОН)2
2 NaOH
H2SO4
H2CO3
?
Слайд 16IV.Круговорот воды в природе
Вода постоянно испаряется с поверхности наземных водоемов,
Атмосферная вода попадает на землю в виде осадков.
Но не нужно думать, что круговорот – это панацея от исчерпания доступных запасов пресной воды. Все же он происходит медленно.
Берегите воду!
Слайд 17Вопрос 1
Вопрос 2
Вопрос 3
Вопрос 4
Вопрос 5
Вопрос 6
Вопрос 7
Вопрос 8
Вопрос 9
Вопрос 10
+
-
+
+
+
+
+
+
+
+
+
-
-
-
-
-
-
-
-
-
Рефлексия:Тест по теме « Вода и её св-ва»
Слайд 181.При обычных условиях вода может реагировать с:
a)ZnO b) SiO2
2.При обычных условиях вода может реагировать с
a)кальцием b)оксидом алюминия
c) золотом d)оксидом кремния(IV)
3.При обычных условиях вода не может реагировать с:
a)Na2O b)K c) Fe2O3 d)SO3
4.Только при нагревании с водой реагирует: a)оксид калия b)кальций
c)железо d)натрий
Тест
Слайд 195.При растворении в воде основного оксида образуется:
а)кислота b)соль
c)снование
6. Формула продукта реакции оксида серы(IV) с водой:
a)H2S b) H2SO4 c)H2S2O3 d)H2SO3
7.Вода при обычных условиях может взаимодействовать со всеми вещ-ми группы:
кальций, оксид бария, оксид серы(VI) b) калий, оксид алюминия, медь
c)оксид кремния(IV), водород,хлорид натрия d)сера, алюминий, оксид фосфора(V).
Тест
Слайд 20
Вода
В жизни растений и животных
В быту человека
Для получения оснований
Для получения кислот
Как
В системах охлаждения
Для получения органических веществ
Для получения водорода
В паровых двигателях
Для производства минеральных удобрений
V.Применение воды
Вода
Слайд 21Вода необходима всем живым организмам: растениям, животным и человеку. Без воды нет
VI.Охрана воды
Слайд 23Пожалуй, ни одна проблема не вызывает сейчас у человечества такие оживленные
Слайд 24Попадают ли отходы в океан? Оказывается, 75 г. твердых отходов в
Слайд 25
« Вода – у тебя нет ни цвета, ни вкуса, ни
Нельзя сказать, что ты необходима для жизни: ты – сама жизнь!»
Антуан Сент – Экзюпери
Слайд 27 Научно-фантастическое будущее медленно, но верно пробирается в наши дома. И вот
Как же работают эти чудо -часы? Внутри находится конвертер, который «извлекает»электроны из молекул жидкости, и работает как топливная ячейка для часов. Расход воды очень небольшой. Сообщается что одной заправки резервуара хватит на «несколько недель» бесперебойной работы.
Вода топливо
NB!
Слайд 28 Японский исследователь Масару Эмото (Masaru Emoto) приводит удивительные доказательства информационных свойств
Память воды
NB!
Слайд 30Закончите уравнения реакций,
расставьте коэффициенты:
а) Li2O + H2O →
б) Mg +
в) SO3 + H2O →
г) SiO2 + H2O →
Самостоятельная работа
Задание№1
Слайд 31Составьте уравнения реакций взаимодействия с водой следующих веществ:
а) натрий;
г) литий; д) железо; ж) серебро.
Запишите реакции, расставьте коэффициенты, укажите названия образующихся веществ.
Самостоятельная работа
Задание№2
Слайд 32Укажите физическое свойство воды:
голубой цвет 2) имеет приятный запах
3) температура кипения
4) имеет вкус
Тест
Задание№1
С водой могут вступать в реакцию
оба вещества пары
H2, Na
2) CuO, Ca
3) CO2 , P2O5
4) N2 , Fe
Задание№2
Слайд 33В процессе взаимодействия двух веществ образовались гидроксид натрия и водород. Какие
1) оксид натрия и вода
2) натрий и вода
3) натрий и соляная кислота
4) оксид натрия и соляная кислота
Тест
Задание№3
Слайд 34Выберите формулу гидроксида, который можно получить реакцией соответствующего оксида с водой:
Тест
Задание№4
Сумма коэффициентов в уравнениях реакций воды с натрием и воды с оксидом лития соответственно равна
1) 7 и 3 2) 6 и 3 3) 4 и 4 4) 7 и 4
Задание№5
Слайд 35Тест
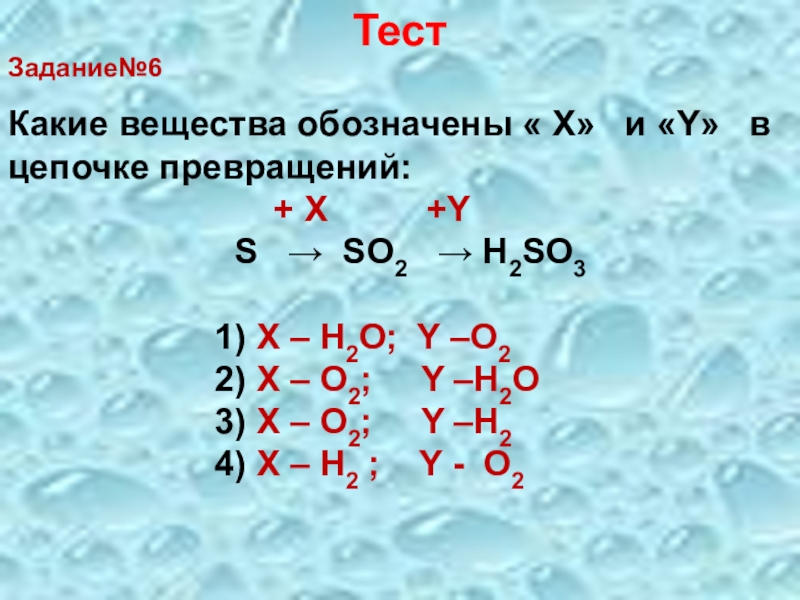
Задание№6
Какие вещества обозначены « Х» и «Y» в цепочке
+ X +Y
S → SO2 → H2SO3
1) X – H2O; Y –O2
2) X – O2; Y –H2O
3) X – O2; Y –H2
4) X – H2 ; Y - O2
Слайд 37Рефлексия
1.На уроке я работал…
2.Своей работой на уроке я…
3.Урок для меня показался…
4.За
активно, доволен, коротким, не устал, полезен, стало лучше, понятен, интересен, легким.
Слайд 38
Разобрать конспект.
Повторить параграф: § 5.1-5.3
Выполнить задания:
упр.1, упр.3 (г,д,е)
Домашнее задание