- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Виды химической связи
Содержание
- 1. Презентация по химии Виды химической связи
- 2. Под химической связью понимаются электрические силы притяжения,
- 3. Причина образования химической связи — стремление атомов
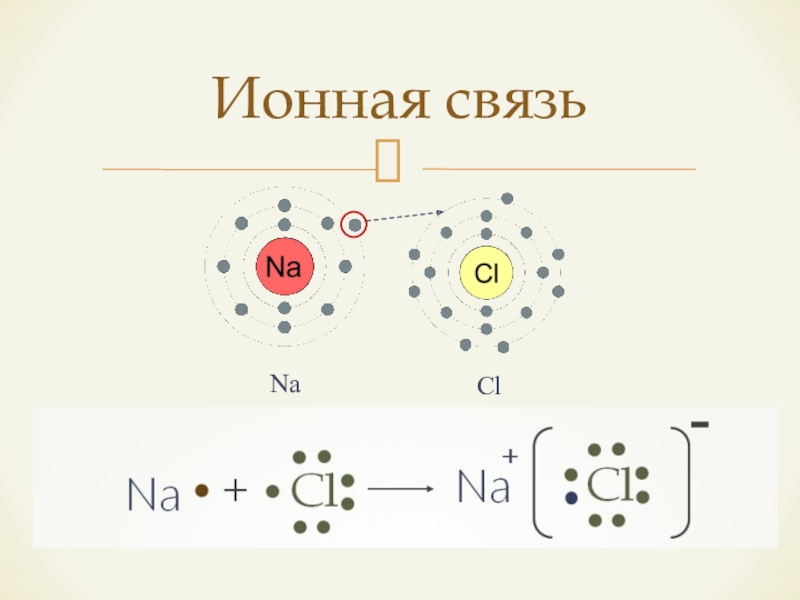
- 4. Ионная связьNaCl
- 5. ИоныПоложительныеОтрицательныеКатионыОбразуются в результате процесса окисленияАнионыОбразуются в результате процесса восстановления
- 6. Как правило, ионная связь возникает между атомами типичных металлов и типичных неметаллов.
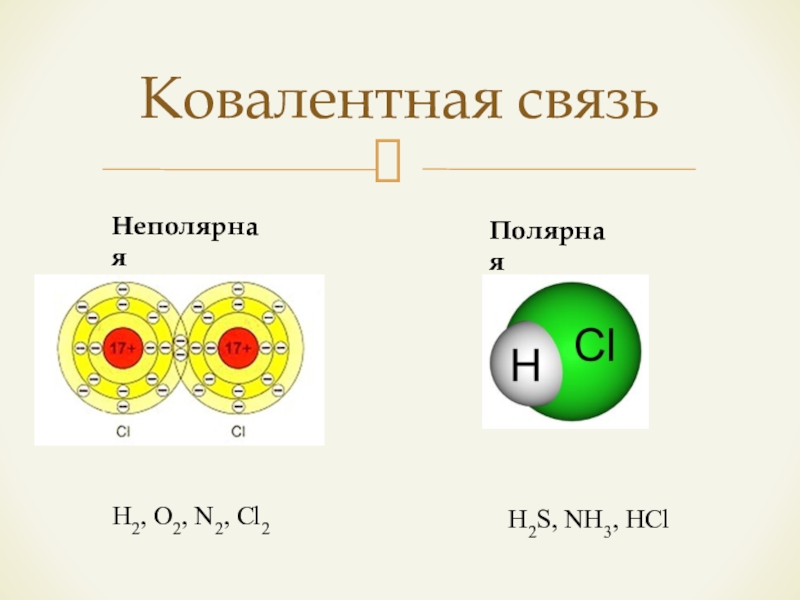
- 7. Ковалентная связьНеполярнаяПолярная H2, O2, N2, Cl2 H2S, NH3, HCl
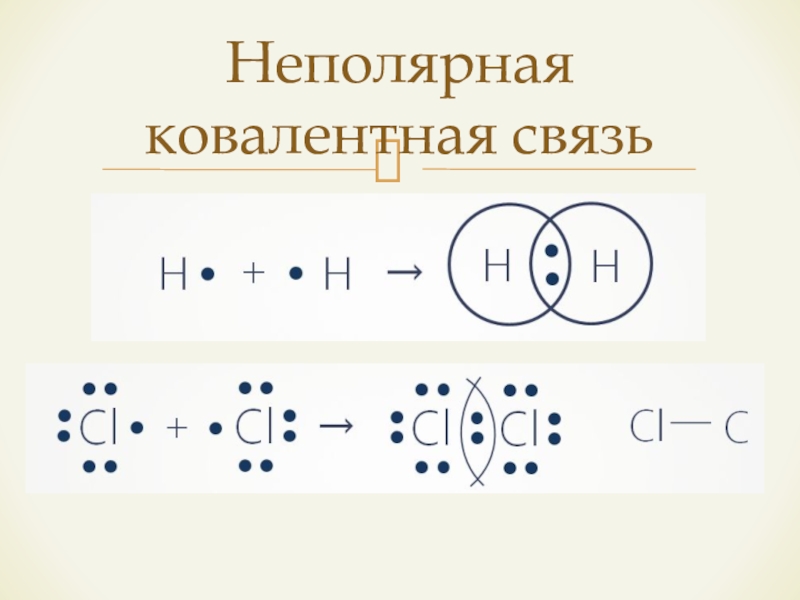
- 8. Неполярная ковалентная связь
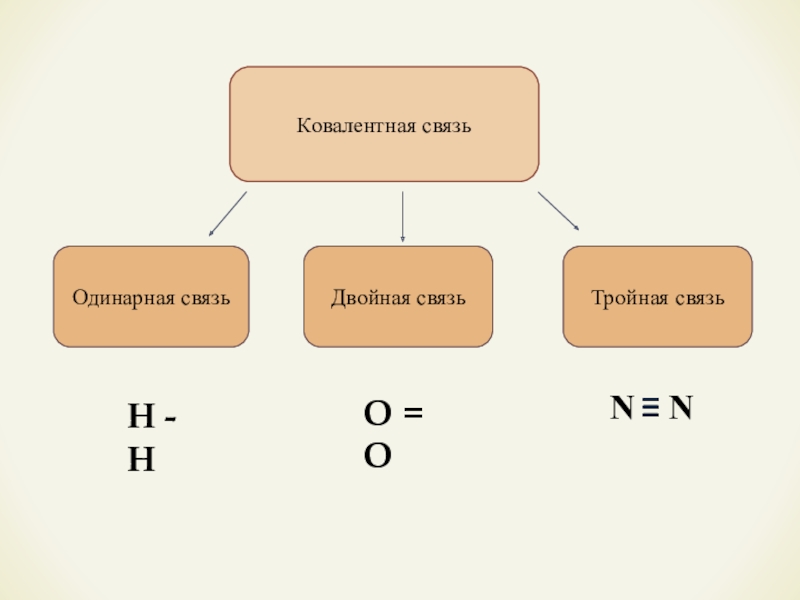
- 9. Ковалентная связьОдинарная связьДвойная связьТройная связьО = ОН - Н
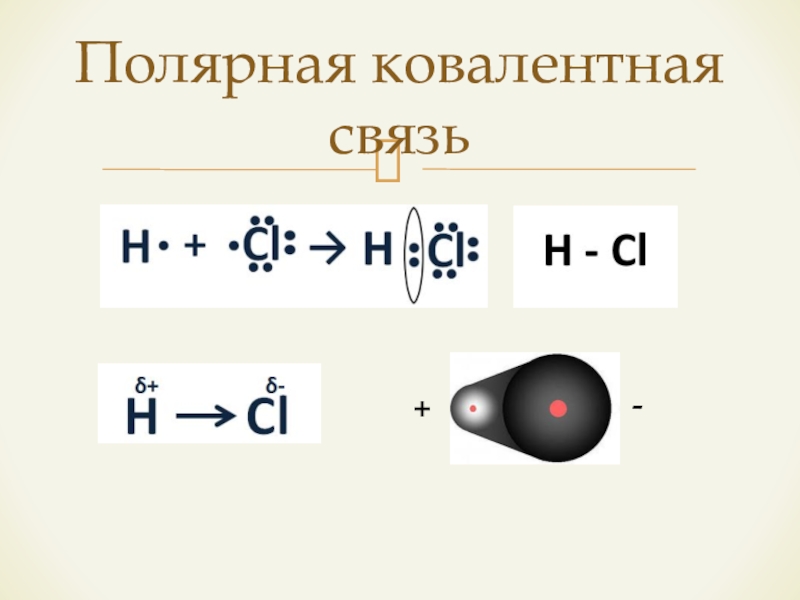
- 10. Полярная ковалентная связь+-
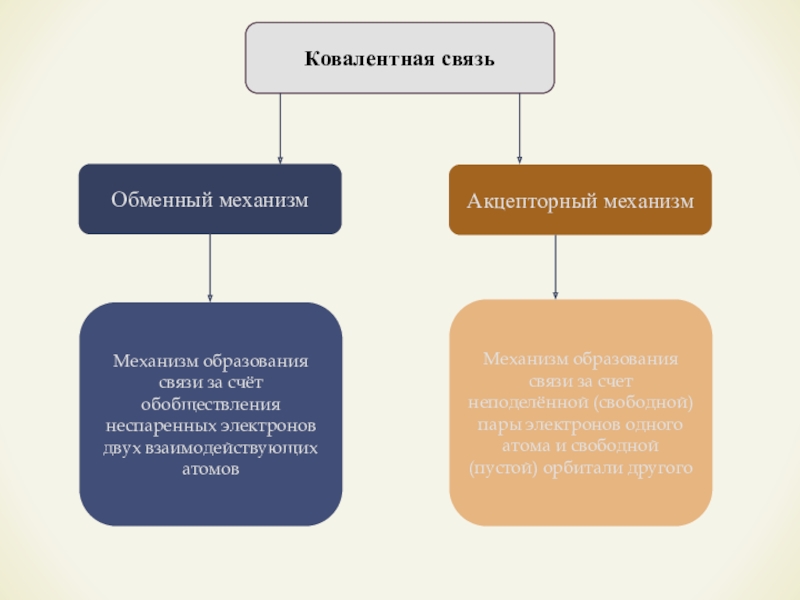
- 11. Ковалентная связьОбменный механизмАкцепторный механизмМеханизм образования связи за
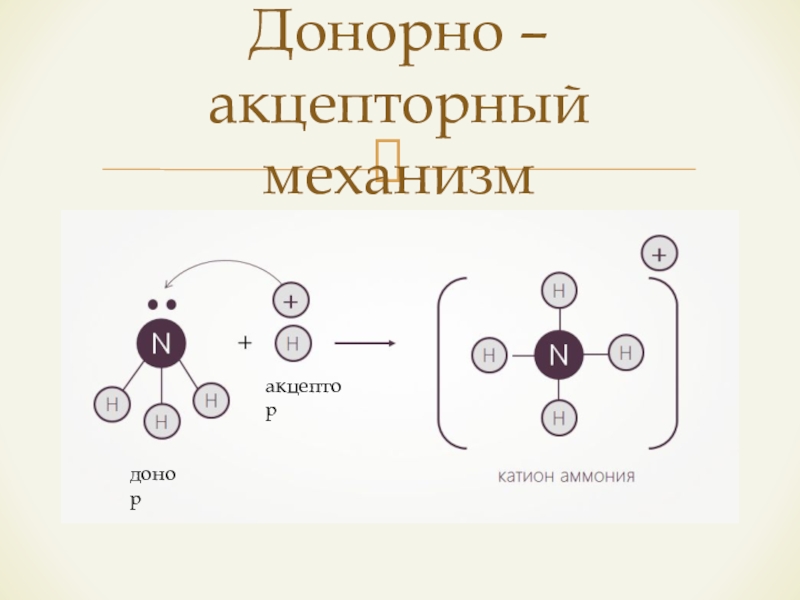
- 12. Донорно – акцепторный механизмдоноракцептор
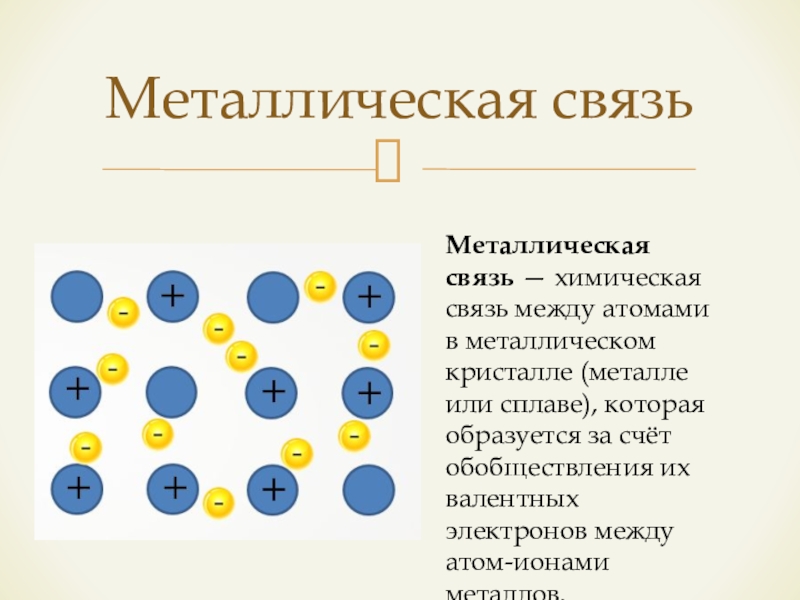
- 13. Металлическая связьМеталлическая связь — химическая связь между
- 14. Сходство металлической связи с ионной проявляется в
- 15. Межмолекулярная водородная связь – это связь между
- 16. Внутримолекулярная водородная связь – это связь, которая
Под химической связью понимаются электрические силы притяжения, удерживающие частицы друг около друга. Частицами могут быть атомы, ионы, молекулы.
Слайд 2Под химической связью понимаются электрические силы притяжения, удерживающие частицы друг около
друга. Частицами могут быть атомы, ионы, молекулы.
Слайд 3Причина образования химической связи — стремление атомов посредством взаимодействия с другими
атомами достичь более устойчивого состояния.
Электроотрицательность (ЭО) – способность притягивать электроны.
Если атомы обладают одинаковой ЭО, возникает ковалентная неполярная связь;
Если атомы обладают ЭО разной, но не резко отличаются, разность в ЭО < 1,7 – возникает ковалентная полярная связь;
Если атомы обладают ЭО разной, резко отличаются, разность в ЭО > 1,7 – возникает ионная связь.
Электроотрицательность (ЭО) – способность притягивать электроны.
Если атомы обладают одинаковой ЭО, возникает ковалентная неполярная связь;
Если атомы обладают ЭО разной, но не резко отличаются, разность в ЭО < 1,7 – возникает ковалентная полярная связь;
Если атомы обладают ЭО разной, резко отличаются, разность в ЭО > 1,7 – возникает ионная связь.
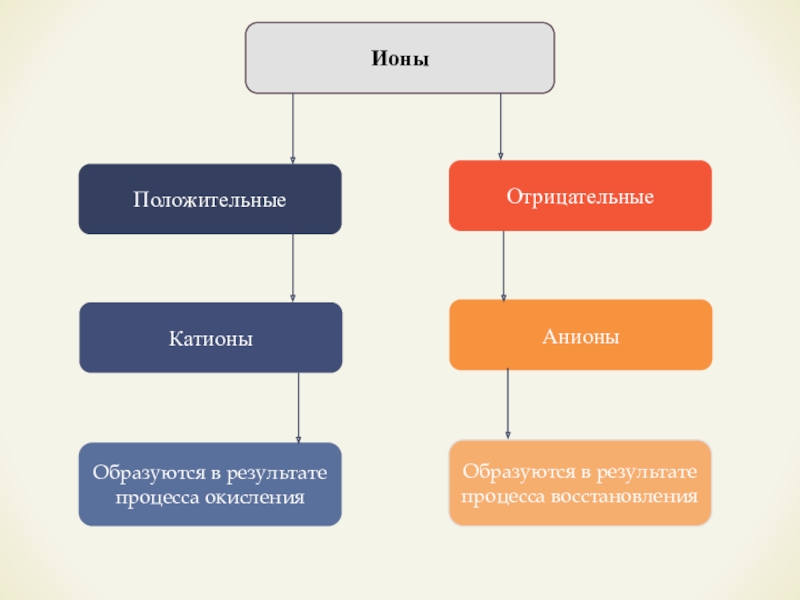
Слайд 5Ионы
Положительные
Отрицательные
Катионы
Образуются в результате процесса окисления
Анионы
Образуются в результате процесса восстановления
Слайд 11Ковалентная связь
Обменный механизм
Акцепторный механизм
Механизм образования связи за счёт обобществления неспаренных электронов
двух взаимодействующих атомов
Механизм образования связи за счет неподелённой (свободной) пары электронов одного атома и свободной (пустой) орбитали другого
Слайд 13Металлическая связь
Металлическая связь — химическая связь между атомами в металлическом кристалле
(металле или сплаве), которая образуется за счёт обобществления их валентных электронов между атом-ионами металлов.
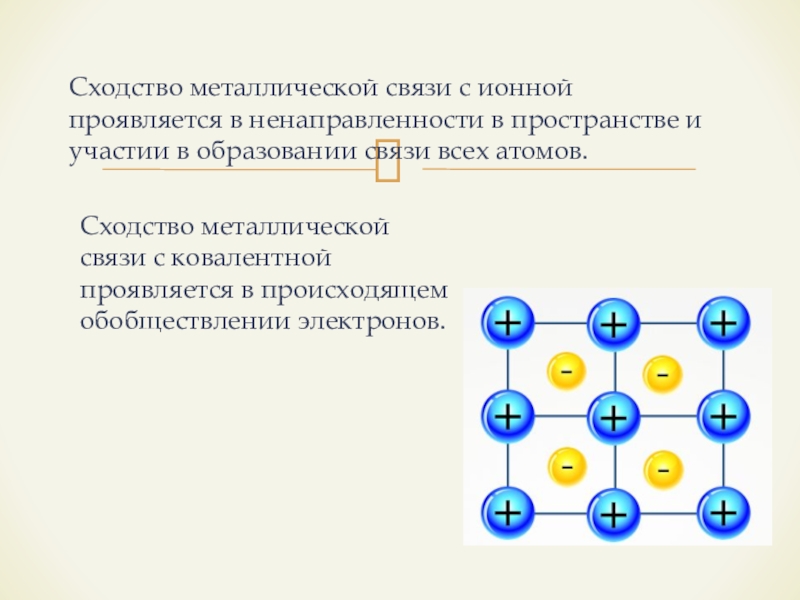
Слайд 14Сходство металлической связи с ионной проявляется в ненаправленности в пространстве и
участии в образовании связи всех атомов.
Сходство металлической связи с ковалентной проявляется в происходящем обобществлении электронов.
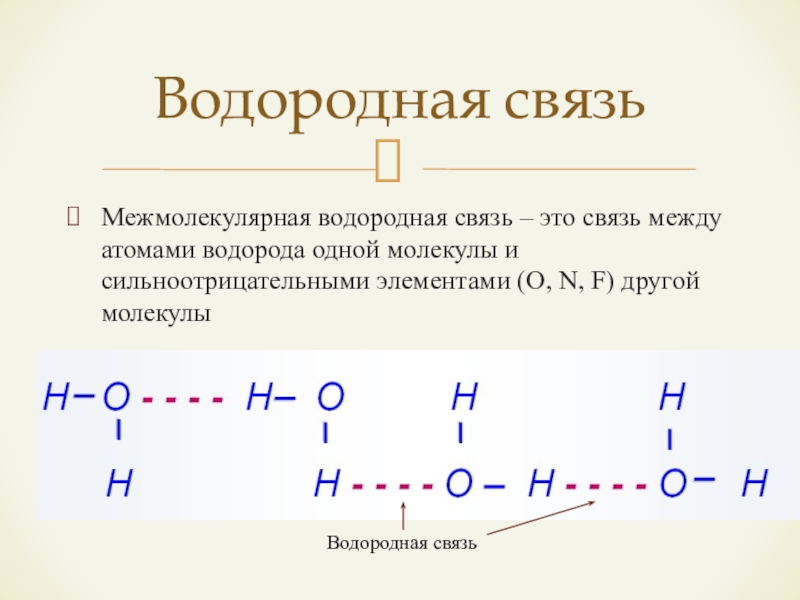
Слайд 15Межмолекулярная водородная связь – это связь между атомами водорода одной молекулы
и сильноотрицательными элементами (O, N, F) другой молекулы
Водородная связь
Водородная связь
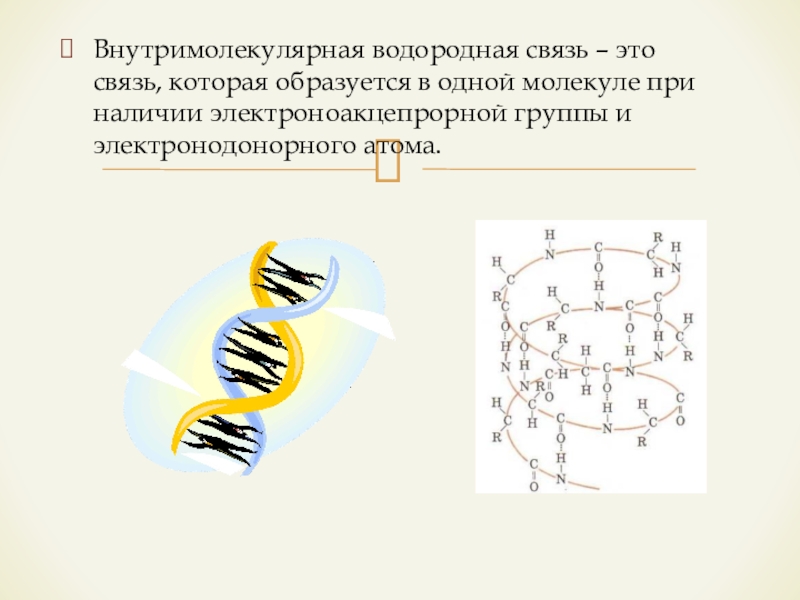
Слайд 16Внутримолекулярная водородная связь – это связь, которая образуется в одной молекуле
при наличии электроноакцепрорной группы и электронодонорного атома.