- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
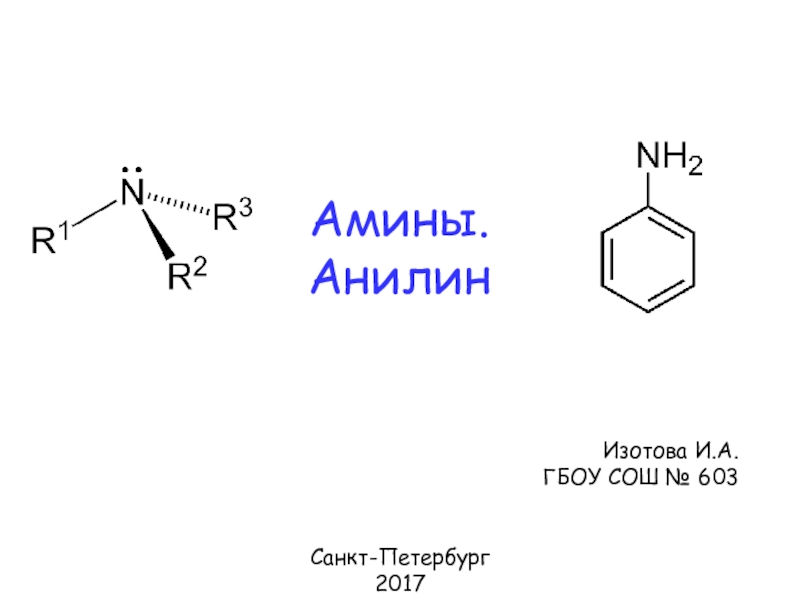
Презентация, доклад по химии. Тема урока Амины. Анилин
Содержание
- 1. Презентация по химии. Тема урока Амины. Анилин
- 2. Амины — это органические соединения, являющиеся производными аммиака,
- 3. Амины: Первичные Н3С
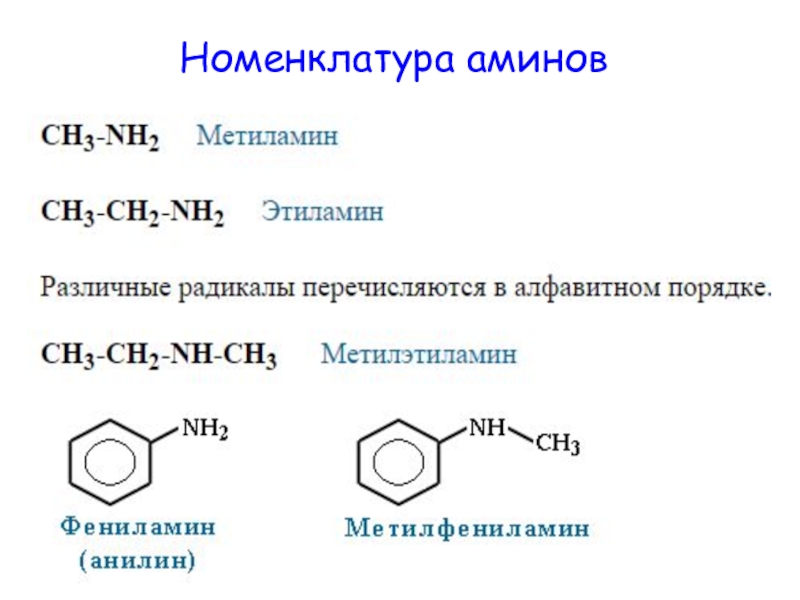
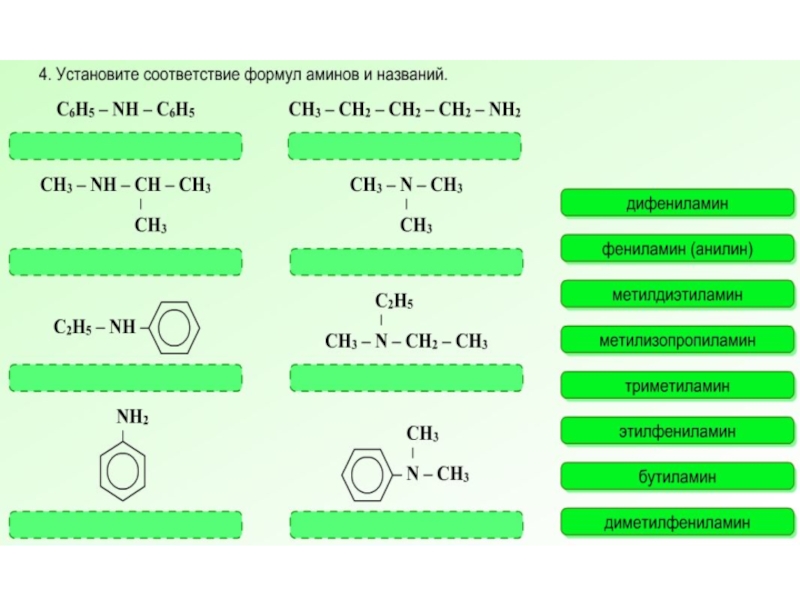
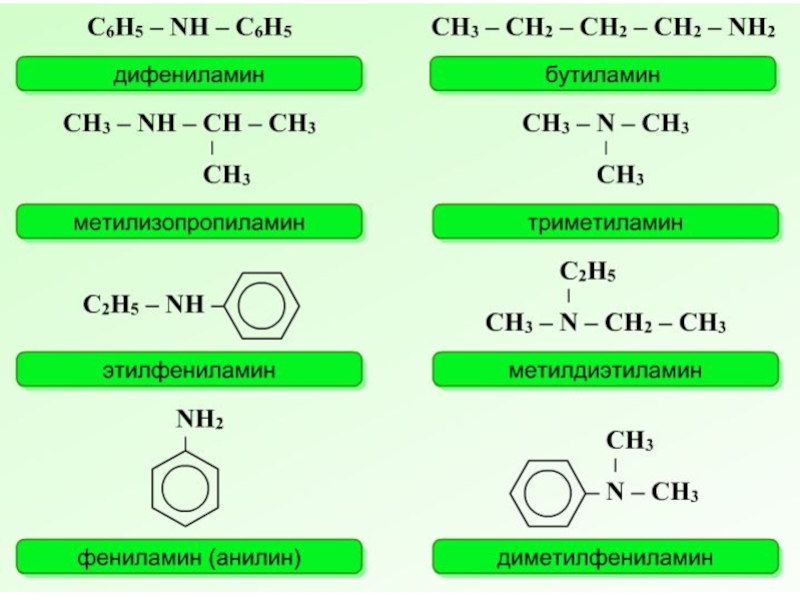
- 4. Номенклатура аминов
- 5. Н3С – NH2 метиламин –
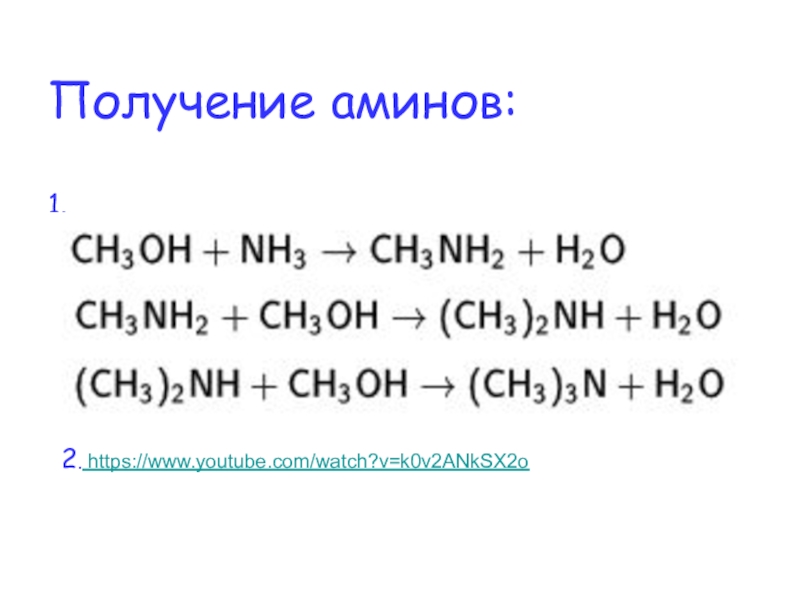
- 6. Получение аминов: 1.2. https://www.youtube.com/watch?v=k0v2ANkSX2o
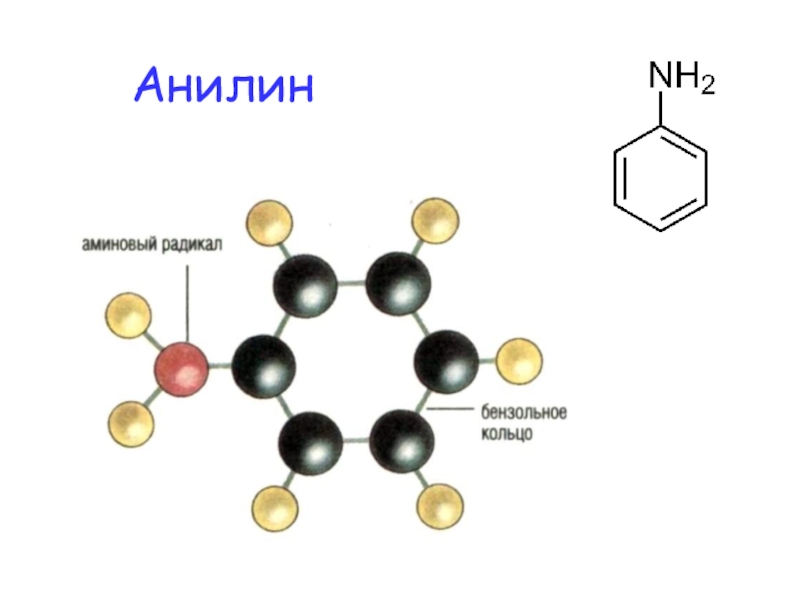
- 7. Анилин
- 8. Анилин (фениламин, аминобензол) С6Н5NН2 бесцветная
- 9. Химические свойства аминов1. Амины - органические основания,реагируют
- 10. 2. Галогенирование (реакция замещения). Бромирование
- 11. 3. Горение: 4Н3С–NH2 + 9О2 → 4СО2
- 12. Николай Николаевич Зинин Открыл в 1842 году
- 13. Получение анилинаВ промышленности: восстановление нитробензола водородом при
- 14. Получение В промышленности анилин получают в
- 15. Слайд 15
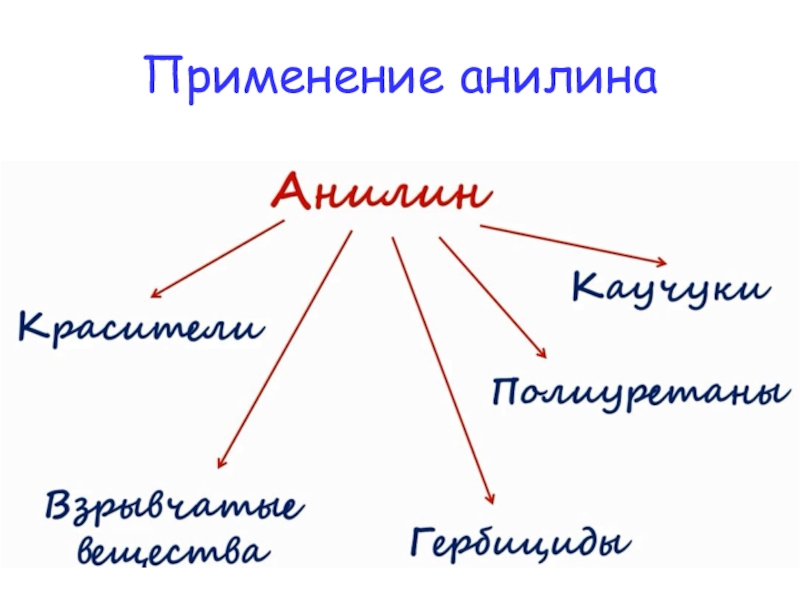
- 16. Применение анилина
- 17. Чем больше электронная плотность на атоме азота, тем сильнее выражены основные свойства амина
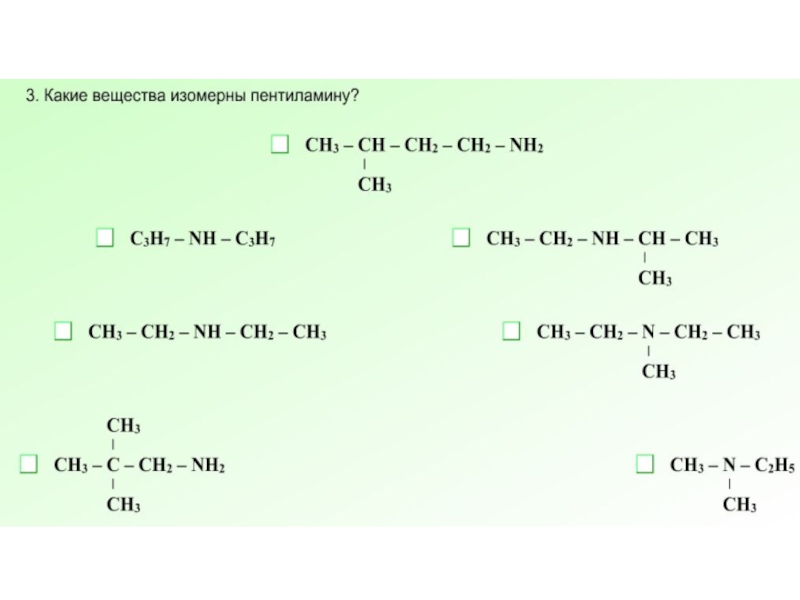
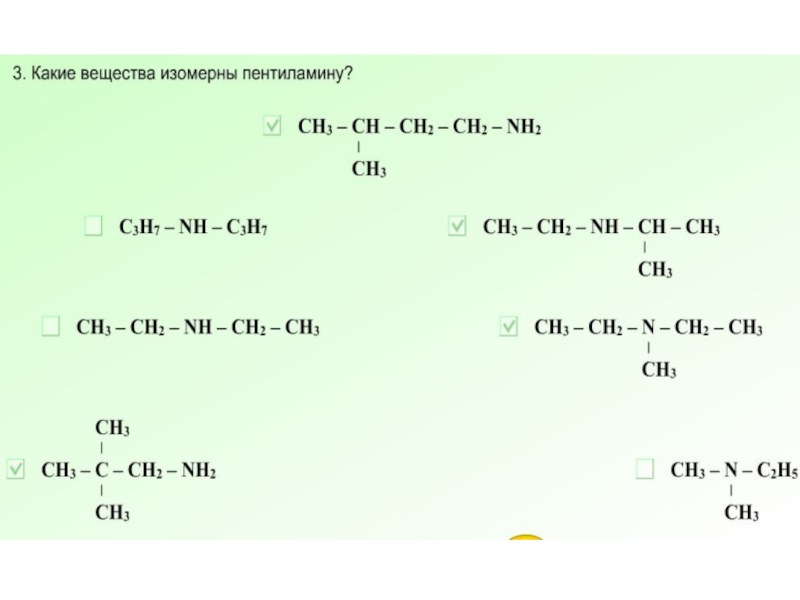
- 18. Повторение изученного материала
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Слайд 25
- 26. Слайд 26
- 27. Решите задачуОрганическое вещество содержит:38,7% углерода,45,15% азота и
- 28. Интернет-ресурсы:http://earchiv.ru/nauchno_tehnicheskiy_entsiklopedicheskiy_slovar/page/anilin.192/http://www.meysner.ru/index.php/2009-12-20-11-39-52/2009-11-05-19-58-09/2010-02-10-09-38-42/3271-2010-02-10-07-09-43http://900igr.net/prezentatsii/khimija/KHimija-aminy/012-Primenenie-aminov.htmlhttps://www.youtube.com/watch?v=2c6J-4sNGPchttps://www.youtube.com/watch?v=d_pxNj5sd8ghttps://www.youtube.com/watch?v=k0v2ANkSX2o
Амины — это органические соединения, являющиеся производными аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
Слайд 2Амины —
это органические соединения, являющиеся производными аммиака,
в молекуле которого
один, два или три атома водорода замещены на углеводородные радикалы.
Слайд 3
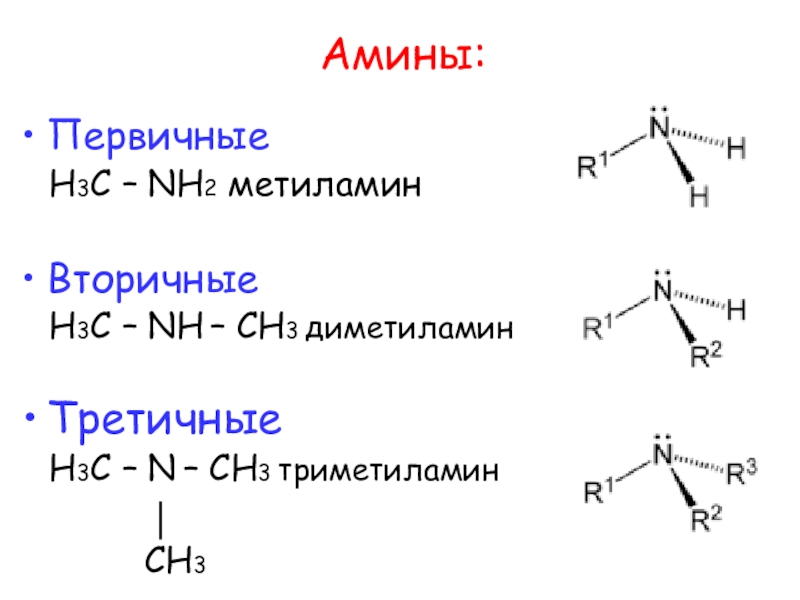
Амины:
Первичные
Н3С – NH2 метиламин
Вторичные
Н3С – NH –
СН3 диметиламин
Третичные
Н3С – N – СН3 триметиламин
СН3
Третичные
Н3С – N – СН3 триметиламин
СН3
Слайд 5
Н3С – NH2 метиламин –
бесцветный газ с запахом аммиака,
хорошо растворим в воде;
горюч и взрывоопасен.
Применяется для синтеза пестицидов, лекарств, растворителей, красителей, фотоматериалов,
взрывчатых веществ…
Слайд 8
Анилин (фениламин, аминобензол) С6Н5NН2
бесцветная маслянистая жидкость,
плохо растворимая в воде;
на
воздухе быстро окисляется и приобретает красно-бурую окраску;
Яд
https://www.youtube.com/watch?v=2c6J-4sNGPc
Яд
https://www.youtube.com/watch?v=2c6J-4sNGPc
Слайд 9Химические свойства аминов
1. Амины - органические основания,
реагируют с кислотами, образуя соли:
С6Н5NН2
+ HCl → С6Н5NН3Сl
хлорид фениламмония
https://www.youtube.com/watch?v=gPG3vCFBNIU
Н3С – NH2 + HCl → СН3NН3Сl
хлорид метиламмония
хлорид фениламмония
https://www.youtube.com/watch?v=gPG3vCFBNIU
Н3С – NH2 + HCl → СН3NН3Сl
хлорид метиламмония
Слайд 10
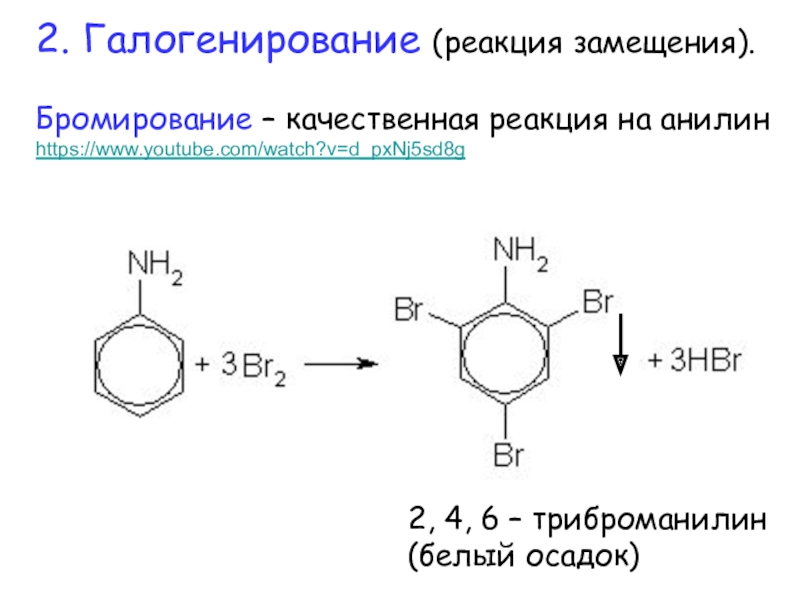
2. Галогенирование (реакция замещения).
Бромирование – качественная реакция на анилин
https://www.youtube.com/watch?v=d_pxNj5sd8g
2, 4, 6
– триброманилин (белый осадок)
Слайд 113. Горение:
4Н3С–NH2 + 9О2 → 4СО2 + 10Н2О + 2N2
метиламин
4С6Н5NH2 + 31О2 →24СО2 + 14Н2О + 2N2
анилин
Слайд 12Николай Николаевич Зинин
Открыл в 1842 году реакцию восстановления ароматических нитросоединений
и получил анилин.
Доказал, что амины – основания, способные образовывать соли с различными кислотами.
Синтезировал и изучал многие органические соединения.
Доказал, что амины – основания, способные образовывать соли с различными кислотами.
Синтезировал и изучал многие органические соединения.
Слайд 13Получение анилина
В промышленности:
восстановление нитробензола водородом при 250-350°С
на никелевом или
медном катализаторе:
C6H5NO2 + 3Н2 → C6H5NH2 + 2Н2О
C6H5NO2 + 3Н2 → C6H5NH2 + 2Н2О
t, Ni
Слайд 14
Получение
В промышленности анилин получают в две стадии:
На первой стадии бензол нитруется
смесью концентрированной азотной и серной кислот при температуре 50 - 60°C в результате образуется нитробензол.
На втором этапе нитробензол гидрируют при температуре 200-300°C в присутствии катализаторов
Впервые восстановление нитробензола было произведено с помощью железа:
Другим способом получение анилина является восстановление нитросоединений — Реакция Зинина:
На втором этапе нитробензол гидрируют при температуре 200-300°C в присутствии катализаторов
Впервые восстановление нитробензола было произведено с помощью железа:
Другим способом получение анилина является восстановление нитросоединений — Реакция Зинина:
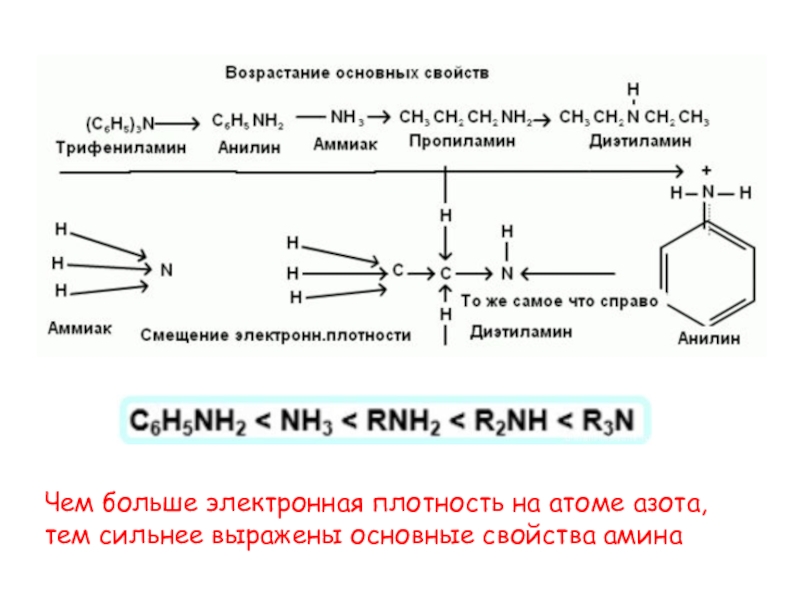
Слайд 17Чем больше электронная плотность на атоме азота,
тем сильнее выражены основные
свойства амина
Слайд 27Решите задачу
Органическое вещество содержит:
38,7% углерода,
45,15% азота
и 16,15% водорода.
Относительная плотность
его паров по водороду равна 15,5.
Определите формулу вещества.
Определите формулу вещества.