- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Щелочные металлы
Содержание
- 1. Презентация по химии Щелочные металлы
- 2. Щелочные металлы – элементы I А группы
- 3. Слайд 3
- 4. Нахождение в природеКаменная соль Глауберова соль сильвиниткарналлитNaCl
- 5. Физические свойстваМеталлический цезий в ампулеМеталлический рубидий в
- 6. Б и о л о г и
- 7. Содержание ионов щелочных металлов в человеческом
- 8. Х И М И Ч Е С
- 9. Взаимодействие с водойВсе щелочные металлы активно реагируют
- 10. Окраска пламени ионами щелочных металловLi+Rb+Na+Cs+К+
- 11. биологическая роль и применение калия и натрияответответответNaClКристалли-ческая содаNa2CO3*10H2OПитьевая содаNaHCO3поташK2CO3Калийная селитраKNO3Глауберова сольNa2SO4*10H2O
- 12. Применение щелочных металлов
- 13. § 112. Выполнить цепочку химических превращений: Na →Na2O2→Na2O→Na2CO3 NaOH → NaClДомашнее задание
Слайд 2Щелочные металлы – элементы I А группы
Li
Li (1817) лат. " литос" - камень
Na (1807) араб. "натрум" -сода
К (1807) араб. "алкали" - щелочь
Rb (1861) лат. "рубидус" - темно-красный
Cs (1860) лат. "цезиус" - небесно-голубой
Fr (1939) от названия страны Франция.
Положение в периодической системе Д.И.Меделеева
Слайд 3 общая характеристика элементов I группы Общая характеристика элементов
Li
Na
K
Rb
Cs
Fr
7
23
39
85
133
[223]
2s1
3s1
4s1
5s1
6s1
7s1
))
)))
))))
)))))
))))))
)))))))
усиливаются
усиливаются
Элемент
Аr
Валентные
электроны
Число энергетических уровней
Металлические свойства
Восстановительные свойства
R
атома
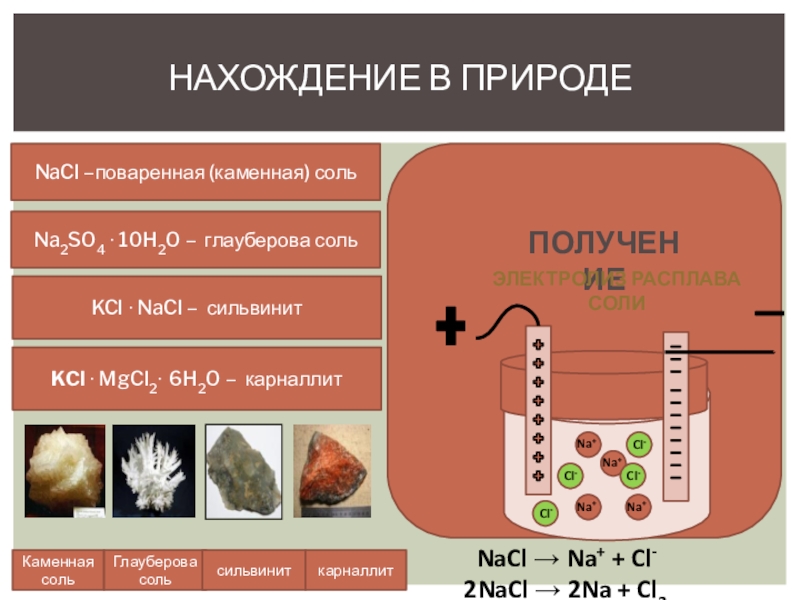
Слайд 4Нахождение в природе
Каменная соль
Глауберова соль
сильвинит
карналлит
NaCl –поваренная (каменная) соль
Na2SO4 ∙
KCl ∙ NaCl – сильвинит
KCl ∙ MgCl2· 6H2O – карналлит
получение
Электролиз расплава соли
NaCl → Na+ + Cl-
2NaCl → 2Na + Cl2
получение
Электролиз расплава соли
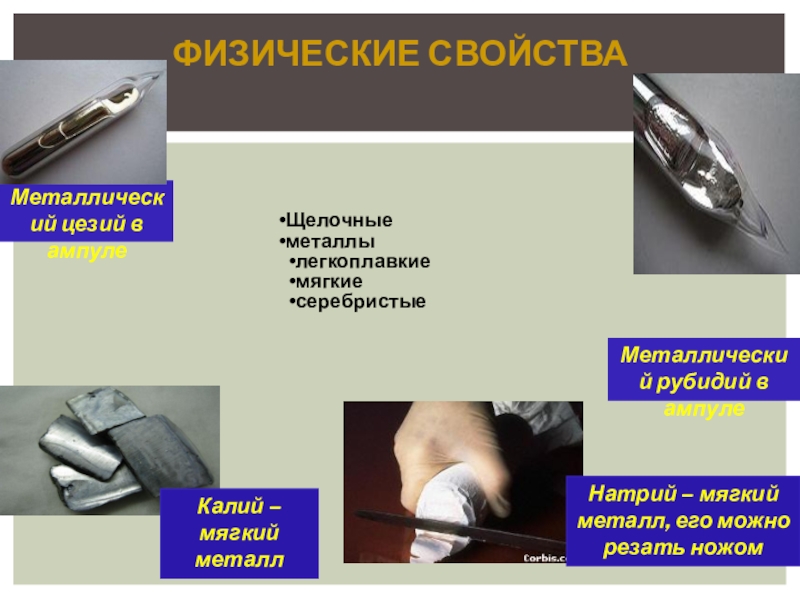
Слайд 5Физические свойства
Металлический цезий в ампуле
Металлический рубидий в ампуле
Натрий – мягкий металл,
Калий – мягкий металл
Слайд 6
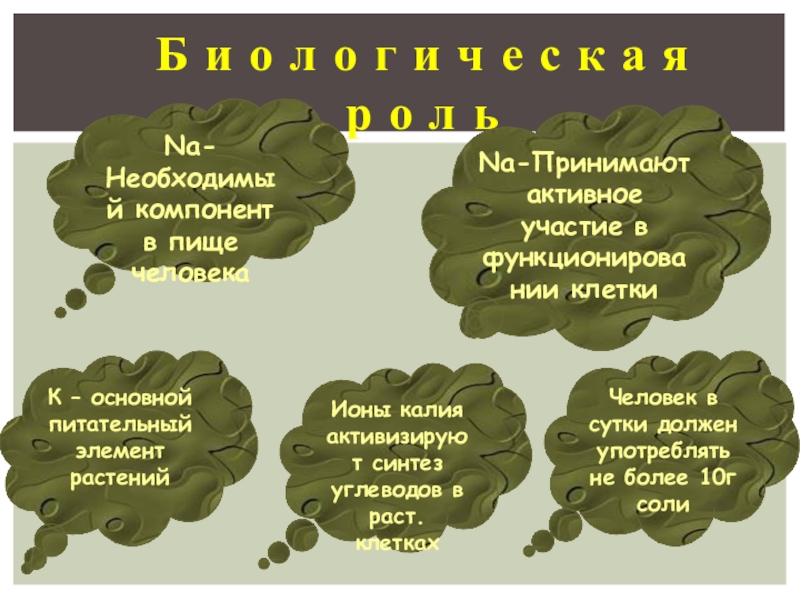
Б и о л о г и ч е с к
К – основной питательный элемент растений
Na-Необходимый компонент в пище человека
Ионы калия активизируют синтез углеводов в раст. клетках
Человек в сутки должен употреблять не более 10г соли
Na-Принимают активное участие в функционировании клетки
Слайд 7
Содержание ионов щелочных металлов
в человеческом организме
Na 0,08%
Li 10 %
Rb 10 %
Cs 10 %
-4
-4
-5
макроэлементы
микроэлементы
Слайд 8Х И М И Ч Е С К И Е С
Щелочные металлы активно взаимодействуют почти со всеми неметаллами
2М0 + Н20 = 2М+1Н-1 (гидрид)
2М0 + Cl20 = 2M+1Cl-1 (хлорид)
2М0 + S0 = M+12S (сульфид)
С кислородом натрий и калий образуют не оксиды, а пероксиды:
2М0 + О20 = М+12О12 пероксид
Слайд 9
Взаимодействие с водой
Все щелочные металлы активно реагируют с водой, образуя
водорода:
2М0 + 2Н2О = 2М+1ОН + Н2
Скорость взаимодействия
щелочного металла с водой
увеличивается от лития к
цезию.
Кусочек металлического натрия реагирует с водой в присутствии фенолфталеина
Слайд 11 биологическая роль и применение
калия и натрия
ответ
ответ
ответ
NaCl
Кристалли-ческая сода
Na2CO3*10H2O
Питьевая сода
NaHCO3
поташ
K2CO3
Калийная
KNO3
Глауберова соль
Na2SO4*10H2O
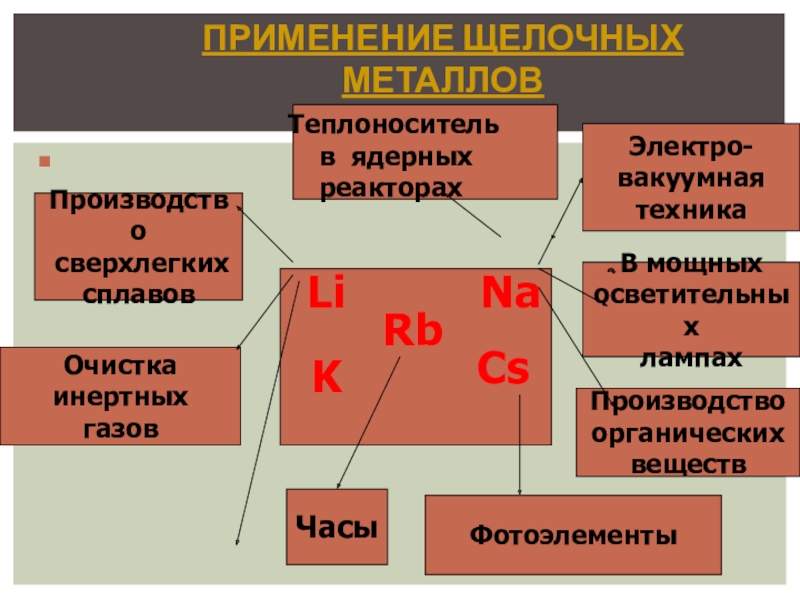
Слайд 12Применение щелочных металлов
Электро-
вакуумная
техника
В мощных
осветительных
лампах
Производство
органических
веществ
Производство
сверхлегких
сплавов
Фотоэлементы
Очистка
инертных
газов
Li
Na
Cs
Rb
K
Теплоноситель
в ядерных
реакторах
Часы
Слайд 13§ 11
2. Выполнить цепочку химических превращений:
Na →Na2O2→Na2O→Na2CO3
NaOH →
Домашнее задание