Тема: Практическая работа «Качественное определение
углерода, водорода, хлора в органических соединениях»
Выполнила: учитель биологии и химии
Мустафина Ильзия Райнуровна
2013
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Практическая работа Качественное определение углерода, водорода, хлора в органических соединений
Содержание
- 1. Презентация по химии Практическая работа Качественное определение углерода, водорода, хлора в органических соединений
- 2. СодержаниеРекомендации к определению « С, Н »
- 3. Рекомендации к выполнению эксперимента по определению углерода
- 4. Лабораторное оборудованиеЛабораторный физический штатив с лапкойлапкаХимический стаканКруглодонная колбаСпиртовка с колпачкомпробиркаФарфоровая чашка
- 5. Опыт №1. Качественное определение углерода в
- 6. Опыт №2. Качественное определение водорода в
- 7. Опыт. Качественное определение углерода и водорода
- 8. Оформление работы к опытам № 1, 2
- 9. Опыт №3. Определение углерода в
- 10. H2OОпыт № 4. Определение углерода в сахаре
- 11. Опыт №5. Качественное определение хлора в
- 12. Прокаленную медную спираль помещаем в раствор органического вещества, содержащего хлор, например тетрахлорметан CCl4
- 13. Затем медную спираль повторно вносим в пламя
- 14. Проверь свои знания. Тест № 1 Вместо
- 15. Проверь свои знания. Тест № 2 Вместо
- 16. Контроль знаний по теме « Алканы »
- 17. Контроль знаний по теме « Алканы »
- 18. Полные ответы к контрольным тестам
- 19. Полные ответы к контрольным тестам
- 20. Короткие ответы к контрольным тестам по теме
- 21. Библиография 1. Рудзитис Г. Е. и
Слайд 1Муниципальное бюджетное образовательное учреждение «Средняя общеобразовательная школа с.Маскара» Кукморского муниципального района
Слайд 2Содержание
Рекомендации к определению « С, Н » в парафине
Лабораторное оборудование
Опыт
Опыт №2. Определение водорода в органическом веществе
Оформление работы к опытам № 1,2
Опыт №3. Определение углерода пробой на обугливание в
целлюлозе или в бумаге.
Опыт №4. Определение углерода в сахаре или сахарозе
пробой на обугливание.
Опыт №5. Определение хлора в органическом веществе.
Проверь свои знания. Тест №1
Проверь свои знания. Тест №2
Контрольные тесты № 1 – 2
Полные ответы к тестам № 1 – 2
Короткие ответы к тестам № 1-2
Библиография
Слайд 3Рекомендации к выполнению эксперимента по определению углерода и водорода в парафине
1.
оксида меди и измельченного парафина до его плавления,
потом ее содержимое несколько раз встряхнуть для
перемешивания веществ .
2. Затем закрепите пробирку в штативе в горизонтальном
положении и поместите в нее немного безводного
светло-серого порошка сульфата меди.
3. Далее закройте пробирку пробкой с газоотводной
трубкой и нагревайте ее в течение 1 минуты.
4. После этого конец газоотводной трубки вставить в
пробирку с прозрачной известковой Ca(OH)2 или баритовой
водой Ba(OH)2 и пропускать через нее углекислый газ до
выпадения белого осадка.
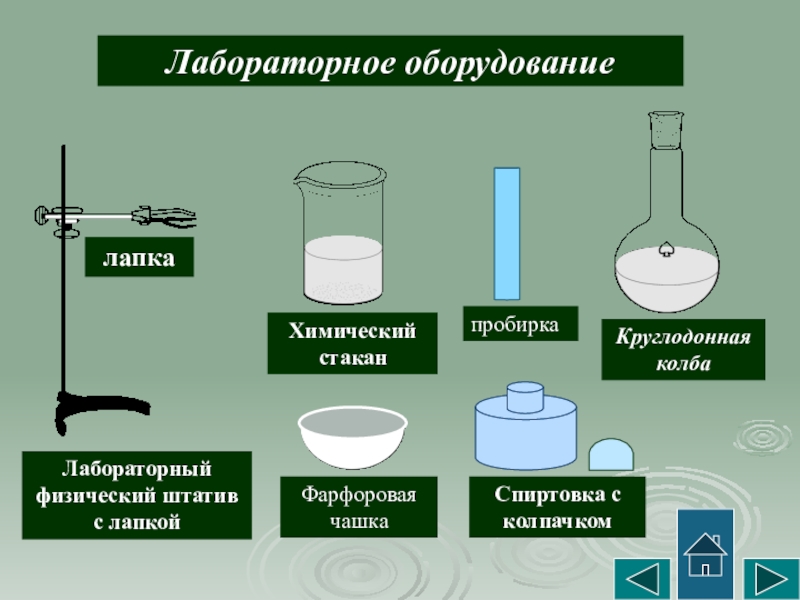
Слайд 4Лабораторное оборудование
Лабораторный физический штатив с лапкой
лапка
Химический стакан
Круглодонная колба
Спиртовка с колпачком
пробирка
Фарфоровая чашка
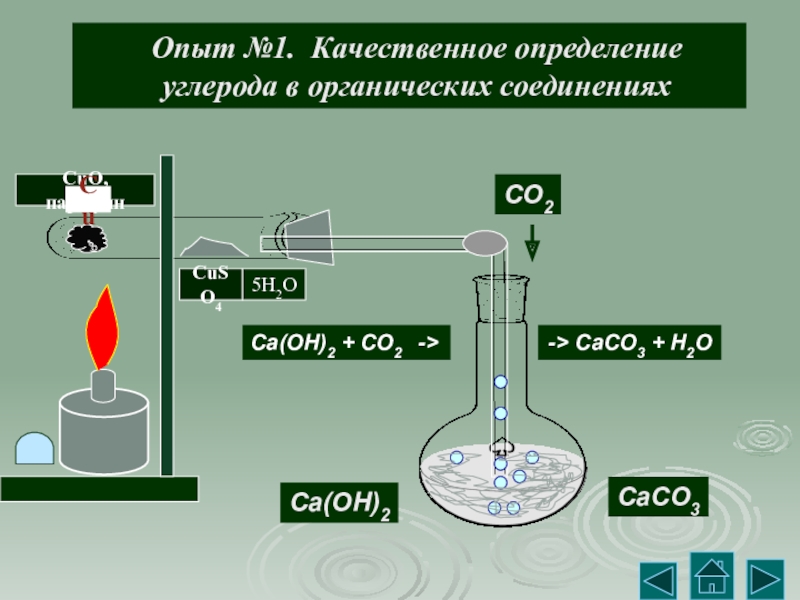
Слайд 5Опыт №1. Качественное определение
углерода в органических соединениях
CO2
Ca(OH)2
Ca(OH)2 + CO2
-> CaCO3 + H2O
CaCO3
CuSO4
CuO, парафин
Cu
5H2O
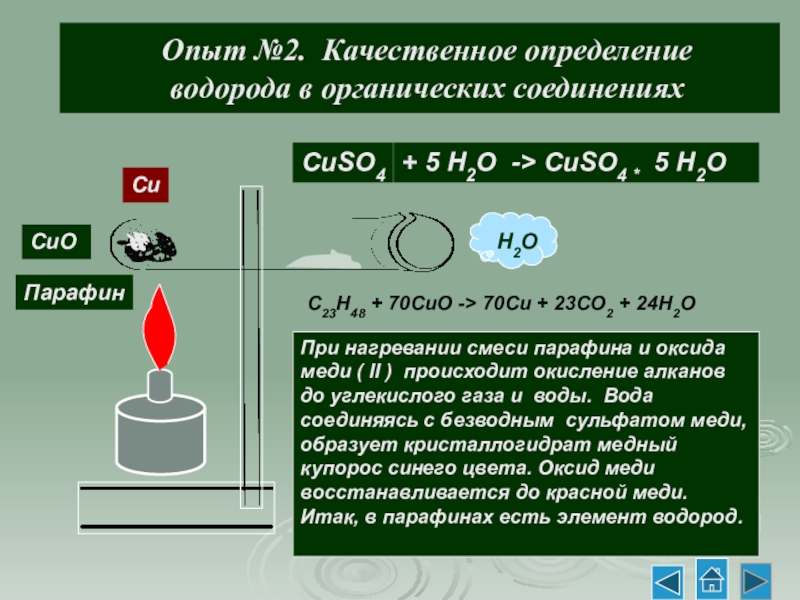
Слайд 6Опыт №2. Качественное определение
водорода в органических соединениях
H2O
CuSO4
+ 5 H2O ->
При нагревании смеси парафина и оксида меди ( II ) происходит окисление алканов до углекислого газа и воды. Вода соединяясь с безводным сульфатом меди, образует кристаллогидрат медный купорос синего цвета. Оксид меди восстанавливается до красной меди.
Итак, в парафинах есть элемент водород.
CuO
Парафин
Cu
C23H48 + 70CuO -> 70Cu + 23CO2 + 24H2O
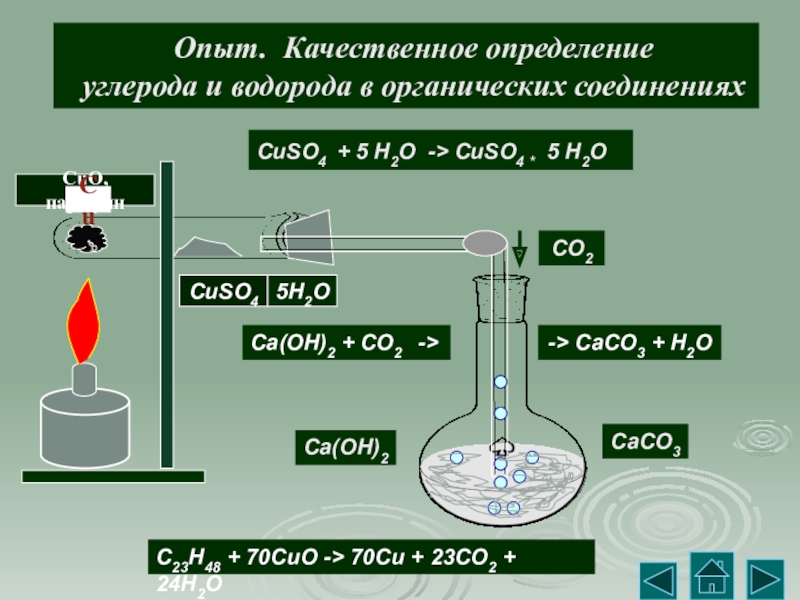
Слайд 7Опыт. Качественное определение
углерода и водорода в органических соединениях
CO2
Ca(OH)2
Ca(OH)2 + CO2
-> CaCO3 + H2O
CaCO3
CuSO4
CuO, парафин
Cu
5H2O
C23H48 + 70CuO -> 70Cu + 23CO2 + 24H2O
CuSO4 + 5 H2O -> CuSO4 * 5 H2O
Слайд 8Оформление работы к опытам № 1, 2 Качественное определение углерода и водорода
1. Закрепили в штативе пробирку со смесью парафина и оксида меди.
Поместили в нее немного безводного сульфата меди. Закрыли пробирку
пробкой с газоотводной трубкой , конец которой поместили в другую
пробирку с известковой водой. Содержимое пробирки нагрели.
2. Наблюдаем следующие изменения: черный оксид меди покраснел, так
как образовалась красная медь; бесцветный сульфат меди приобрел
голубой цвет, потому что в результате гидратации образуется
кристаллогидрат медный купорос; углекислый газ проходящий через
известковую воду, вызвал ее помутнение.
3. Т.о. в результате окисления парафина оксидом меди образуются оксид
углерода (IV) и вода, которые содержат элементы углерод и водород.
а) C23H48 +70 CuO -> 23 CO2 + 24H2O + 70 Cu
б) CuSO4 + 5H2O -> CuSO4 * 5H2O;
в) Ca(OH)2 + CO2 -> CaCO3 + H2O
Слайд 9
Опыт №3. Определение углерода
в целлюлозе пробой на обугливание
На листе бумаге
(C6H10O5 )n
Концентрированная серная
кислота отщепляет воду
от органических веществ,
в данном случае от целлюлозы
из которой состоит бумага.
Происходит обугливание
бумаги, т.е. выделение
углерода в виде простого
вещества угля, сажи или копоти.
C
Слайд 10
H2O
Опыт № 4. Определение углерода
в сахаре ( сахарозе ) пробой
В фарфоровую чашку насыпали немного сахара . Затем чашку с сахаром нагрели. Сахар почернел
Происходит обугливание сахара, т. е.
выделение углерода в виде простого
вещества угля
t
C12H22O11 -> 12 C + 11 H2O
Слайд 11Опыт №5. Качественное определение
хлора в органических соединениях
Медную
проволоку
спираль
прокалили в
пламени
спиртовки, чтобы очистить от посторонних
веществ
Слайд 12Прокаленную медную спираль помещаем в раствор органического вещества, содержащего хлор, например
Слайд 13
Затем медную спираль повторно вносим в пламя спиртовки.
Медь с
Таким образом, органическое соединение содержит элемент хлор.
Слайд 14Проверь свои знания. Тест № 1
Вместо точек вставить правильный ответ
1. Известковая
через ее раствор ……
2. Помутнение известковой воды подтверждает
наличие в органическом веществе элемента ……
3. Оксид меди в реакции - …………
4. Из оксида меди образуется ….
5. Безводный сульфат меди становится синим,
так как образуется ……………
H
малахит
CO2
Cl
кислород
O
восстановитель
медный купорос
SO2
окислитель
C
CO
медь
Слайд 15Проверь свои знания. Тест № 2
Вместо точек вставить правильный ответ
1. Цвет
процесса ………..
2. Усредненная формула парафина …….
3. Образование CuSO4* 5H2O доказывает наличие в
органическом веществе элемента …
4. Формула тетрахлорметана …….
5. Пламя спиртовки окрашивается в зеленый цвет из-за
элемента ….
CH4
C8H18
S
CCl4
дегидратации
H
CHCl3
гидрирования
C23H48
C23H46
гидратации
O
Cu
Cl
C
Слайд 16Контроль знаний по теме « Алканы » № 1
1. Общая формула
2. При взаимодействии хлорметана с натрием образуется:
а) Пропан б) метан в) этан г) этилен
3. Для алканов характерны реакции:
а) Обмена б) замещения в) присоединения г) горения
4. Гомологи метана: а) C2H4 , C3H6 , C5H8 б) C3H4 , C3H8 , C5H10
в) C4H10 , C3H8 , C5H12 г) C2H6, C4H10 , C6H6
Слайд 17Контроль знаний по теме « Алканы » №2
1. В молекуле гексана
в состоянии гибридизации:
а) sp б) sp3d в) sp2 г) sp3
2. При нагревании ацетата натрия с гидроксидом натрия
образуется:
а) метан б) пропан в) этан г) бутан
3. Формула алкана, содержашего 6 атомов углерода:
а) C6H10 б) C6H14 в) C6H12 г) C6H6
4. В холодильных установках применяется:
а) C2H6 б) C3H7Cl в) CH3Cl г) CH4
Слайд 18Полные ответы к контрольным тестам по теме « Алканы »
1. Общая формула алканов: б) CnH2n+2
2. При взаимодействии хлорметана с натрием
образуется: в) этан
3. Для алканов характерны реакции: б) замещения
4. Гомологи метана: в) C4H10 , C3H8 , C5H12
Слайд 19Полные ответы к контрольным тестам по теме « Алканы »
1. В молекуле гексана орбитали каждого атома углерода
находятся в состоянии гибридизации: г) sp3
2. При нагревании ацетата натрия с гидроксидом
натрия образуется: а) метан
3. Формула алкана, содержашего 6 атомов углерода:
б) C6H14
4. В холодильных установках применяется: в) CH3Cl
Слайд 20Короткие ответы к контрольным тестам по теме « Алканы »
Тест №1
1
2 в
3 б
4 в
Тест№2
1 г
2 а
3 б
4 в
Слайд 21
Библиография
1. Рудзитис Г. Е. и Фельдман Ф. Г. « Химия -10
М. : Просвещение, 2008 год.
2. Пономарев В. Д. « Аналитическая химия »
М. : Медицина, 1992 год.
3. Цветков Л. А. « Органическая химия » М. :
Владос, 2001 год
4. Сафронова Л. В. « Практикум по химии »
авторская методическая разработка.