- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии ОВР в органической химии
Содержание
- 1. Презентация по химии ОВР в органической химии
- 2. Окисление спиртовВ качестве окислителей чаще всего используются: KMnO4 +H2SO4K2Cr2O7 + H2SO4O2 (Cu)CuO
- 3. Полное окисление спиртов (горение в кислороде)Спирты+О2→СО2+Н2О
- 4. Частичное окисление первичных спиртов
- 5. Частичное окисление вторичных спиртов
- 6. Частичное окисление третичных спиртов
- 7. Окисление альдегидовВ качестве окислителей используют:[Ag(NH3)2]OH (аммиачный раствор
- 8. Реакция серебряного зеркала
- 9. Окисление свежеосажденным гидроксидом меди (II)
- 10. Окисление перманганатом калия в кислой, нейтральной, щелочной средах
- 11. Особенности окисления муравьиного альдегида
- 12. Суммарное уравнение реакции:
- 13. Окисление алкеновПолное окислениеCnH2n + 1,5nO2 = nCO2 + nH2O
- 14. Неполное окисление
- 15. Окисление перманганатом калия в нейтральной среде (реакция Вагнера, продуктами являются двухатомные спирты)
- 16. Окисление перманганатом калия в кислой среде (образуются карбоновые кислоты или кетоны)
- 17. Окисление перманганатом калия в кислой среде (образуются карбоновые кислоты или кетоны)
- 18. Окисление перманганатом калия в кислой среде (образуются карбоновые кислоты или кетоны)
- 19. Окисление перманганатом калия в кислой среде (образуются карбоновые кислоты или кетоны)
- 20. Окисление алкенов в присутствии солей палладия (образуются альдегиды или кетоны)
- 21. Окисление алкинов. Реакция Кучерова (под воздействием воды
- 22. Окисление ацетилена KMnO4, K2Cr2O7 протекает с образованием
- 23. Окисление алкинов KMnO4, K2Cr2O7 протекает с образованием
- 24. Окисление бензола и его гомологов KMnO4, K2Cr2O7
- 25. Окисление кумола кислородом в присутствии катализатора (серной кислоты)
- 26. Окисление алкановПолное сгорание CnH2n+2 + O2 =
- 27. Неполное каталитическое окисление алкановC2H6 + O2 = CH3CHO + H2O2C4H10 + 5O2 = 4CH3COOH + 2H2O
- 28. Восстановительные процессыалкен + Н2 = алканалкин +
Окисление спиртовВ качестве окислителей чаще всего используются: KMnO4 +H2SO4K2Cr2O7 + H2SO4O2 (Cu)CuO
Слайд 2Окисление спиртов
В качестве окислителей чаще всего используются:
KMnO4 +H2SO4
K2Cr2O7 + H2SO4
O2
(Cu)
CuO
CuO
Слайд 7Окисление альдегидов
В качестве окислителей используют:
[Ag(NH3)2]OH (аммиачный раствор оксида серебра, реактив Толленса)
Cu(OH)2
(свежеосаждённый гидроксид меди (II)
KMnO4 +H2SO4
K2Cr2O7 + H2SO4
KMnO4 +H2SO4
K2Cr2O7 + H2SO4
Слайд 15Окисление перманганатом калия в нейтральной среде (реакция Вагнера, продуктами являются двухатомные
спирты)
Слайд 21Окисление алкинов. Реакция Кучерова (под воздействием воды в присутствии солей ртути
в кислой среде образуются альдегиды или кетоны)
Слайд 22Окисление ацетилена KMnO4, K2Cr2O7 протекает с образованием щавелевой кислоты (в кислой
среде),или ее соли (в нейтральной или щелочной средах)
Слайд 23Окисление алкинов KMnO4, K2Cr2O7 протекает с образованием карбоновых кислот (в кислой
среде),или их солей (в нейтральной или щелочной средах)
Слайд 26Окисление алканов
Полное сгорание
CnH2n+2 + O2 = CO2 + H2O
Неполное
сгорание
CnH2n+2 + O2 = CO + H2O
CnH2n+2 + O2 = C + H2O
CnH2n+2 + O2 = CO + H2O
CnH2n+2 + O2 = C + H2O
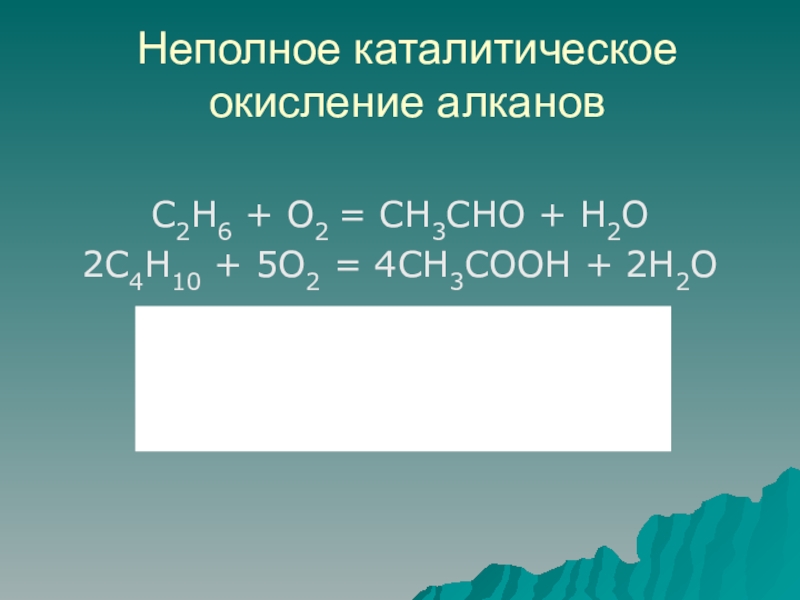
Слайд 27Неполное каталитическое окисление алканов
C2H6 + O2 = CH3CHO + H2O
2C4H10 +
5O2 = 4CH3COOH + 2H2O
Слайд 28Восстановительные процессы
алкен + Н2 = алкан
алкин + Н2 = алкен
бензол +
Н2 = циклогексан
циклогексан + Н2 =гексан
альдегид + Н2 = спирт (в присутствии катализатора никеля)
циклогексан + Н2 =гексан
альдегид + Н2 = спирт (в присутствии катализатора никеля)





![Презентация по химии ОВР в органической химии Окисление альдегидовВ качестве окислителей используют:[Ag(NH3)2]OH (аммиачный раствор оксида серебра, реактив Толленса)Cu(OH)2 Окисление альдегидовВ качестве окислителей используют:[Ag(NH3)2]OH (аммиачный раствор оксида серебра, реактив Толленса)Cu(OH)2 (свежеосаждённый гидроксид меди (II)KMnO4 +H2SO4K2Cr2O7 +](/img/thumbs/406ce3696a6c16fb2e51b07efe904f58-800x.jpg)