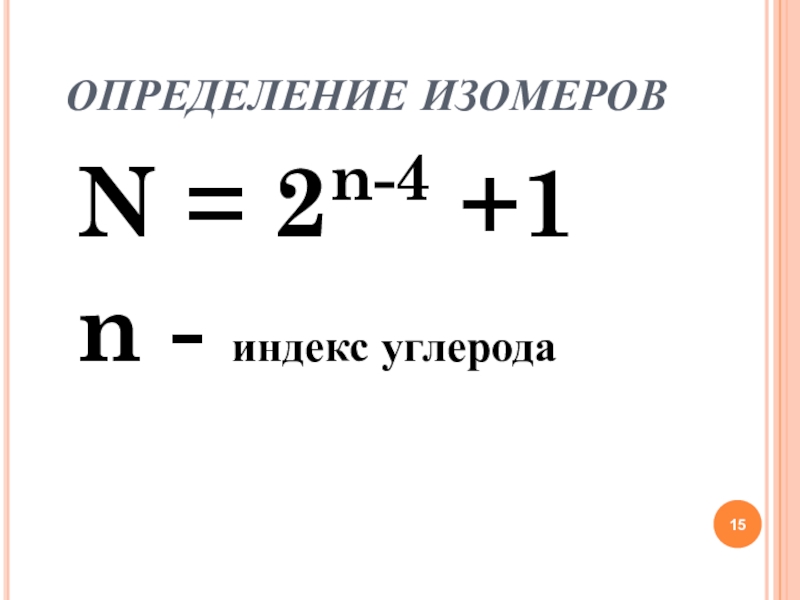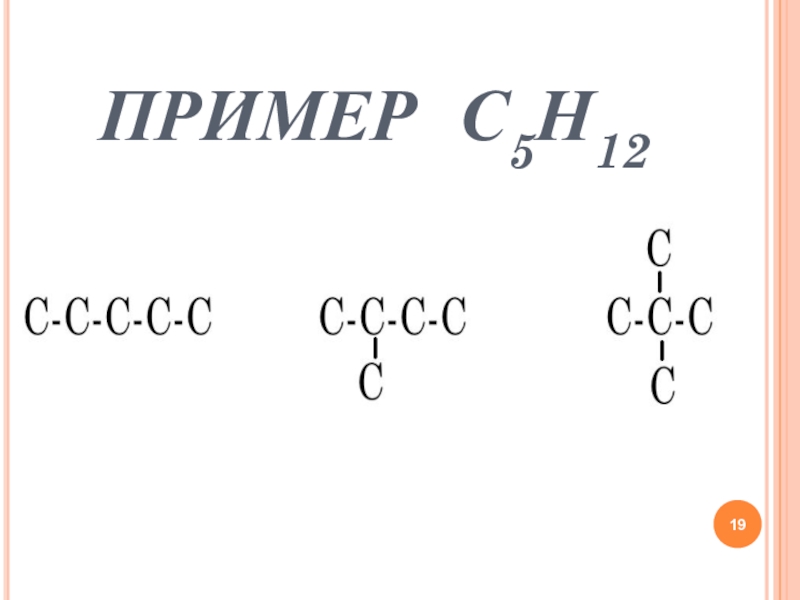- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему:Предельные углеводороды.Алканы.
Содержание
- 1. Презентация по химии на тему:Предельные углеводороды.Алканы.
- 2. ЦЕЛЬ УРОКА: Рассмотреть гомологический ряд предельных
- 3. ПЛАНГомологический ряд.Определение. Общая формула класса углеводородов.Строение алканов.Виды изомерии.Физические свойства.Химические свойства.Способы получения.Применение.
- 4. ГОМОЛОГИЧЕСКИЙ РЯДСН4 метан С2Н6 этан С3Н8
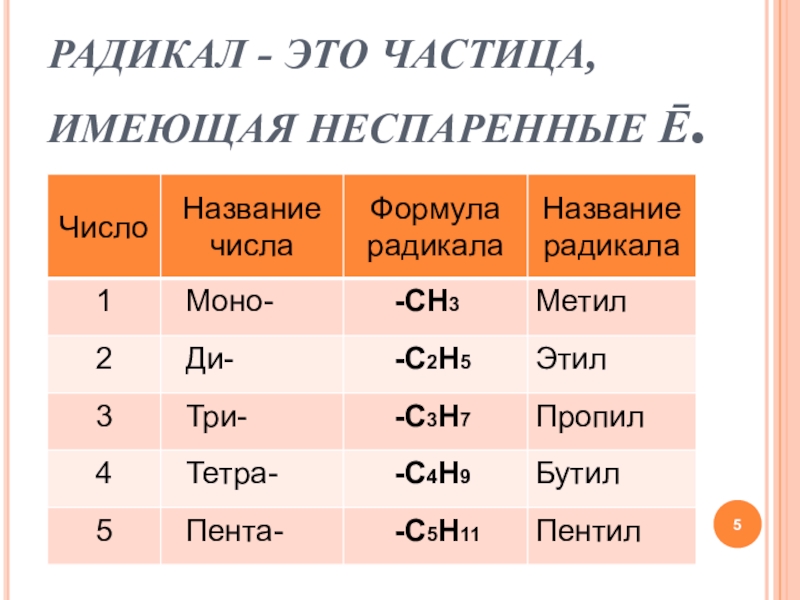
- 5. РАДИКАЛ - ЭТО ЧАСТИЦА, ИМЕЮЩАЯ НЕСПАРЕННЫЕ ē.
- 6. ОПРЕДЕЛЕНИЕ АЛКАНОВЭто предельные углеводороды, в молекулах которых все атомы связаны одинарными связями
- 7. ОБЩАЯ ФОРМУЛА АЛКАНОВСn H2n+2, где n=1,2,3…
- 8. СТРОЕНИЕ УГЛЕРОДА
- 9. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕДля алканов характерна sp³-гибридизация; Длина С-С
- 10. СТРОЕНИЕ МЕТАНАДля алканов характерна sp³-гибридизация; Длина С-С
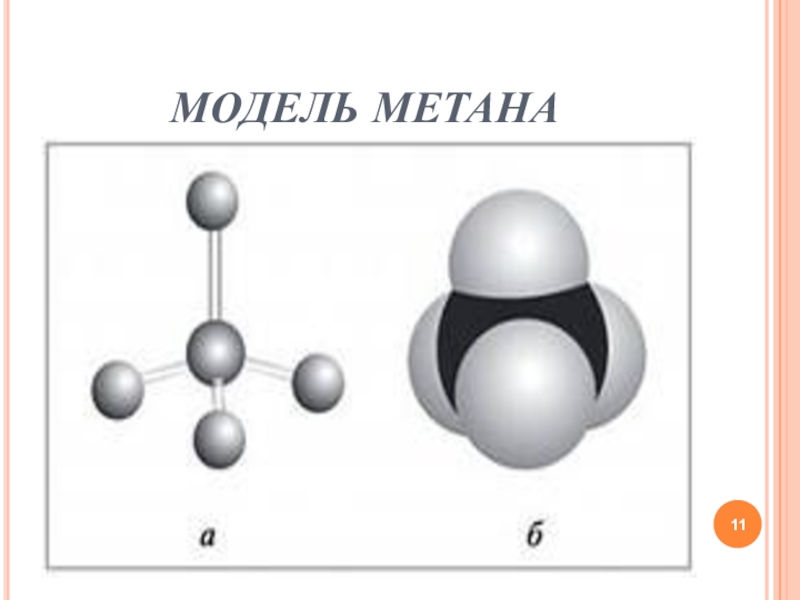
- 11. МОДЕЛЬ МЕТАНА
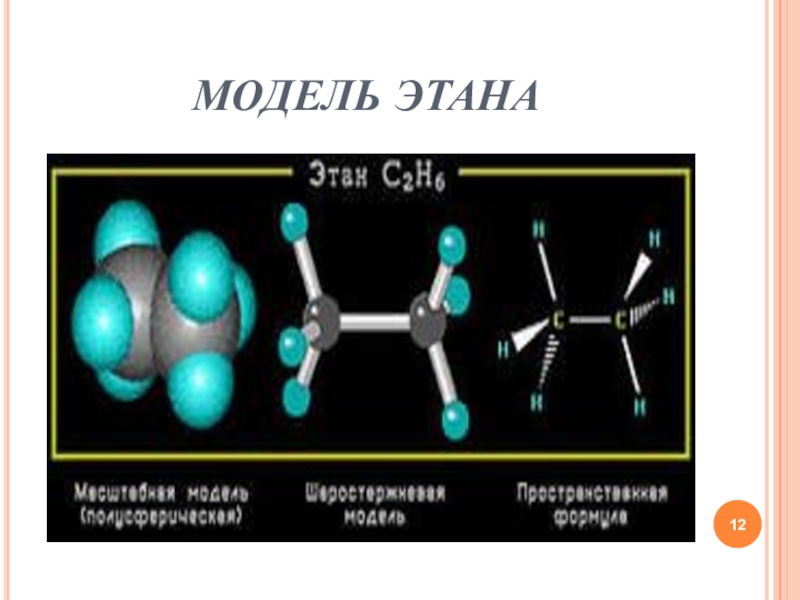
- 12. МОДЕЛЬ ЭТАНА
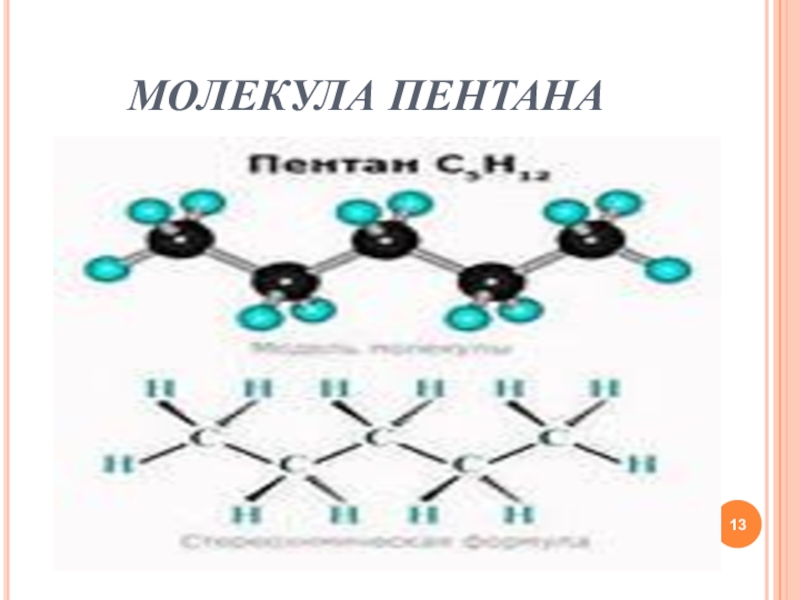
- 13. МОЛЕКУЛА ПЕНТАНА
- 14. ВИДЫ ИЗОМЕРИИСтруктурная: Углеродного скелета Положения кратной связи Положения функциональной группы Межклассовая
- 15. ОПРЕДЕЛЕНИЕ ИЗОМЕРОВ N = 2n-4 +1 n - индекс углерода
- 16. НОМЕНКЛАТУРАПервые 4 представителя- исторически сложившиеся названия.Следующие – греческие числительные + суффикс анРациональнаяТривиальнаяСистематическая
- 17. НОМЕНКЛАТУРА Международный Союз теоретической и прикладной химии ИЮПАК – Международная номенклатура ИЮПАК.
- 18. АЛГОРИТМ СОСТАВЛЕНИЯ НАЗВАНИЯ АЛКАНОВ 1. В структурной
- 19. ПРИМЕР С5Н12
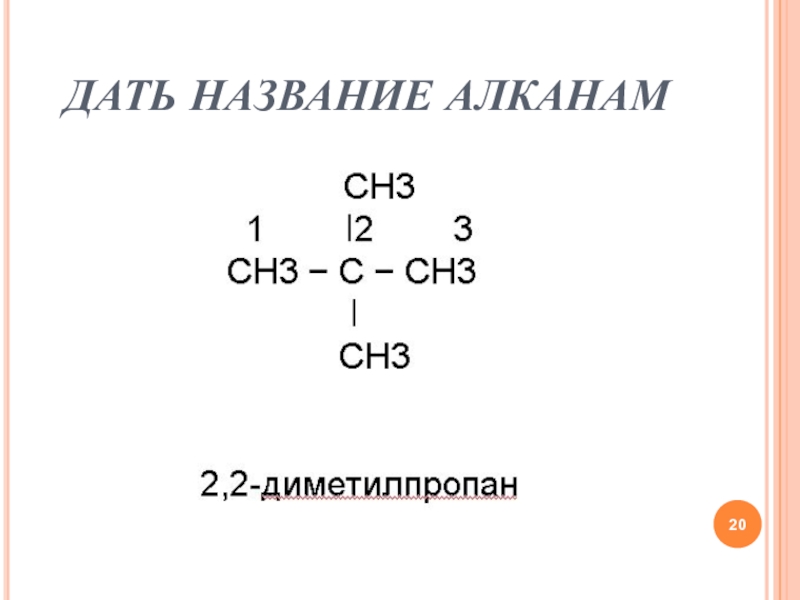
- 20. ДАТЬ НАЗВАНИЕ АЛКАНАМ
- 21. ДАТЬ НАЗВАНИЕ АЛКАНАМ 1
- 22. СОСТАВЛЕНИЯ НАЗВАНИЯ АЛКАНОВ 7
- 23. ФИЗКУЛЬТМИНУТКА
- 24. Гимнастика для глаз«КРЕСТ»
- 25. Гимнастика для глаз«Восьмерка»
- 26. Гимнастика для глаз«ЦИФЕРБЛАТ»
- 27. ФИЗИЧЕСКИЕ СВОЙСТВА С1 – С4 – газы,
- 28. ХИМИЧЕСКИЕ СВОЙСТВАРеакция горения:CH4 +2O2 → 2H2O + CO2↑Попробуй сам: C4H10 +O2 →
- 29. ПРОВЕРКА2C4H10 +13O2 → 10H2O + 8CO2↑
- 30. РЕАКЦИЯ ЗАМЕЩЕНИЯ СН4 + Cl2 = CH3Cl
- 31. РЕАКЦИЯ РАЗЛОЖЕНИЯПолное разложение метана:СН4 = С +2Н2 (10000 С)
- 32. РЕАКЦИЯ РАЗЛОЖЕНИЯНеполное разложение: 2СН4 = С2Н2 +3Н2
- 33. РЕАКЦИЯ ДЕГИДРИРОВАНИЯ Процесс отщепления молекул водорода от молекул органического соединения.
- 34. ПОЛУЧЕНИЕ АЛКАНОВПолучение метана В п
- 35. ПОЛУЧЕНИЕ МЕТАНА В л а б о
- 36. ПРИМЕНЕНИЕШирокоиспользуются в качестветоплива, в том числе длядвигателей внутреннегосгорания.
- 37. ПРИМЕНЕНИЕ1-3 – производство сажи(1 – картриджи;2 –
- 38. ЗАКРЕПЛЕНИЕПодчеркните в тесте правильныеответы.
- 39. ОСНОВНЫЕ ПОНЯТИЯ УРОКА
- 40. ДОМАШНЕЕ ЗАДАНИЕ §3, учить записи в тетрадях.
- 41. ИСТОЧНИКИ ИНФОРМАЦИИ, ПРЕДСТАВЛЕННОЙ В ПРЕЗЕНТАЦИИ1. О.С. Габриэлян.
ЦЕЛЬ УРОКА: Рассмотреть гомологический ряд предельных УВ, строение молекул алканов. Познакомиться с изомерией предельных УВ. Изучить
Слайд 2ЦЕЛЬ УРОКА:
Рассмотреть гомологический ряд предельных УВ, строение молекул алканов.
Познакомиться с изомерией предельных УВ.
Изучить физические, химические свойства алканов.
Рассмотреть основные способы получения алканов и применение алканов.
Слайд 3ПЛАН
Гомологический ряд.
Определение. Общая формула класса углеводородов.
Строение алканов.
Виды изомерии.
Физические свойства.
Химические свойства.
Способы получения.
Применение.
Слайд 4ГОМОЛОГИЧЕСКИЙ РЯД
СН4 метан С2Н6 этан
С3Н8 пропан С4Н10 бутан
С5Н12 пентан С6Н14 гексан
С7Н16
гептан С8Н18 октан
С9Н20 нонан С10Н22 декан
С9Н20 нонан С10Н22 декан
Слайд 6ОПРЕДЕЛЕНИЕ АЛКАНОВ
Это предельные углеводороды, в молекулах которых все атомы связаны одинарными
связями
Слайд 9ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ
Для алканов характерна sp³-гибридизация;
Длина С-С – связи = 0,154
нм
Углы между орбиталями = 109° 28´
Углы между орбиталями = 109° 28´
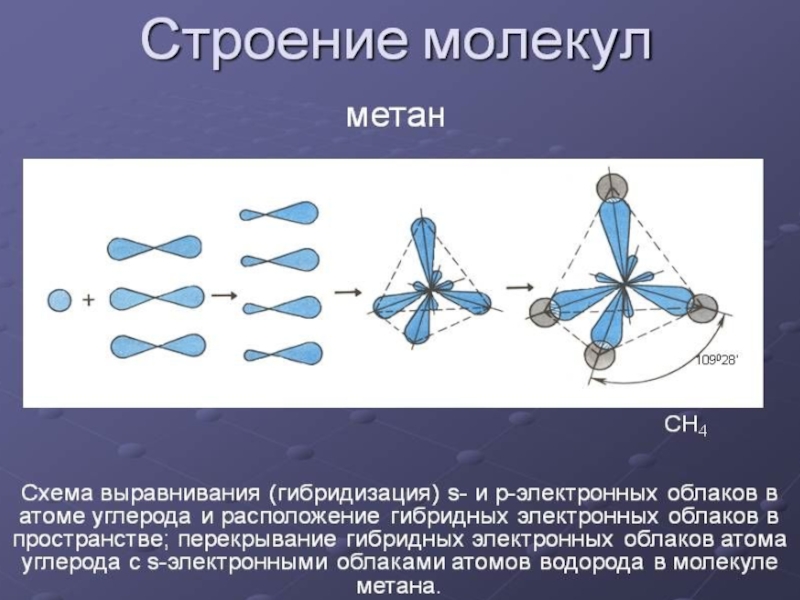
Слайд 10СТРОЕНИЕ МЕТАНА
Для алканов характерна sp³-гибридизация;
Длина С-С – связи = 0,154
нм
Углы между орбиталями=109° 28´
Углы между орбиталями=109° 28´
Слайд 14ВИДЫ ИЗОМЕРИИ
Структурная:
Углеродного скелета
Положения кратной связи
Положения функциональной группы
Межклассовая
Слайд 16НОМЕНКЛАТУРА
Первые 4 представителя- исторически сложившиеся названия.
Следующие – греческие числительные + суффикс
ан
Рациональная
Тривиальная
Систематическая
Рациональная
Тривиальная
Систематическая
Слайд 17НОМЕНКЛАТУРА
Международный Союз теоретической и прикладной химии ИЮПАК – Международная номенклатура
ИЮПАК.
Слайд 18АЛГОРИТМ СОСТАВЛЕНИЯ НАЗВАНИЯ АЛКАНОВ
1. В структурной формуле выбирают самую длинную
цепь атомов углерода (главную цепь)
2. Атомы углерода главной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
3. В начале названия перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле присутствует несколько одинаковых радикалов в их названии ставят соответственно частицы ди-, три-, тетра- и т.д.
4. Основой названия служит наименование предельного углеводорода с тем же числом атомов углерода, что и в главной цепи.
2. Атомы углерода главной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
3. В начале названия перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле присутствует несколько одинаковых радикалов в их названии ставят соответственно частицы ди-, три-, тетра- и т.д.
4. Основой названия служит наименование предельного углеводорода с тем же числом атомов углерода, что и в главной цепи.
Слайд 21ДАТЬ НАЗВАНИЕ АЛКАНАМ
1
2 3 4 1 2 3 4 5
CH3 − CH − CH2 − CH3 CH3 − CH − CH2 − CH − CH3
ǀ ǀ ǀ
CH3 CH3 CH3
CH3 − CH − CH2 − CH3 CH3 − CH − CH2 − CH − CH3
ǀ ǀ ǀ
CH3 CH3 CH3
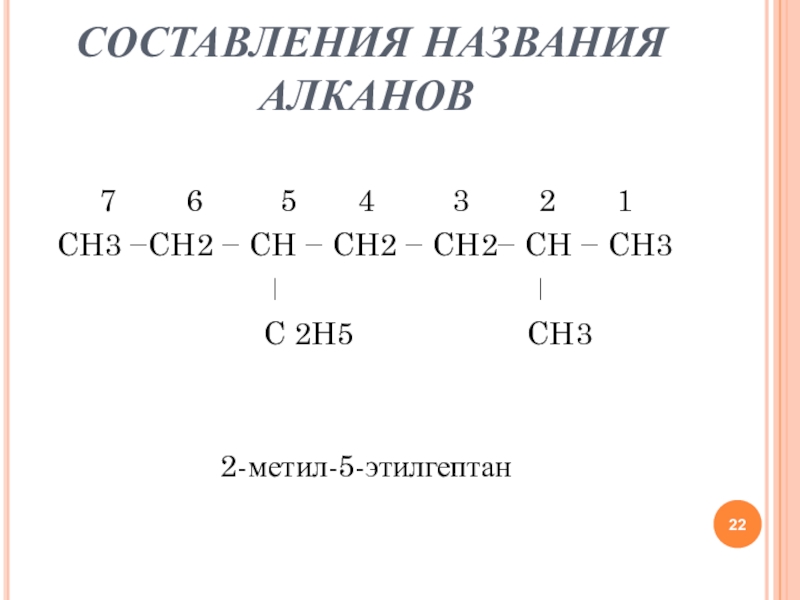
Слайд 22 СОСТАВЛЕНИЯ НАЗВАНИЯ АЛКАНОВ
7 6
5 4 3 2 1
CH3 −CH2 − CH − CH2 − CH2− CH − CH3
ǀ ǀ
C 2H5 CH3
2-метил-5-этилгептан
CH3 −CH2 − CH − CH2 − CH2− CH − CH3
ǀ ǀ
C 2H5 CH3
2-метил-5-этилгептан
Слайд 27ФИЗИЧЕСКИЕ СВОЙСТВА
С1 – С4 – газы,
С5 – С15 –
жидкости,
С16 – ∞ – твердые вещества
Газы и твердые алканы запаха не имеют, жидкие имеют бензиновый запах. Легче воды. Плохо растворимы в воде .
С16 – ∞ – твердые вещества
Газы и твердые алканы запаха не имеют, жидкие имеют бензиновый запах. Легче воды. Плохо растворимы в воде .
Слайд 30РЕАКЦИЯ ЗАМЕЩЕНИЯ
СН4 + Cl2 = CH3Cl +HCl
хлорметан
CH3Cl
+Cl2 = CH2Cl2 +HCl
дихлорметан
CH2Cl2+ Cl2 = CHCl3+ HCl
трихлорметан
CHCl3 + Cl2 = CCl4+ HCl
тетрохлорметан
дихлорметан
CH2Cl2+ Cl2 = CHCl3+ HCl
трихлорметан
CHCl3 + Cl2 = CCl4+ HCl
тетрохлорметан
Слайд 33РЕАКЦИЯ ДЕГИДРИРОВАНИЯ
Процесс отщепления молекул водорода от молекул органического соединения.
Слайд 34ПОЛУЧЕНИЕ АЛКАНОВ
Получение метана
В п р о м ы
ш л е н н о с т и:
а) из природного газа
б) синтез из оксида углерода (II) и водорода
Ni,300˚C
CO + 3H2 → CH4 ↑ +H2O
а) из природного газа
б) синтез из оксида углерода (II) и водорода
Ni,300˚C
CO + 3H2 → CH4 ↑ +H2O
Слайд 35ПОЛУЧЕНИЕ МЕТАНА
В л а б о р а т о
р и и:
а) гидролиз карбида алюминия
Al4C3 +12H2O → 3CH4 ↑ +4Al(OH)3
б) сплавление солей уксусной кислоты со щелочами
CH3COONa +NaOH (т) → CH4 ↑ +Na2CO3
а) гидролиз карбида алюминия
Al4C3 +12H2O → 3CH4 ↑ +4Al(OH)3
б) сплавление солей уксусной кислоты со щелочами
CH3COONa +NaOH (т) → CH4 ↑ +Na2CO3
Слайд 36ПРИМЕНЕНИЕ
Широко
используются в
качестве
топлива, в том
числе для
двигателей
внутреннего
сгорания.
Слайд 37ПРИМЕНЕНИЕ
1-3 – производство сажи
(1 – картриджи;
2 – резина;
3 – типографическая краска)
4-7
– получение
органических веществ
(4 – растворителей;
5 – хладагентов,
используемых
в холодильных установках;
6 – метанол;
7 - ацетилен)
органических веществ
(4 – растворителей;
5 – хладагентов,
используемых
в холодильных установках;
6 – метанол;
7 - ацетилен)
Слайд 40ДОМАШНЕЕ ЗАДАНИЕ
§3, учить записи в тетрадях.
1. Изготовить шаростержневую модель
молекулы бутана.
2. Составить структурные формулы возможных изомеров гексана дать названия.
3. Выучить определения основных понятий.
2. Составить структурные формулы возможных изомеров гексана дать названия.
3. Выучить определения основных понятий.
Слайд 41ИСТОЧНИКИ ИНФОРМАЦИИ, ПРЕДСТАВЛЕННОЙ В ПРЕЗЕНТАЦИИ
1. О.С. Габриэлян. Химия 10 класс (базовый
уровень) М. «Дрофа»,2008
2.Википедия
3. О.С. Габриэлян, А. В. Яшукова Химия . Методическое пособие. 10 класс (базовый уровень) М. «Дрофа»,2008
2.Википедия
3. О.С. Габриэлян, А. В. Яшукова Химия . Методическое пособие. 10 класс (базовый уровень) М. «Дрофа»,2008