- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Водород (9 класс)
Содержание
- 1. Презентация по химии на тему Водород (9 класс)
- 2. План урокаПоложение водорода в ПС.Строение атома водорода.
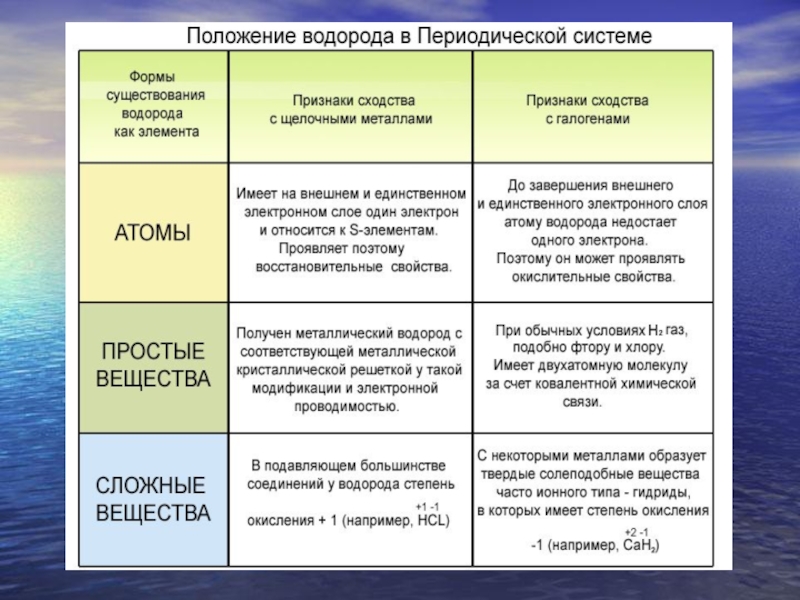
- 3. Положение в ПСХЭВодород – элемент с порядковым
- 4. Слайд 4
- 5. Строение атома водорода.
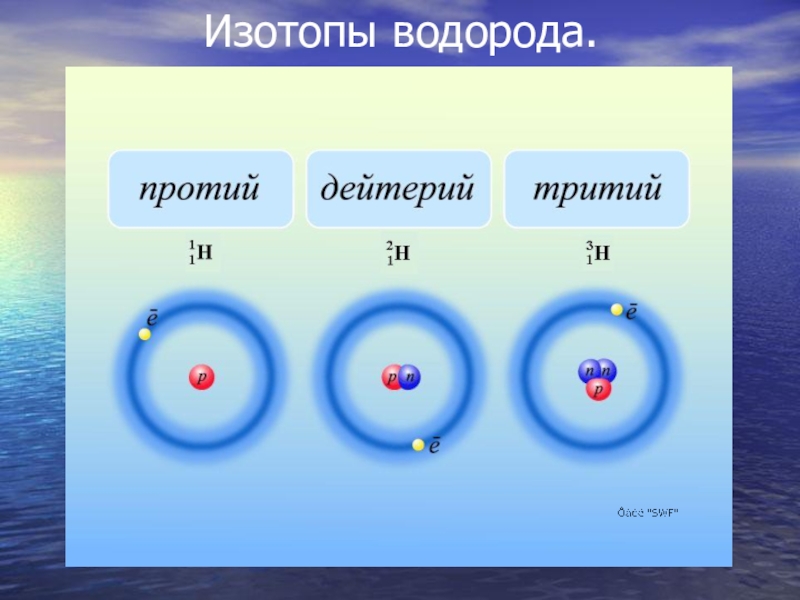
- 6. Изотопы водорода.
- 7. Образование молекулы водорода Атомы образуют связь, осуществляемую
- 8. Физические свойства водородаГаз, без цвета, вкуса, запаха,
- 9. Химические свойства водорода1. Горение водорода2. Взаимодействие водорода
- 10. Применение водорода
- 11. Нахождение водорода в природе
- 12. Получение водорода в лаборатории
План урокаПоложение водорода в ПС.Строение атома водорода. Изотопы.Водород – простое вещество: -физические свойства; -химические свойства: а) взаимодействие с простыми веществами (восстановительные и окислительные свойства) б)взаимодействие со сложными веществами.Применение водорода.Нахождение водорода в природе.Получение
Слайд 2План урока
Положение водорода в ПС.
Строение атома водорода. Изотопы.
Водород – простое вещество:
-физические свойства;
-химические свойства:
а) взаимодействие с простыми веществами (восстановительные и окислительные свойства)
б)взаимодействие со сложными веществами.
Применение водорода.
Нахождение водорода в природе.
Получение водорода:
а) в лаборатории
б) в промышленности
-химические свойства:
а) взаимодействие с простыми веществами (восстановительные и окислительные свойства)
б)взаимодействие со сложными веществами.
Применение водорода.
Нахождение водорода в природе.
Получение водорода:
а) в лаборатории
б) в промышленности
Слайд 3Положение в ПСХЭ
Водород – элемент с порядковым номером 1, его относительная
атомная масса 1,008.
Электронная формула атома водорода 1s¹.
Степень окисления 0;+1;-1.
Водород занимает двойственное положение в периодической системе элементов, его принято размещать и в I и в VII группах в главных подгруппах.
Электронная формула атома водорода 1s¹.
Степень окисления 0;+1;-1.
Водород занимает двойственное положение в периодической системе элементов, его принято размещать и в I и в VII группах в главных подгруппах.
Слайд 7Образование молекулы водорода
Атомы образуют связь, осуществляемую общей для них электронной парой,
для достижения наиболее стабильной электронной конфигурации, которая может быть представлена следующим образом (электроны обозначены точками):
Электронную пару можно обозначить черточкой:
Связь между двумя атомами образуется тогда, когда они приближаются друг к другу на расстояние, достаточное для того, чтобы электроны каждого из них оказались в пределах взаимодействия с ядром другого атома. Связь в молекуле водорода – ковалентная неполярная.
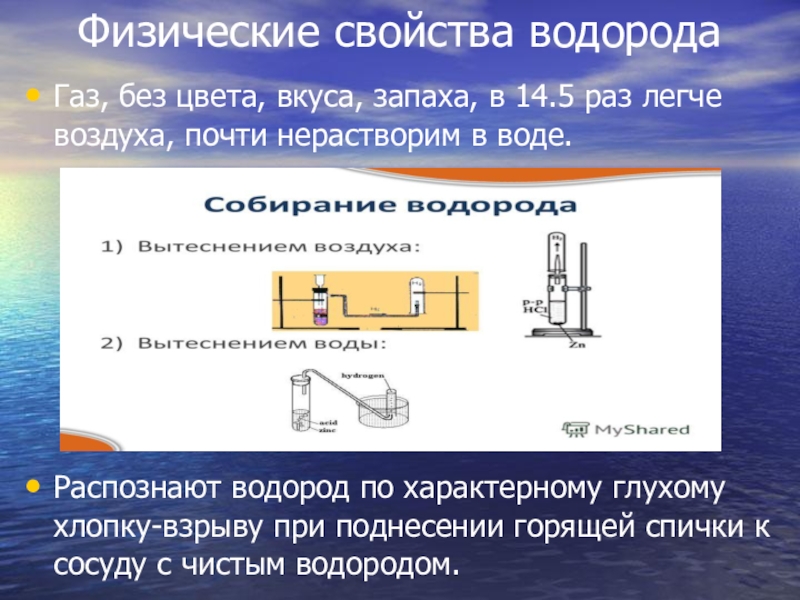
Слайд 8Физические свойства водорода
Газ, без цвета, вкуса, запаха, в 14.5 раз легче
воздуха, почти нерастворим в воде.
Распознают водород по характерному глухому хлопку-взрыву при поднесении горящей спички к сосуду с чистым водородом.
Распознают водород по характерному глухому хлопку-взрыву при поднесении горящей спички к сосуду с чистым водородом.
Слайд 9Химические свойства водорода
1. Горение водорода
2. Взаимодействие водорода с хлором
3. Взаимодействие водорода
с оксидом меди (II)
4. Взаимодействие водорода с активными металлами
4. Взаимодействие водорода с активными металлами