- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Теория электролитической диссоциации
Содержание
- 1. Презентация по химии на тему Теория электролитической диссоциации
- 2. Актуализация знаний 1.Что такое электролиты?Электролитами называются вещества,
- 3. Почему диссоциация электролитов происходит только в воде?
- 4. При растворении в воде электролиты диссоциируют (распадаются)
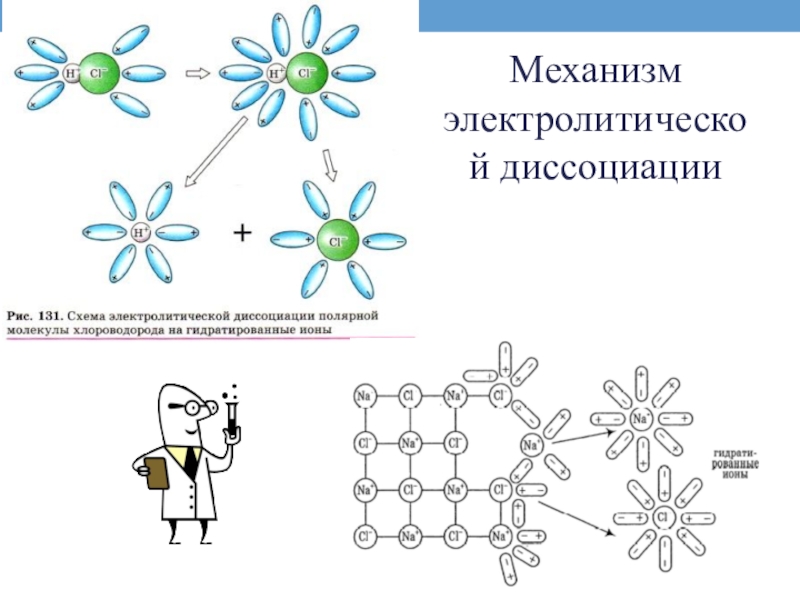
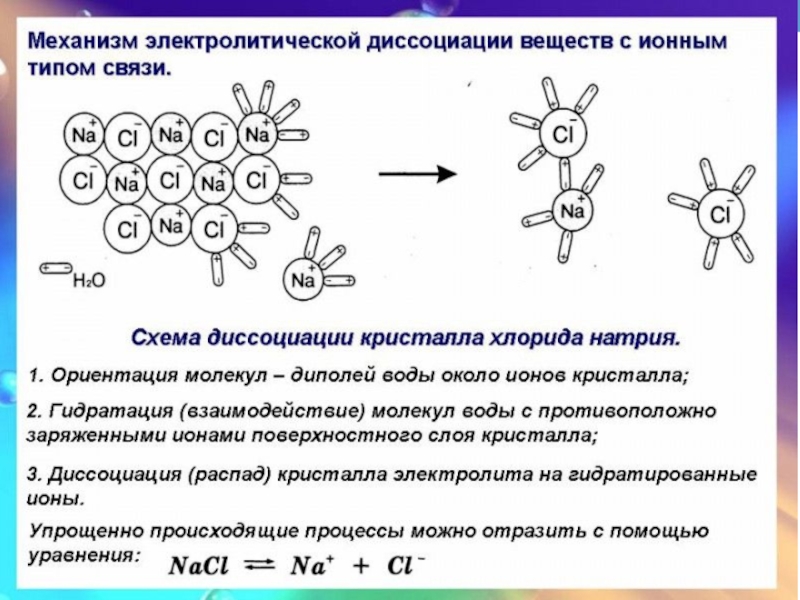
- 5. Механизм электролитической диссоциации
- 6. Слайд 6
- 7. Слайд 7
- 8. Механизм диссоциации веществ с ковалентной полярной связью
- 9. Какие соединения относятся к сильным электролитам, а
- 10. ОДНООСНОВНЫЕ КИСЛОТЫ Диссоциируют в одну ступень
- 11. ОДНОКИСЛОТНЫЕ ОСНОВАНИЯМНОГОКИСЛОТНЫЕ ОСНОВАНИЯдиссоциируют в одну ступеньNaOH NaOH
- 12. СолиНезависимо от числа катионов и анионов кислотного
- 13. Слайд 13
- 14. ЗакреплениеНапишите уравнения диссоциации следующих веществ: HCl, H3PO4, KOH.
- 15. Закрепление изученного материала (самостоятельная работа):1 вариантОтветить на
- 16. Рефлексия:Насколько сложно было работать?Что вызвало наибольшие затруднения?Оцените
- 17. Домашнее задание:Прочитать параграф 36, 37, выучить определения.
- 18. Слайд 18
Слайд 2Актуализация знаний
1.Что такое электролиты?
Электролитами называются вещества, растворы или расплавы которых
Что такое неэлектролиты?
Неэлектролитами называются вещества, растворы или расплавы которых электрический ток не проводят.
Дать определение Электролитической диссоциации.
Распад электролитов на ионы при растворении его в воде или расплавлении называют электролитической диссоциацией.
Слайд 4При растворении в воде электролиты диссоциируют (распадаются) на положительные и отрицательные
Что такое ионы?
Ионы – это атомы или группы атомов, имеющие положительный или отрицательный заряд.
Слайд 9Какие соединения относятся к сильным электролитам, а какие к слабым?
Химические свойства
По характеру образующихся ионов различают три типа электролитов:
Кислоты – это электролиты, которые диссоциируют на катионы водорода и анионы кислотного остатка.
Основания – это электролиты, которые диссоциируют на катионы металла и анионы гидроксогрупп.
Соли – это электролиты, которые диссоциируют на катионы металла и анионы кислотного остатка.
Слайд 10
ОДНООСНОВНЫЕ КИСЛОТЫ
Диссоциируют в одну ступень
HNO3 = H+ + NO3-
Диссоциируют в несколько ступеней
H2SO4
H2SO4 ↔ H+ + HSO4-
HSO4- ↔ H+ + SO42-
Слайд 11
ОДНОКИСЛОТНЫЕ ОСНОВАНИЯ
МНОГОКИСЛОТНЫЕ ОСНОВАНИЯ
диссоциируют в одну ступень
NaOH
NaOH ↔ Na+ + OH-
диссоциируют
Ba(OH)2
Ba(OH)2 ↔ BaOH+ + OH-
BaOH+ ↔ Ba2+ + OH-
Слайд 12Соли
Независимо от числа катионов и анионов кислотного остатка средние соли диссоциируют
Al2(SO4) = 2Al3+ + 3SO42-
Слайд 15Закрепление изученного материала (самостоятельная работа):
1 вариант
Ответить на вопрос: «Почему раствор гидроксида
2 вариант
Ответить на вопрос: «Почему при разбавлении раствора электролита степень его диссоциации увеличивается?»
3 вариант
Докажите, что деление химических связей на ковалентную полярную и ковалентную ионную условно.